Clear Sky Science · ru
Мультиомный анализ сигнальных сетей человека PHACTR1
Почему этот ген сосудов важен для вас
Инфаркты, инсульты и гипертония в конечном счёте зависят от здоровья наших сосудов. Один ген, называемый PHACTR1, неоднократно появлялся в крупных генетических исследованиях этих состояний, но учёные долго не понимали, почему. В этом исследовании применили широкий «многоуровневый» подход к человеческим клеткам, чтобы проследить, чем на самом деле занимается PHACTR1, и выяснили, как он может влиять на рост клеток, использование энергии и обращение с железом — процессы, которые в конечном счёте формируют здоровье артерий.
Общий обзор внутри клеток
Вместо изучения одной молекулы за раз исследователи использовали стратегию, называемую мульти-омикой — одновременное измерение тысяч РНК, белков, малых метаболитов и липидов в клетках. Они модифицировали человеческие клетки так, чтобы те вырабатывали либо больше PHACTR1, либо имели пониженное выражение гена, имитируя естественные генетические различия у людей. Сравнивая эти изменённые клетки с нормальными контрольными в четырёх молекулярных слоях и обрабатывая данные с помощью сложного программного обеспечения для анализа путей, авторы построили глобальную карту того, как изменение PHACTR1 распространяется по внутренним механизмам клетки. 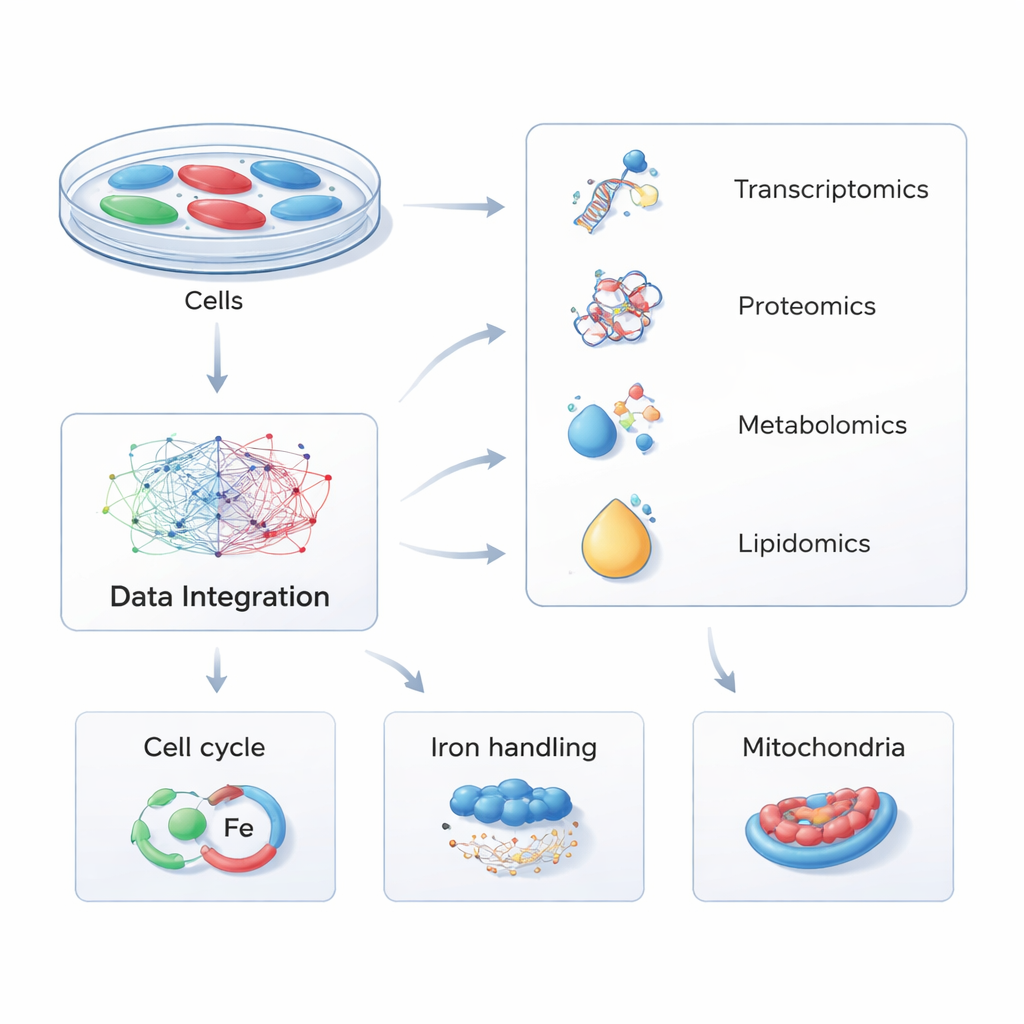
Не только клеточный скелет: контроль цикла роста
Ранее PHACTR1 в основном ассоциировали с организацией клеточного каркаса из актиновых волокон. Новые данные показали, что он также существенно влияет на контроль клеточного цикла — хореографию копирования ДНК и деления клеток. Клетки с повышенным PHACTR1 выходили из отдыхающей фазы G1 и накапливались в фазах, связанных с копированием ДНК и предделением, при этом меньше клеток успешно переходили в полноценный митоз. Были изменены ключевые регуляторы, такие как Cyclin B1, Cdt1 и другие белки клеточного цикла. Повторив эксперименты на первичных эндотелиальных клетках человека — клетках, выстилающих сосуды, — команда вновь заметила изменения в основных регуляторах клеточного цикла. Это указывает на то, что PHACTR1 помогает решать, когда сосудистые клетки отдыхают, делятся или останавливаются, — баланс, жизненно важный как для восстановления стенок сосудов, так и для образования опасных разрастаний тканей.
Управление железом и защита от повреждений
Интеграция мульти-омных данных также указала на пути, связанные с железом, и на специализированную форму железозависимой гибели клеток — ферроптоз. Хотя клетки не умирали активным ферроптозом, повышение PHACTR1 снижало уровни основных белков, работающих с железом, включая тяжёлую цепь ферритина (основную оболочку для хранения железа) и гемооксигеназу 1 (которая перерабатывает железо из гема). В первичных эндотелиальных клетках PHACTR1 аналогично изменял эти белки и ключевые защитные механизмы против окислительного повреждения. Поскольку неуправляемое железо может подпитывать воспаление, оксидативный стресс и нестабильные бляшки в артериях, результаты указывают, что PHACTR1 может настраивать то, как сосудистые клетки хранят и детоксифицируют железо, что потенциально влияет на восприимчивость к некоторым сосудистым заболеваниям.
Митохондрии, энергия и здоровье артерий
Ещё одним сюрпризом стала роль PHACTR1 в митохондриях — электростанциях клетки. Команда обнаружила белок PHACTR1 в изолированных митохондриях и заметила, что изменение его уровня перестраивает митохондриальную сеть. При высоком PHACTR1 митохондрии становились более удлинёнными, и белок Drp1 подвергался химической модификации в сайте, снижающем их дробление. Уровни анкера-скелетного белка AKAP1, помогающего организовать сигналы на поверхности митохондрий, менялись в такт с PHACTR1. Эти структурные сдвиги соответствовали изменениям в производстве энергии: высокий PHACTR1 снижал митохондриальное производство АТФ и был связан с накоплением определённых молекул, производных жирных кислот, указывающих на замедленное сжигание жиров, тогда как низкий PHACTR1 смещал клетки в сторону большей зависимости от гликолиза — сжигания сахара. Анализ образцов человеческих артерий показал, что PHACTR1 и AKAP1 имеют тенденцию к совместной активации, связывая эту митохондриальную цепь управления непосредственно с реальными кровеносными сосудами. 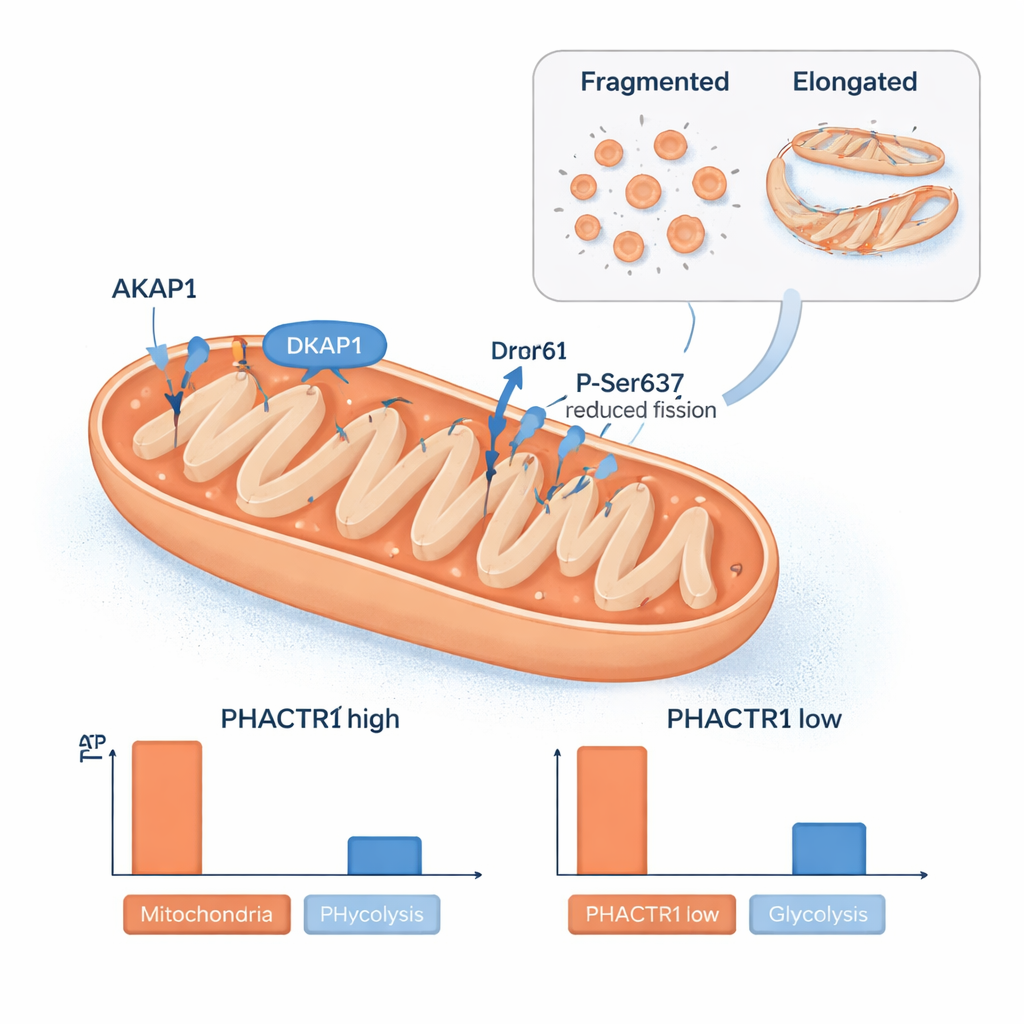
Что всё это означает для сосудов
В целом работа показывает, что PHACTR1 — не ген с одной функцией, а мастер‑координатор, влияющий на то, как сосудистые клетки делятся, хранят железо и обеспечивают себя энергией. Проследив эти связи через тысячи молекул, исследование помогает объяснить, почему естественные вариации в PHACTR1 связаны с таким широким спектром сосудистых заболеваний — от ишемической болезни сердца до спонтанных разрывов артерий и мигрени. Для неспециалистов суть в том, что ген, отмеченный человеческой генетикой, теперь сопоставлен с конкретными клеточными поведениями, которые влияют на рост бляшек, стабильность сосудов и энергетический баланс. В долгосрочной перспективе понимание сетей, контролируемых PHACTR1, может открыть путь к более точным терапиям, которые скорректируют клеточные циклы, обращение с железом или митохондриальную функцию в пользу здоровья у людей, подверженных сердечно‑сосудистым заболеваниям.
Цитирование: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Ключевые слова: PHACTR1, заболевания сосудов, мульти-омика, митохондрии, метаболизм железа