Clear Sky Science · ru
Таргетирование PAK4 усиливает вызванную гемцитабином пироптозу при раке поджелудочной железы через ось NLRP1/caspase-3/GSDME
Почему важна «огненная» смерть раковых клеток
Рак поджелудочной железы входит в число самых смертоносных опухолей, и даже наши лучшие химиопрепараты часто теряют эффективность из‑за развития резистентности. В этом исследовании рассматривается неожиданный поворот: тот же препарат гемцитабин может убивать раковые клетки более взрывным, воспалительным способом — пироптозом, если отключить ключевой молекулярный «тормоз» PAK4. Понимание и таргетирование этого тормоза может повысить эффективность существующих лечений для многих пациентов.
Упорная опухоль, которая игнорирует терапию
Аденокарцинома протоков поджелудочной железы обычно диагностируется на поздних стадиях и плохо отвечает на лечение, поэтому гемцитабин остается опорным препаратом, несмотря на ограничения. Гемцитабин обычно вызывает апоптоз — аккуратную, бесшумную форму программируемой гибели клеток. Но более половины исследованных опухолей поджелудочной железы экспрессировали высокий уровень белка GSDME, который способен превратить тихую гибель в пироптоз — быструю «взрывообразную» гибель с повреждением мембраны клетки и выделением провоспалительных сигналов. Это поставило важный вопрос: если опухоли вообще способны на пироптоз, почему многие из них все же устойчивы к гемцитабину?
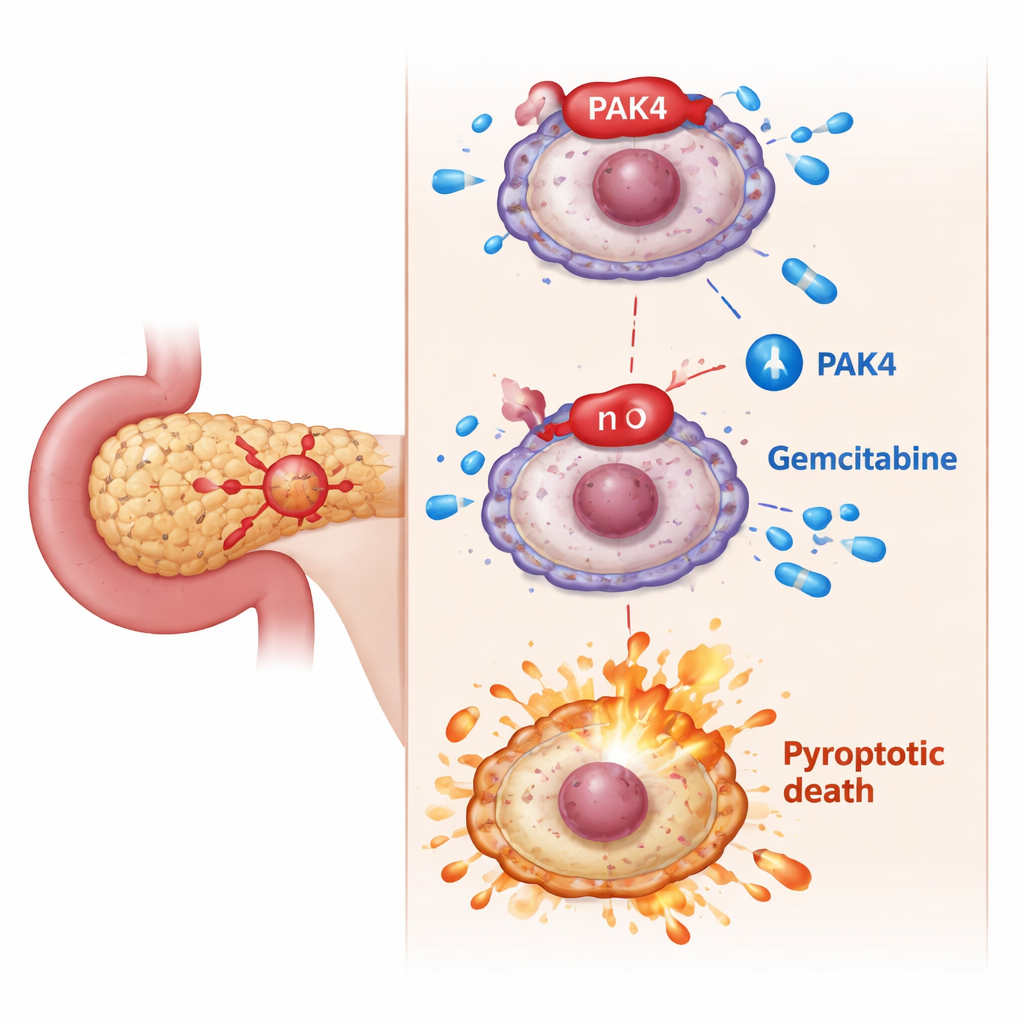
Скрытый тормоз: PAK4 блокирует «огненную» смерть клеток
Исследователи сосредоточились на PAK4 — протеине, стимулирующем рост, который часто гиперактивен при раке поджелудочной и связывается с плохим ответом на гемцитабин. В клеточных экспериментах клетки с высоким уровнем PAK4 было сложнее уничтожить гемцитабином. Когда PAK4 снижали, гемцитабин внезапно становился гораздо более летальным: клетки демонстрировали классические признаки пироптоза — набухание, пузыриобразные выпячивания, разрыв мембран и повышенный выход внутриклеточного содержимого. На молекулярном уровне этот сдвиг зависел от расщепления GSDME в активный фрагмент ферментом caspase‑3. Блокирование caspase‑3 предотвращало активацию GSDME и пироптоз, подтверждая, что PAK4 обычно действует как сдерживающий фактор этого пути гибели.
Как PAK4 нейтрализует систему тревоги клетки
Углубившись в механизм, ученые обнаружили, что PAK4 не действует непосредственно на GSDME. Вместо этого он саботирует вышестоящий «датчик тревоги» — NLRP1. У пациентов более высокий уровень NLRP1 ассоциировался с лучшей выживаемостью, что указывает на его роль в контроле опухолей. В клетках удаление NLRP1 резко уменьшало гибель при обработке гемцитабином и активацию GSDME, показывая, что NLRP1 подпитывает механизм пироптоза. Уровни PAK4 и NLRP1 в опухолевых образцах были обратно пропорциональны: при высоком PAK4 NLRP1 был низким. Исследование показало, что активный PAK4 действует через другой белок, E3‑лигазу Mdm2, помечая NLRP1 для разрушения системой утилизации клетки. Маркируя NLRP1 таким образом, PAK4 предотвращает активацию каскада через caspase‑9 и caspase‑3, который в норме приводил бы к пироптозу, опосредованному GSDME.
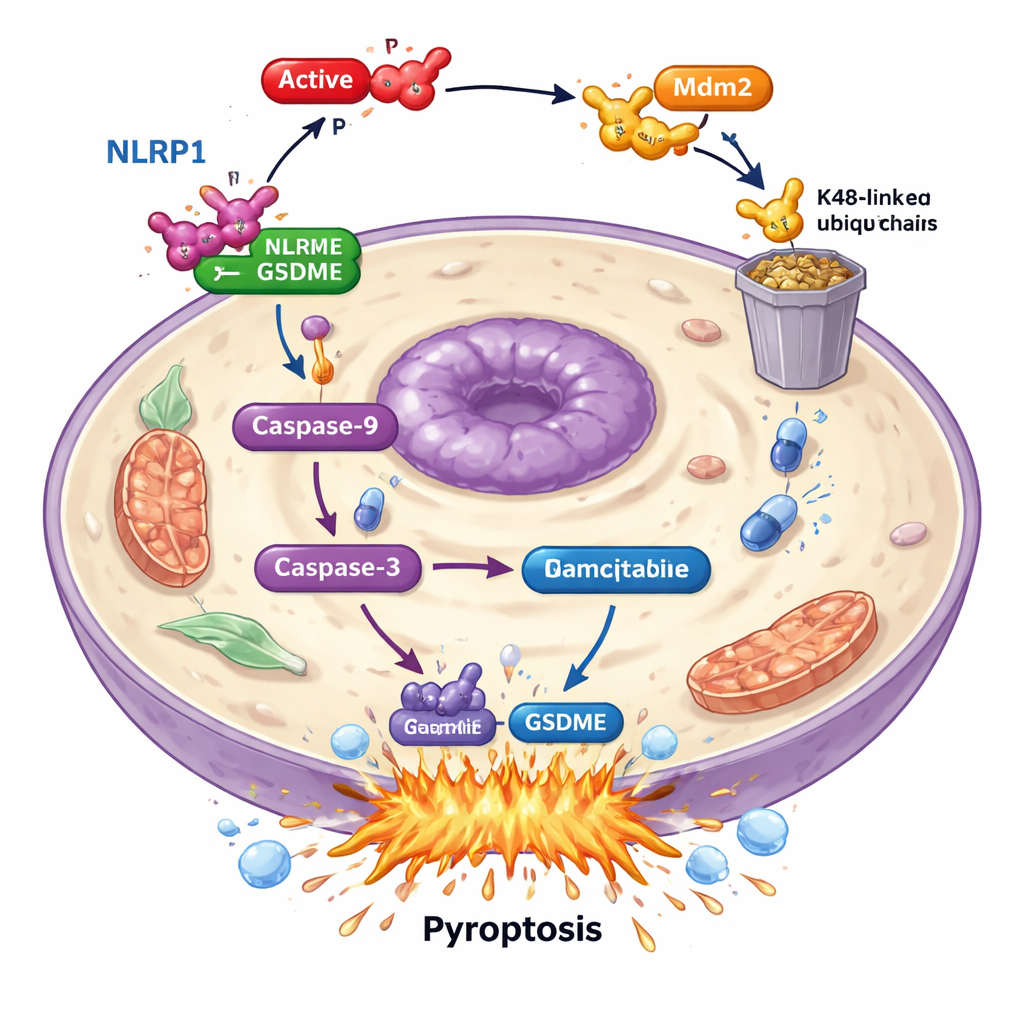
Отключение PAK4 для усиления химиотерапии
Поскольку PAK4 действует как тормоз пироптоза, команда проверила, можно ли блокировать его активность, чтобы вернуть гемцитабину убойную силу. Они использовали малую молекулу‑ингибитор PAK4 PF‑3758309. Сам по себе этот ингибитор уже сдвигал клетки поджелудочной железы в сторону пироптоза, увеличивая активацию caspase‑3, расщепление GSDME и разрушение мембран. В комбинации с гемцитабином эффект усиливался: больше клеток погибало через пироптоз, а молекулярные маркеры пути были усилены. В модельных мышах с человеческими опухолями поджелудочной как снижение PAK4, так и лечение ингибитором PAK4 делали гемцитабин более эффективным в уменьшении опухолей и усиливали маркеры пироптоза в ткани опухоли.
Что это значит для пациентов и будущих методов лечения
Проще говоря, работа выявляет молекулярный замок — PAK4 — который удерживает клетки рака поджелудочной от гибели в особенно разрушительной форме при химиотерапии. Отключив PAK4, возможно, удастся перевести опухоли, леченные гемцитабином, в состояние пироптоза, сделав препарат более эффективным и потенциально активируя иммунную систему против рака. Хотя нужны дополнительные исследования на моделях, полученных от пациентов, и клинические испытания, исследование предлагает ясную стратегию: таргетировать путь PAK4–Mdm2–NLRP1–GSDME, чтобы преобразовать резистентные опухоли в чувствительные, используя уже имеющиеся препараты в более продуманных сочетаниях.
Цитирование: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Ключевые слова: рак поджелудочной железы, резистентность к гемцитабину, пироптоз, PAK4, таргетная терапия