Clear Sky Science · ru
Целенаправленное блокирование сплайсинга генов может нарушать регуляцию заложенных в интронах первичных микроРНК
Скрытые послания внутри наших генов
Многие новые генные терапии действуют, корректируя РНК‑сообщения в клетках, но эти РНК нередко содержат дополнительные «заметки на полях», которые ученые только начинают понимать. В этой работе показано, что препараты, разработанные для исправления дефектного сплайсинга генов, могут случайно повышать уровни крошечных регуляторных РНК, спрятанных внутри интронов — некодирующих участков между сегментами генов, — с неожиданными последствиями для формирования связей в мозге и развития организма.
Генные терапии, переписывающие РНК
Антисэнсовые олигонуклеотиды (АСО) — короткие синтетические фрагменты генетического материала, которые связываются с РНК и меняют то, как она читается или обрабатывается. Несколько АСО уже проходят испытания или используются при редких наследственных заболеваниях, в особенности вызванных нарушением сплайсинга — этапа, на котором соединяются кодирующие участки гена. Большинство тестов безопасности сосредоточено на том, восстанавливает ли АСО правильный белок и не вызывает ли явные побочные эффекты. Но многие гены также несут некодирующие РНК, включая микроРНК, внутри своих интронов. Эти крошечные молекулы сильно регулируют активность генов, и до половины известных микроРНК у позвоночных получается из интронов. Новое исследование задается вопросом: что происходит с такими встроенными микроРНК, когда мы принудительно меняем сплайсинг с помощью АСО?
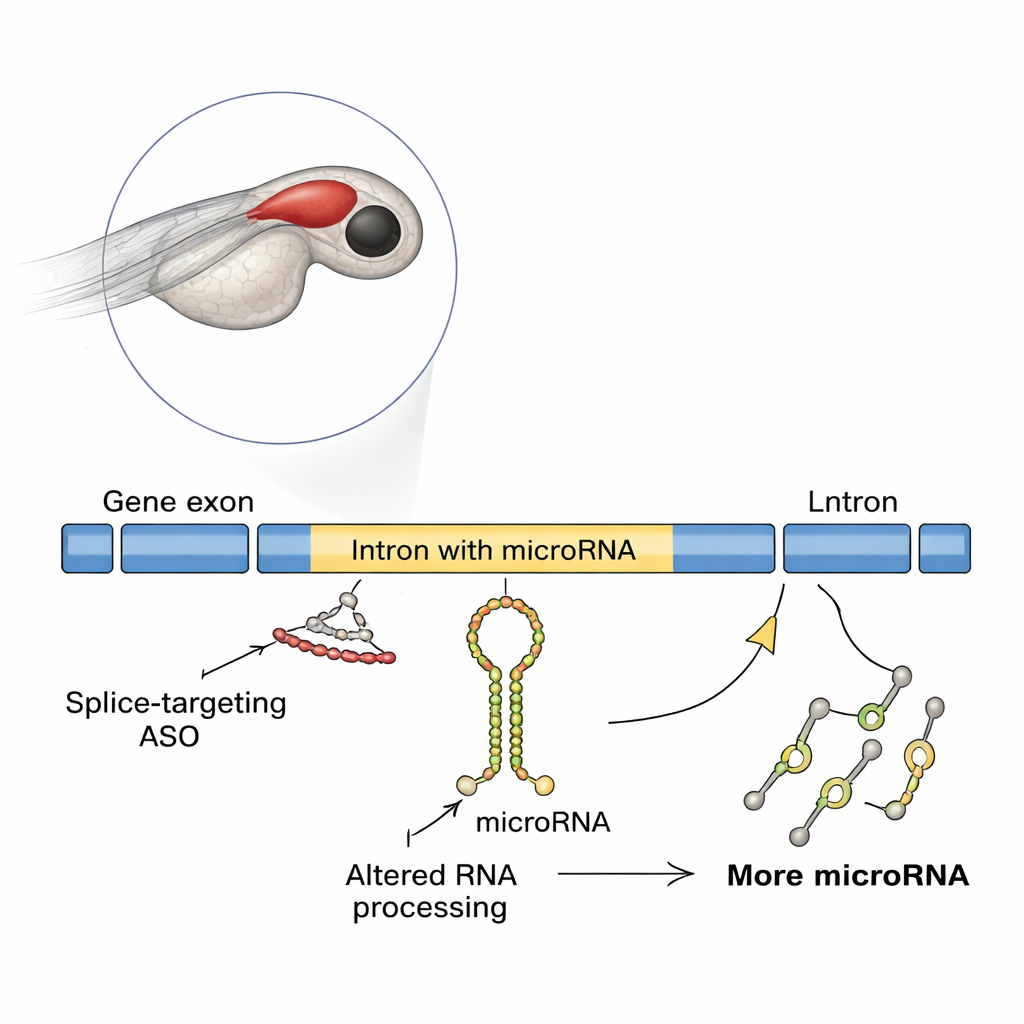
Неожиданный эффект в развивающемся мозге рыбы
Исследователи использовали модельный организм — данио‑рерио (zebrafish) — чьи прозрачные эмбрионы упрощают наблюдение за развитием мозга. Они сосредоточились на гене slit3, который помогает направлять нервные волокна и содержит микроРНК mir-218a-1 в одном из своих интронов. Когда команда блокировала старт трансляции slit3, развитие аксонов, секретирующих гормоны гипофиза, выглядело нормально. Но при применении другого АСО, блокирующего сплайсинг в конкретном сайсплайс‑сайте slit3, аксоны, направляющиеся к заднему гипофизу, резко уменьшились, несмотря на то, что число окситоциновых нейронов осталось прежним. Молекулярные анализы показали, что это сплайс‑блокирующее АСО вызвало ретенцию интрона в РНК гена, неожиданно повышая уровни транскрипта slit3, его длинного интрона и первичного транскрипта интрон‑вложенной mir-218a-1.
Дефекты обусловлены микроРНК, а не потерей белка
Чтобы выяснить причину проблем с аксонами, авторы сравнили несколько сценариев. Блокада зрелой mir-218a-1 сама по себе не меняла уровни slit3, а отдельный АСО, направленный на другой сайт сплайсинга рядом с микроРНК, не вызывал аксональных дефектов и не повышал mir-218a-1. Ключевой эксперимент: сочетание сплайс‑блокирующего АСО для slit3 с АСО, нейтрализующим mir-218a-1, в значительной степени восстанавливало аксонную проводку. Аналогично, у генетически лишенных mir-218a-1 данио‑рерио то же сплайс‑блокирующее АСО переставало вызывать дефекты аксонов, тогда как инъекция синтетического мимика mir-218a могла воспроизвести фенотип в нормальных особях. Эти эксперименты указывают на повышение интронной микроРНК — а не на укороченный белок Slit3 — как главный фактор развития нарушений.
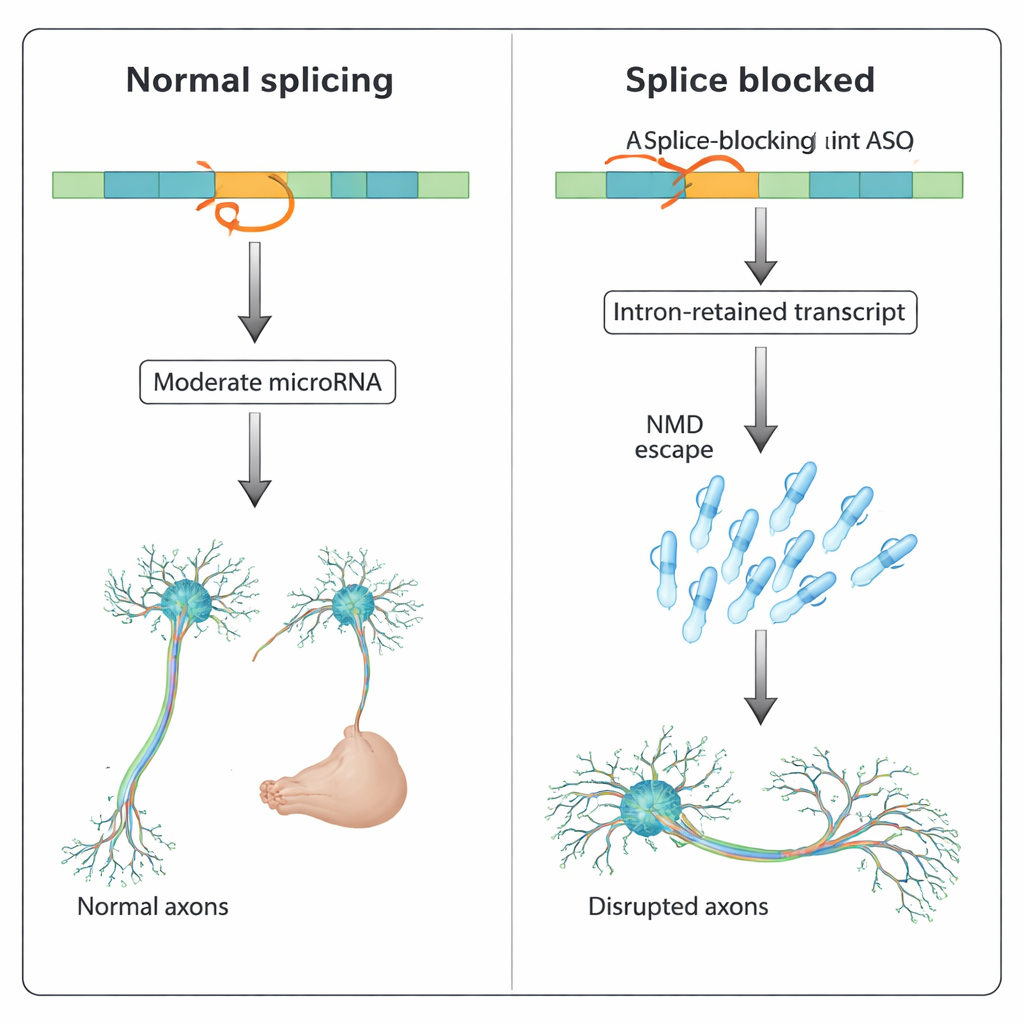
Более широкая картина в нескольких генах
Команда затем проверила, уникален ли этот эффект для slit3. Они просканировали геном данио‑рерио и обнаружили десятки кодирующих белок генов, которые содержат интронные микроРНК, многие из которых участвуют в развитии и сигнальных путях. Два таких гена, pank2 и dnm2a, ранее демонстрировали тяжёлые нарушения развития при блокировании их сплайсинга АСО — включая накопление жидкости в мозге, отёк сердца и деформации тела — проблемы, которые не повторялись в генетических нокаутах тех же генов. В настоящем исследовании совместная инъекция АСО, специально блокирующих интронные микроРНК mir-103 (в pank2) или mir-199-5p (в dnm2a), частично спасала эти фенотипы, индуцированные АСО. В некоторых случаях блокада микроРНК также восстанавливала экспрессию хозяевского гена, в то время как в других — нет, что указывает на то, что повышенная активность микроРНК сама по себе может быть вредной, даже когда суммарные уровни меняются лишь умеренно.
Что это значит для будущих терапий
Результаты показывают, что АСО, нацеленные на сплайсинг, могут вызывать не только пропуск экзонов или ретенцию интронов: они могут стабилизировать интрон‑удерживаемые транскрипты, которые ускользают от клеточных систем контроля качества, и повышать уровни первичных интронных микроРНК, которые затем неправильно регулируют сети целевых генов. В развивающихся нейронах такая неконтролируемая активность микроРНК может искажать рост аксонов и формирование связей. Для разработчиков лекарств это означает, что необычные или «внецелевые» фенотипы в животных испытаниях не всегда происходят от общетоксичных путей, таких как активация p53, а могут быть следствием непреднамеренных эффектов на скрытые интронные РНК. Тщательное сопоставление АСО, блокирующих трансляцию, и АСО, блокирующих сплайсинг, а также мониторинг экспрессии интронных микроРНК помогут выявлять эти риски на ранних этапах и улучшать дизайн АСО до их внедрения для пациентов.
Цитирование: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Ключевые слова: антисэнсовые олигонуклеотиды, микроРНК, сплайсинг РНК, развитие цефалоподобных (zebrafish) эмбрионов, безопасность генной терапии