Clear Sky Science · ru
Нимболид смягчает ОРДС и язвенный колит, нарушая активацию инфламмасомы NLRP3
Почему важно усмирять неконтролируемое воспаление
Многие серьёзные заболевания — от жизнеугрожающей недостаточности лёгких до болезненного поражения кишечника — вызываются не только микробами или травмами, но и чрезмерной реакцией собственной иммунной системы. В этом исследовании проверяли, может ли природное соединение нимболид, выделенное из дерева ним, выступать в роли точного «тормоза» для одного мощного воспалительного механизма в иммунных клетках, что потенциально открывает более безопасный путь лечения состояний, таких как острый респираторный дистресс‑синдром (ОРДС) и язвенный колит.
Тревожная сигнализация внутри иммунных клеток
В центре истории — молекулярная «сигнализация тревоги», называемая инфламмасомой NLRP3. Когда иммунные клетки обнаруживают угрозу — сигналы от инфекции, повреждённой ткани или кристаллов — она может собираться как конструкция из трёх частей: сенсор NLRP3, адаптер ASC и фермент Caspase‑1. После сборки этот комплекс активирует мощные медиаторы, такие как IL‑1β и IL‑18, и может запускать огненную форму гибели клетки, называемую пироптозом. Хотя такая реакция помогает устранять угрозы, её гиперактивация способствует хроническим и острым заболеваниям, включая артрит, осложнения при диабете, болезнь Альцгеймера, ОРДС и воспалительные болезни кишечника. Фармацевтические компании пытались усмирить NLRP3 синтетическими соединениями, но многие кандидаты сталкивались с токсичностью, побочными эффектами или неблагоприятной фармакологией, что подчёркивает потребность в более безопасных и селективных ингибиторах.
Открытие мощного растительного ингибитора
Исследователи протестировали 126 природных соединений, чтобы выяснить, какие лучше всего блокируют выброс IL‑1β из иммунных клеток мышей. Нимболид выделился — он снижал секрецию IL‑1β более чем на 80% при протестированных дозах. Дальнейшие эксперименты показали, что нимболид сильно уменьшал активацию Caspase‑1, выброс IL‑1β и пироптоз в макрофагах, полученных из костного мозга мышей, с эффективностью, сравнимой с эталонным препаратом MCC950. Важно, что нимболид не угнетал выделение других иммунных медиаторов, таких как IL‑6, что указывает на более целенаправленное действие, а не на общее подавление иммунитета. При испытаниях на разных стимулах, активирующих NLRP3 — таких как ATP, нигерицин, кристаллы алюм и имиквимод — нимболид постоянно уменьшал активность инфламмасомы, включая исследования на человеческих клетках THP‑1. В то же время он не блокировал две родственные инфламмасомы, AIM2 и NLRC4, что подчёркивает его специфичность в отношении NLRP3.
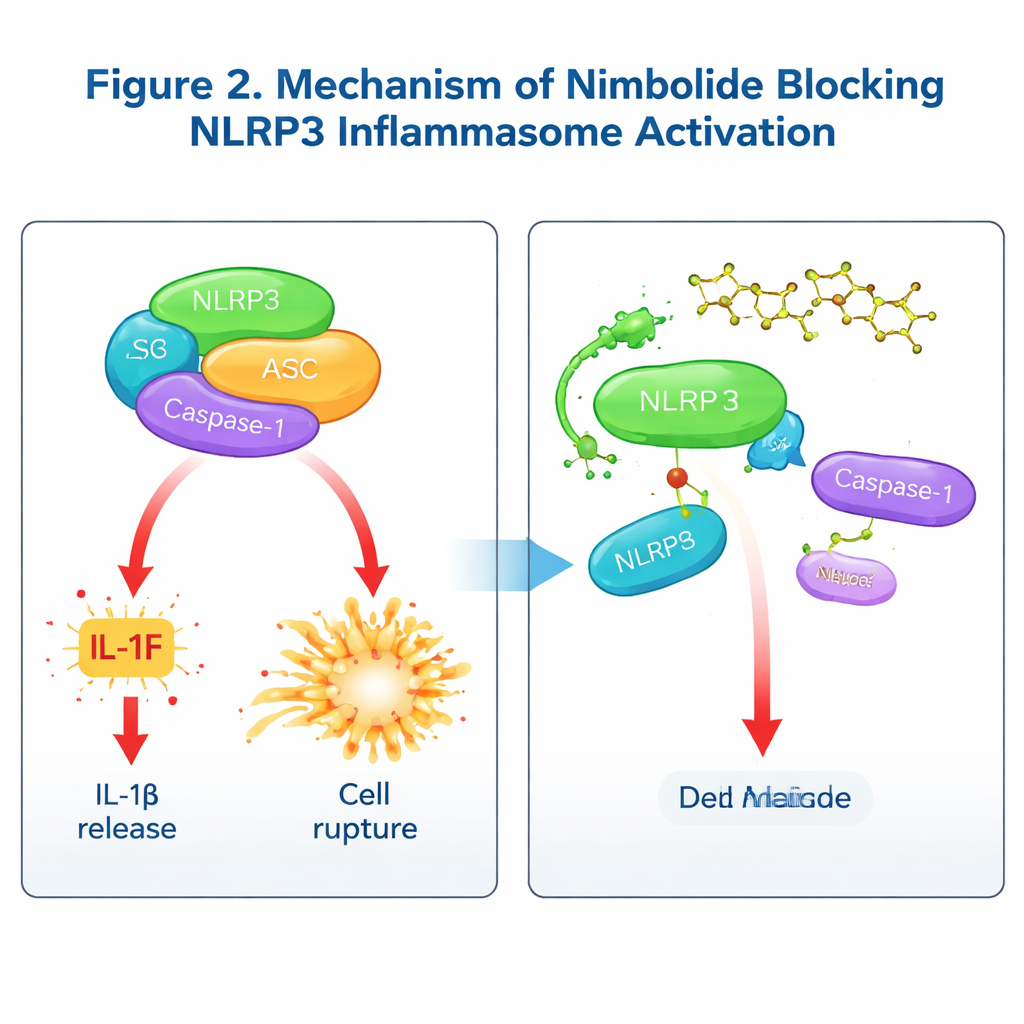
Как нимболид блокирует воспалительный механизм
Чтобы понять механизм действия нимболида, команда проверила, вмешивается ли он в ранние этапы «прайминга», контролируемые путём NF‑κB, или в поздние стадии, когда инфламмасома физически собирается. Кратковременное лечение, проведённое после прайминга, не затронуло ключевые прайминговые сигналы и экспрессию генов, но при этом всё ещё уменьшало IL‑1β и активацию Caspase‑1, показывая, что нимболид действует преимущественно на этапе сборки. Тщательные биохимические тесты выявили, что нимболид не изменяет потоки калия или кальция, повреждение митохондрий или взаимодействие NLRP3 с вспомогательным белком NEK7. Вместо этого он нарушает важное взаимодействие между NLRP3 и ASC, снижает формирование кластеров ASC («спеков») и препятствует образованию высоко порядка олигомеров NLRP3. С помощью методов связывания и молекулярного моделирования авторы показали, что нимболид напрямую присоединяется к участку NACHT NLRP3 на конкретной аминокислоте — лизине 565. При мутации этого сайта нимболид больше не мог защищать NLRP3 от деградации или разрывать его связь с ASC, что подтвердило роль Lys565 как ключевой точки присоединения. Примечательно, что в то время как другие препараты часто нацеливаются на ATP‑азную активность NLRP3, нимболид блокирует сборку без влияния на использование ATP, демонстрируя иной механизм действия.
Испытания нимболида при заболеваниях лёгких и кишечника
Затем команда проверила, переносится ли молекулярный эффект в реальные модели болезни. У мышей, которым вводили бактериальный токсин для индукции ОРДС, лечение нимболидом до воздействия уменьшало повреждение лёгочной ткани, скопление жидкости и утечку белка в воздушные пространства. В лёгких было меньше вторгшихся иммунных клеток, а уровни IL‑1β в лёгочной ткани и крови были снижены. Похожие преимущества наблюдались и в модели, где токсин доставляли непосредственно в дыхательные пути. В отдельной модели язвенного колита, когда мыши пили химическое вещество, повреждающее толстую кишку, нимболид ограничивал потерю веса, улучшал консистенцию стула и показатели кровоточивости, сохранял длину кишечника и уменьшал микроскопические признаки воспаления и эрозии тканей, а также снижал IL‑1β в толстой кишке. Существенно, в генетически модифицированных мышах без NLRP3 течение болезни уже было более лёгким, и нимболид не давал дополнительной пользы, что подчёркивает, что его защитное действие зависит от блокирования NLRP3.
Что это может означать для будущих методов лечения
Для неспециалистов главное — нимболид действует как умный тормоз на одном из самых мощных воспалительных переключателей организма. Прикрепляясь к точечному участку NLRP3 и предотвращая сборку инфламмасомы, он успокаивает чрезмерное воспаление в лёгких и кишечнике, не выключая при этом иммунную защиту в целом. Хотя нимболиду ещё предстоит доработка по таким параметрам, как стабильность и способы доставки, чтобы он мог стать лекарством, эта работа позиционирует его как перспективную отправную точку и план для разработки следующего поколения препаратов против заболеваний, вызванных NLRP3, таких как ОРДС и язвенный колит.
Цитирование: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Ключевые слова: нимболид, инфламмасома NLRP3, воспаление, острый респираторный дистресс‑синдром, язвенный колит