Clear Sky Science · ru
Эпигеномное исследование ассоциаций циркулирующего интерлейкина‑6 связывает метилирование ДНК с иммунометаболическим и воспалительным здоровьем
Почему это важно для повседневного здоровья
Хроническое низкоуровневое воспаление незаметно формирует наш риск заболеваний, таких как диабет 2‑го типа, сердечные болезни и воспалительные заболевания кишечника. Ключевым звеном в этом процессе является белок‑сигнализатор в крови — интерлейкин‑6 (IL‑6). В этом исследовании задают фундаментальный вопрос: как IL‑6 взаимодействует с нашим эпигеномом — химическими метками на ДНК, которые помогают регулировать активность генов — и что это означает для нашего долгосрочного здоровья?
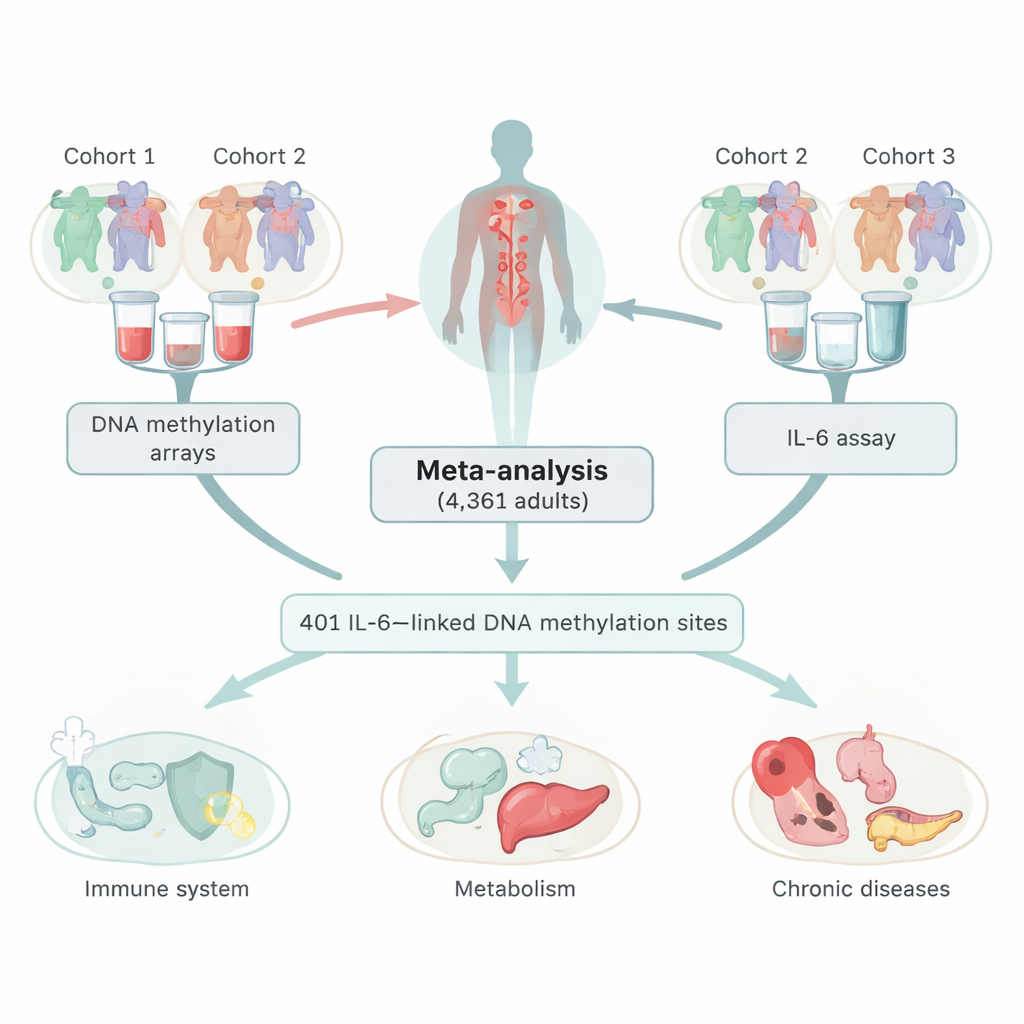
Изучение химических меток на ДНК
Исследователи объединили данные из трёх крупных европейских исследований, охвативших 4 361 взрослого человека, сдавшего образцы крови. В этих образцах они измеряли как уровень IL‑6, так и метилирование ДНК — распространённую химическую метку на ДНК, способную усиливать или ослаблять активность генов без изменения самого генетического кода. Просканировав более 400 000 сайтов по всему геному, они выявили 401 локус, где уровни метилирования коррелировали с концентрацией IL‑6 в крови. Большинство этих сайтов показывали обратную зависимость: более высокий IL‑6 сопровождался более низким метилированием в этих участках. Команда тщательно проверяла, что эти связи не являются простыми побочными эффектами курения, различий в составах клеток крови или другого маркёра воспаления — С‑реактивного белка (CRP).
Связь воспаления с метаболизмом и болезнями
Далее авторы проверили, совпадают ли эти сайты, связанные с IL‑6, с сигналами, обнаруженными в других крупных эпигенетических исследованиях. Они обнаружили сильное обогащение черт с воспалительным или метаболическим компонентом, включая индекс массы тела, липидный профиль, кровяное давление, уровень сахара в крови, диабет 2‑го типа, хронические заболевания почек, а также психиатрические и стресс‑связанные состояния. Многие из тех же сайтов метилирования ранее связывали с CRP, но выявленные шаблоны указывали, что IL‑6 и CRP несут частично разные эпигенетические подписи. Иными словами, химические метки, ассоциированные с IL‑6, не являются просто «копией» меток, связанных с CRP, и могут давать дополнительную информацию о воспалительном и метаболическом состоянии человека.
Где в геноме происходят изменения
Чтобы понять возможную функцию этих сайтов метилирования, команда сопоставила их с известными регуляторными регионами генома. Они обнаружили, что сайты, связанные с IL‑6, были сосредоточены в активных элементах управления, таких как энхансеры — участки ДНК, помогающие включать гены — а не в неактивных регионах. Эти сайты также находились рядом с последовательностями связывания транскрипционных факторов, которые прямо регулируют IL‑6 и реакции на стресс, включая NF‑κB, Atf4, CHOP и Nrf2. Сопоставляя данные о метилировании с крупными наборами данных об экспрессии генов, исследователи связали более 400 генов с участками, ассоциированными с IL‑6. Многие из этих генов находятся в центре иммунного и метаболического контроля — среди них SOCS3, IL6R, AIM2, IFI16, MTOR и RORC — и участвуют в путях, запускающих активацию и расход энергии в специализированном типе Т‑клеток (Th17), вовлечённых в хронические воспалительные заболевания.
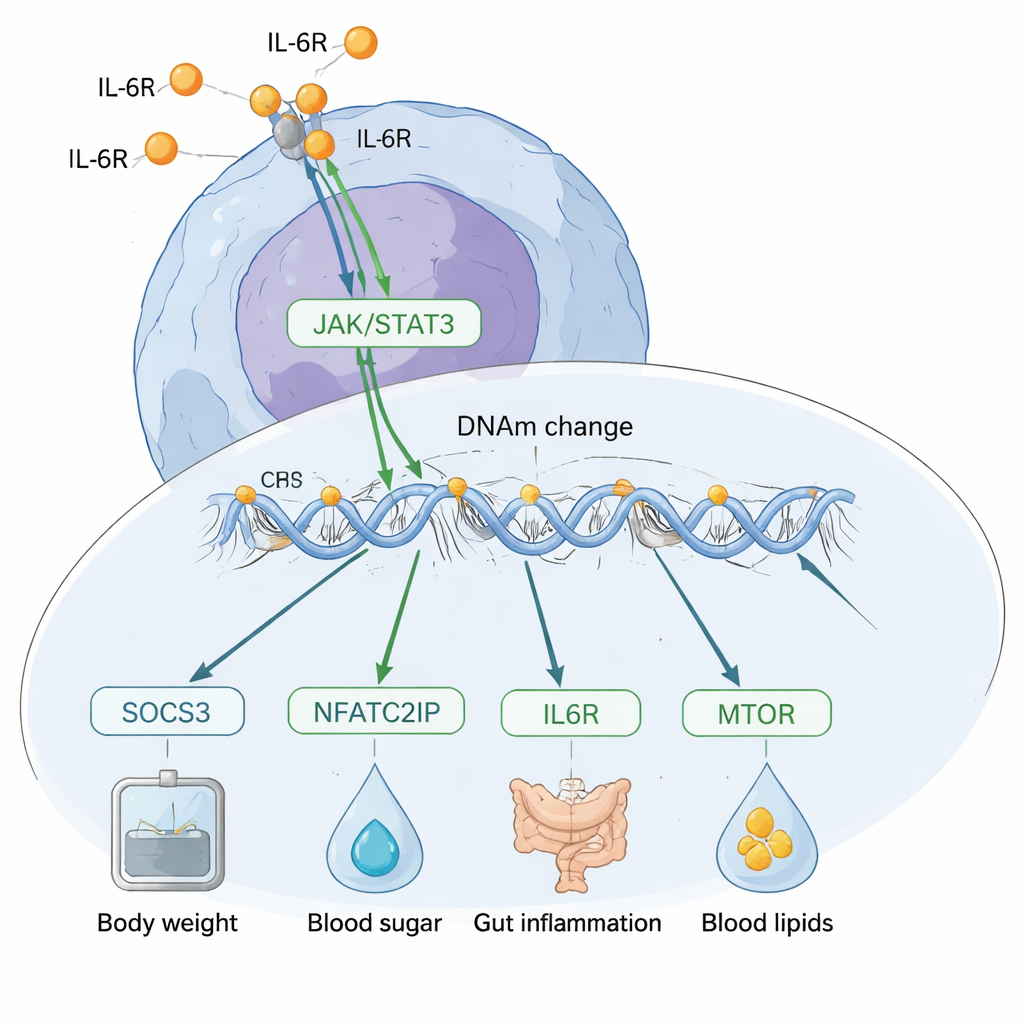
В каком направлении идёт причинно‑следственная связь?
Главная задача — выяснить, вызывает ли метилирование ДНК изменения в IL‑6 или же IL‑6 перестраивает метилирование. Команда использовала несколько генетических приёмов для проверки этого направления. По всему геному их «триангуляционные» анализы поддерживали модель, согласно которой IL‑6 в основном приводит к изменениям метилирования ДНК, а не наоборот. Затем они сосредоточились на отдельных сайтах и обнаружили, что изменения метилирования рядом с геном SOCS3, по‑видимому, опосредуют влияние IL‑6 на факторы риска, такие как масса тела, уровень холестерина, уровень CRP и воспалительные заболевания кишечника. Напротив, один заметный сайт рядом с регулятором гена NFATC2IP показал признаки влияния на продукцию самого IL‑6 и, по‑видимому, затрагивал сразу несколько состояний, включая индекс массы тела, диабет 2‑го типа и воспаления кишечника.
Что это значит для профилактики и лечения в будущем
Для неспециалиста ключевая мысль такова: IL‑6 и эпигенетические метки на ДНК тесно переплетены и влияют на множество распространённых заболеваний. Чаще всего IL‑6 оставляет химический «отпечаток» на геноме, особенно в иммунных клетках, отмечая и, возможно, стабилизируя провоспалительные состояния. Однако в нескольких ключевых точках метилирование может задавать уровень производства IL‑6 и силу иммунных ответов. Эти результаты указывают на паттерны метилирования ДНК как перспективные маркёры воспалительного и метаболического здоровья в крови и предполагают, что прицельное изменение эпигенетики — особенно вокруг генов, таких как SOCS3 и NFATC2IP — однажды может дополнить препараты, блокирующие IL‑6, в предотвращении или лечении хронических заболеваний.
Цитирование: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Ключевые слова: интерлейкин‑6, метилирование ДНК, воспаление, метаболические заболевания, эпигенетика