Clear Sky Science · ru
MAT2A усиливает транскрипцию PARN через SRF, ускоряя гликолиз и стимулируя злокачественное прогрессирование при остеосаркоме
Почему это исследование костного рака важно
Остеосаркома — наиболее распространённый рак кости у детей и подростков, а методы лечения за десятилетия изменились мало. Многие юные пациенты по-прежнему сталкиваются с неблагоприятным прогнозом, особенно при метастазировании или химиорезистентности. В этом исследовании обнаружен скрытый «главный переключатель» — белок MAT2A, который помогает клеткам остеосаркомы расти, перенастраивать энергетический обмен и формировать агрессивные опухоли. Также показано, что препарат, направленный против MAT2A, способен замедлять или уменьшать эти опухоли в лабораторных моделях.
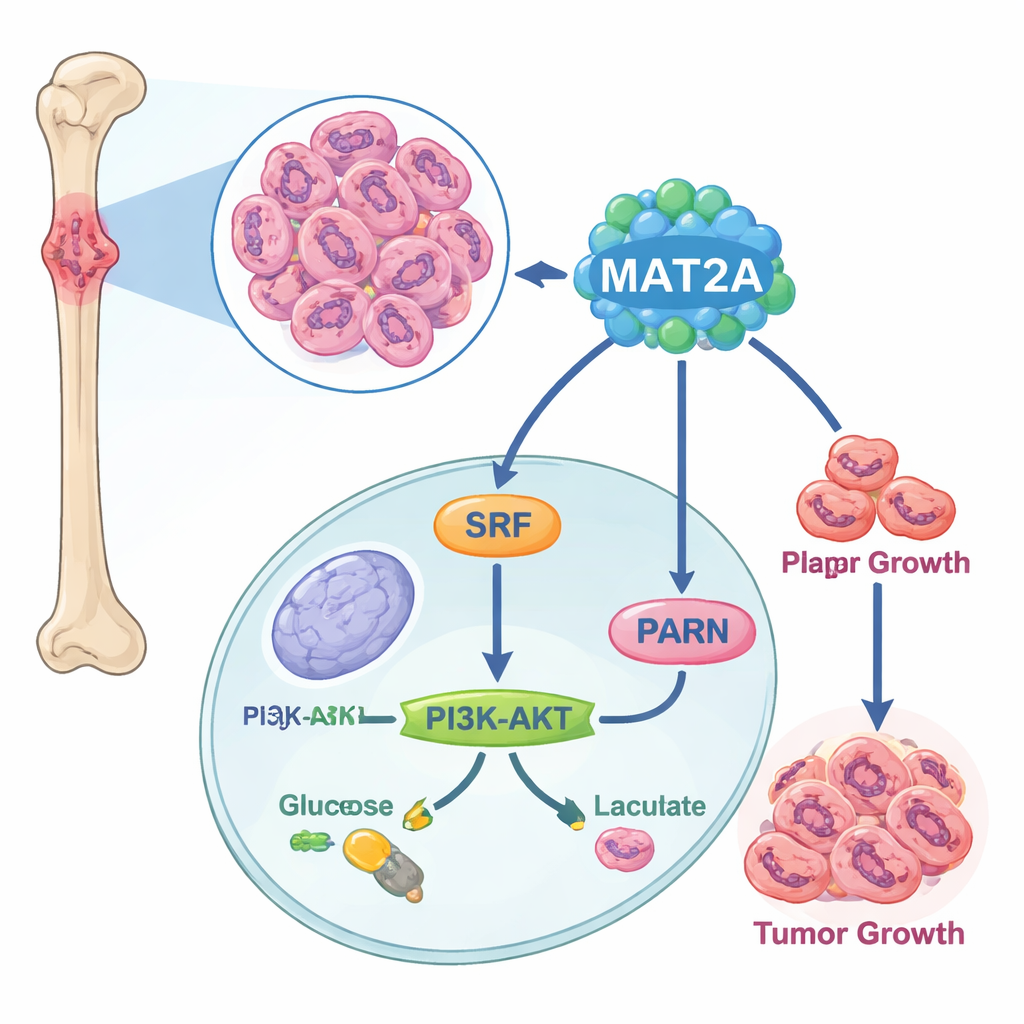
Скрытый двигатель внутри опухолевых клеток
Исследователи начали с сопоставления образцов костного рака и нормальной костной ткани на уровне отдельных клеток. Они обнаружили, что в тканях остеосаркомы больше клеток, строящих опухоль, и меньше иммунных клеток, а один ген — MAT2A — оказался необычно активным в раковых клетках. Анализ публичных онкологических баз данных и лабораторных линий клеток подтвердил, что уровень MAT2A значительно выше при остеосаркоме, чем в здоровых костных клетках, и что у пациентов с повышенным MAT2A чаще наблюдается более прогрессирующее заболевание и поражение лимфатических узлов. Это поставило MAT2A в центр внимания как потенциальный драйвер болезни, а не простого попутчика.
Подавление MAT2A замедляет рост опухоли
Чтобы проверить реальную значимость MAT2A для поведения опухоли, команда использовала генетические инструменты для снижения экспрессии MAT2A в клеточных линиях остеосаркомы. При заглушении MAT2A клетки делились медленнее и чаще подвергались запрограммированной гибели. У мышей, имплантированных этими модифицированными клетками, опухоли росли значительно медленнее и были заметно меньшими, тогда как масса тела животных оставалась стабильной. Эти эксперименты показали, что клетки остеосаркомы сильно зависят от MAT2A как для выживания, так и для способности формировать опухоли.
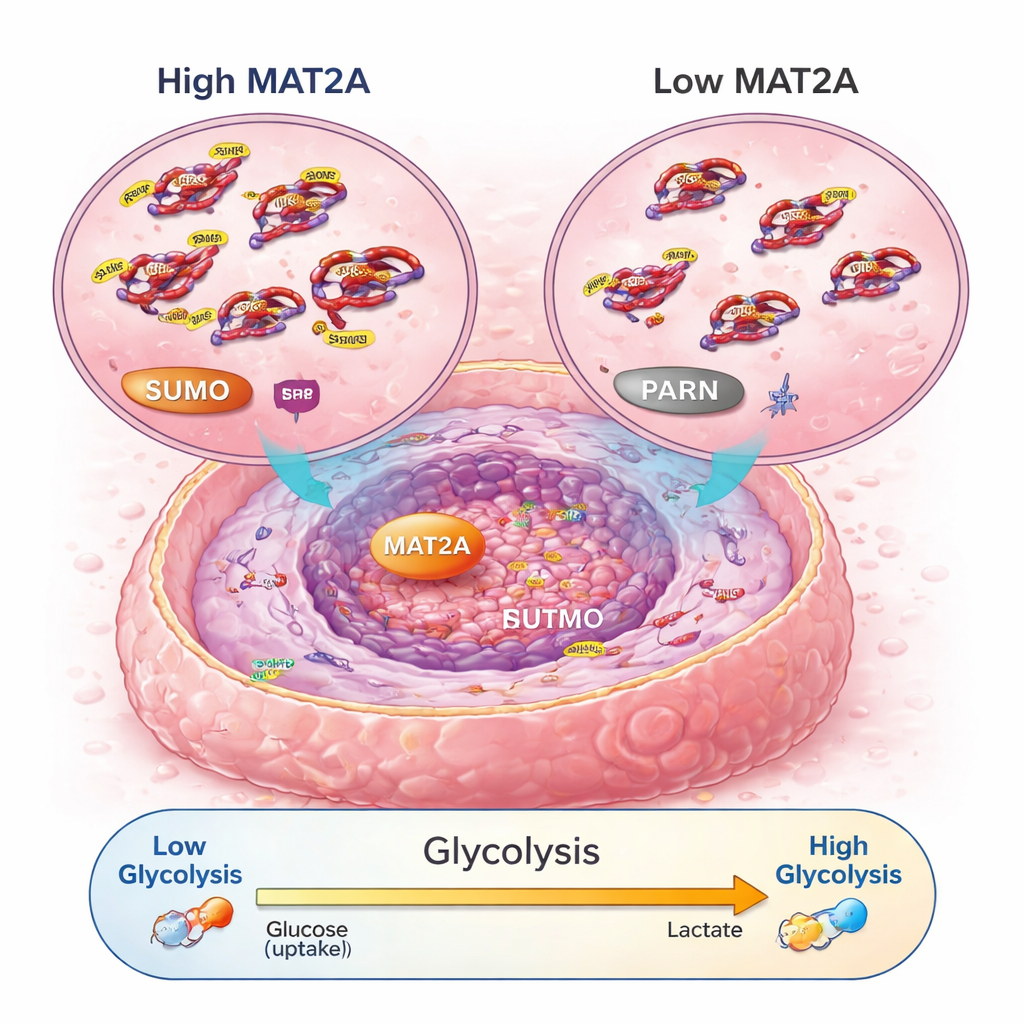
Сигнальная цепочка, усиливающая потребление топлива клеткой
Углублённый анализ показал, что MAT2A выполняет не только свою обычную метаболическую функцию. Внутри ядра он связывается с фактором транскрипции SRF, способствуя его стабилизации и активности за счёт продвижения пометки SUMO. В свою очередь SRF включает ген PARN, который активирует хорошо известный путь PI3K–AKT и усиливает механизмы аэробного гликолиза — быстрый, но неэффективный способ выработки энергии, который предпочитают раковые клетки. При снижении MAT2A клетки производили меньше АТФ (энергетической валюты), поглощали меньше глюкозы, вырабатывали меньше молочной кислоты и переключались в более спокойный режим аэробного дыхания. Нарушение PARN или AKT могло отменить про-пролиферативные и про-гликолитические эффекты MAT2A, подтверждая, что эта цепочка — MAT2A → SRF → PARN → PI3K–AKT — служит ключевым энерго- и ростовым контуром в остеосаркоме.
Нетрадиционная роль и доступная мишень для лекарств
Удивительно, но версия MAT2A, лишённая своей нормальной ферментативной активности, всё ещё поддерживала стабильность SRF и активацию PARN, что означает: эта роль в стимулировании рака не зависит от его обычной химической реакции. Вместо этого MAT2A действует скорее как каркас, организующий другие белки. Это имеет практическое значение: препараты не обязательно должны блокировать каталитический центр, чтобы ослабить опухоль. Исследователи протестировали маломолекулярный ингибитор FIDAS-5, нацеленный на MAT2A, в культурах клеток и моделях на мышах. Лечение снижало уровень ядерного SRF, уменьшало сигнальную активность PARN и PI3K–AKT, подавляло гликолиз, замедляло рост клеток и вызывало гибель раковых клеток. У мышей FIDAS-5 уменьшал или замедлял рост опухолей без заметной потери веса, что указывает на переносимые побочные эффекты в этих экспериментах.
Что это значит для пациентов и будущих терапий
Для неспециалистов ключевая мысль такова: клетки остеосаркомы зависят от MAT2A, чтобы поддерживать свои программы роста и «двигатели» сжигания сахара на полной мощности. Стабилизируя ключевые контрольные белки и усиливая цепочку сигналов, MAT2A помогает опухолям расти быстрее и становиться агрессивнее. Блокирование этого белка — генетическими методами или с помощью препарата вроде FIDAS-5 — отрезает эту поддержку, вынуждая раковые клетки замедлиться, менее активно использовать энергию и в конечном счёте погибать. Хотя до клинического применения ещё далеко, это исследование выделяет MAT2A как перспективную новую мишень в борьбе с раком кости и открывает путь к более точным и менее токсичным методам лечения молодых пациентов.
Цитирование: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Ключевые слова: остеосаркома, MAT2A, метаболизм рака, путь PI3K AKT, таргетная терапия