Clear Sky Science · ru
Анализ гетерогенности эпитопов методом вычислений в иммуномаркерах на сериях разведений антител
Почему качество окрашивания антителами важно
От отслеживания клеток рака до диагностики инфекций — современная биология в значительной степени опирается на антитела, которые «подсвечивают» конкретные молекулы внутри клеток. Тем не менее во многих лабораториях тихо существует назойливая проблема: окрашивание слишком слабое, слишком зашумлённое или просто вводящее в заблуждение. В этой статье предложен практический компьютерный способ извлечь больше информации из рутинной серии разведений антител, помогающий исследователям настраивать окрашивание для получения более чистых изображений, более надёжных измерений и даже новых способов маркировки нескольких целей в одном цветовом канале. 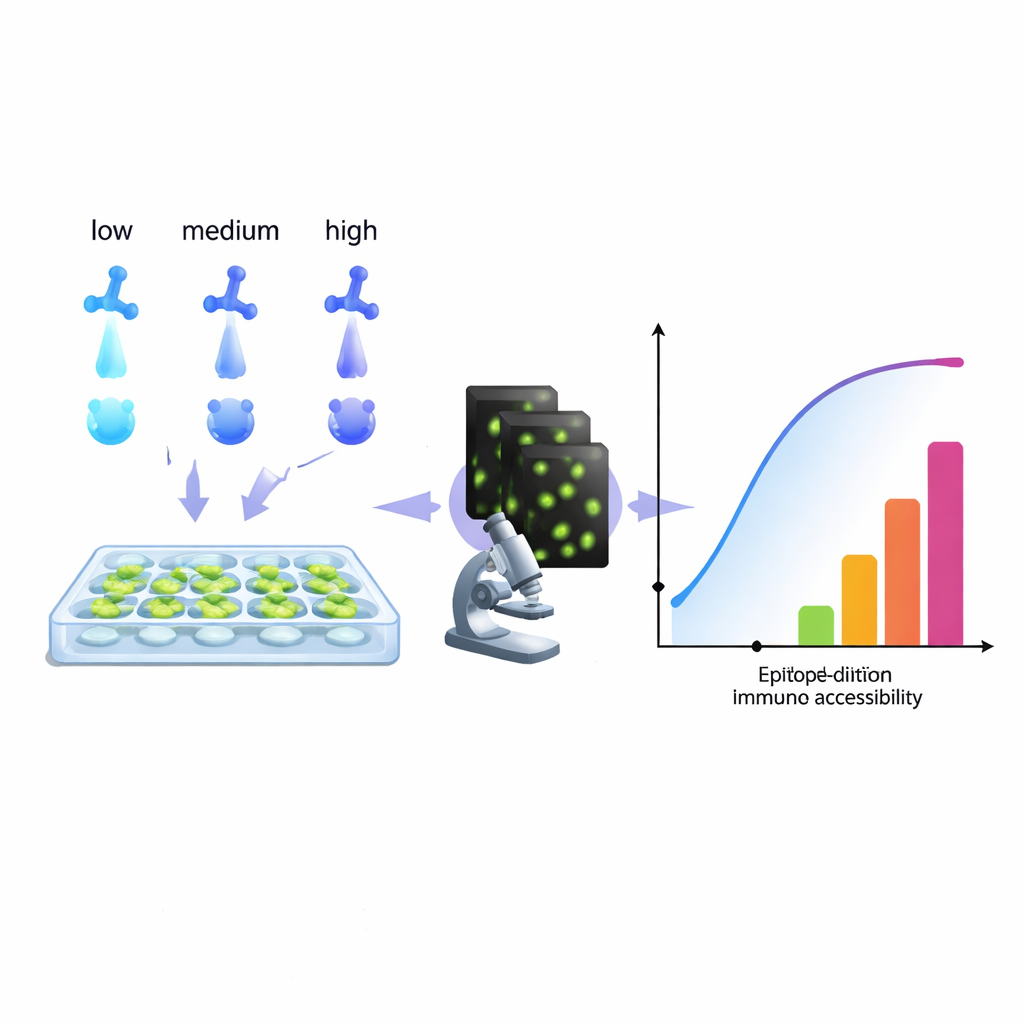
Как учёные обычно настраивают окрашивание антителами
Когда исследователи готовят эксперимент по иммуноокрашиванию, они обычно берут концентрацию антитела по справочнику, пробуют несколько разведений и выбирают то, которое «выглядит хорошо». За кулисами же бесчисленные мелкие факторы — форма белка, плотность внутри клеток, pH и то, насколько антитело может «протиснуться» к месту связывания — решают, прилипнет антитело или смоется. Традиционные методы измерения связывания антител, такие как поверхностно-плазмонный резонанс, лучше работают с очищенными белками на искусственных поверхностях, а не с плотно упакованными клетками или тканями. Это значит, что полученные числа могут не соответствовать реальной биологической среде, где антитело действительно используется. В результате лаборатории могут непреднамеренно выбирать концентрации, которые усиливают размытый фон или скрывают важные, но менее доступные мишени.
Преобразование простой серии разведений в «карты доступности»
Авторы предлагают иной подход: рассматривать стандартную серию разведений антител как богатый набор данных и подгонять её под модель, отражающую то, что действительно видит микроскоп — антитела, остающиеся связанными даже после многократного промывания. Анализируя, как сигнал растёт с увеличением концентрации, их алгоритм восстанавливает «гистограмму доступности». Вместо попыток выделить чистые химические константы связывания, эта гистограмма группирует участки мишени в технические «классы эпитопов» на основе того, насколько легко их окрасить в реальных условиях. Один биологический эпитоп может появляться в нескольких классах, если, например, он легко доступен в одной части клетки и более труднодоступен в плотной области. Существенно то, что метод работает непосредственно с данными микроскопа, без необходимости в очищенных белках или дополнительном оборудовании, поэтому любая лаборатория, способная провести серию разведений и количественно измерить флуоресценцию, теоретически может построить такие гистограммы. 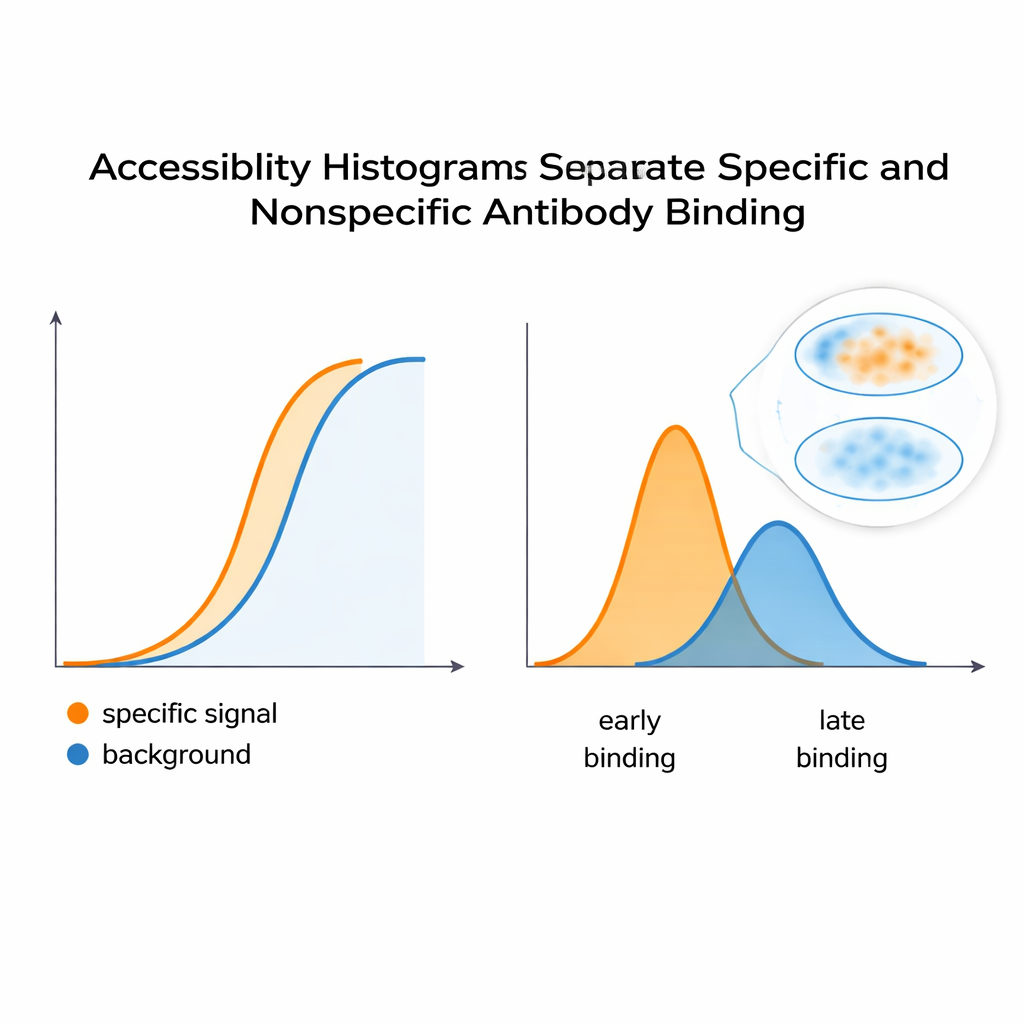
Отделение настоящего сигнала от фона
Чтобы проверить, действительно ли эти гистограммы отражают поведение окрашивания, команда создала контролируемую систему на базе клеток HeLa и двух моноклональных антител: одно имитировало желаемый специфический сигнал, другое действовало как нежелательный фон. При смешивании общая кривая флуоресценции выглядела как единый плавный отклик — ничего очевидного не указывало на двух отдельных вкладчиков. Но вычислительный анализ разделил эту кривую на отдельные пики в гистограмме доступности, выявив по меньшей мере два лежащих в основе класса эпитопов. Похожая стратегия, применённая к антителу, распознающему чувствительный к конформации участок регуляторной субъединицы PKA, показала, что изменения в конформации белка — вызванные молекулой cAMP — смещали распределение доступных эпитопов. Это указывает на то, что метод может сигнализировать о том, когда структуры белков открываются или закрываются, изменяя лёгкость связывания антител внутри клеток.
Выбор лучших разведений и окрашивание большего числа целей одним цветом
Поскольку каждый пик в гистограмме доступности вносит вклад преимущественно в определённом диапазоне концентраций, авторы используют эти пики как ориентир для выбора «оптимальных» разведений. Пики с низкой доступностью, появляющиеся только при очень высоких концентрациях антител, скорее всего отражают неспецифическое связывание, тогда как ранние пики обычно соответствуют предполагаемой мишени. Моделируя, как отдельные пики складываются в общую дозово-ответную кривую, команда может предлагать разведения, которые максимизируют специфический сигнал до того, как появятся проблемные пики — иногда значительно более разбавленные, чем рекомендации производителя. Они также развивают эту идею в хитрую форму «вычислительного мультиплексирования». Повторно окрашивая одно и то же фиксированное образец с тщательно подобранными концентрациями, делая снимки после каждого раунда и вычитая ранние изображения из поздних, можно выделять сигналы, связанные с разными классами доступности, фактически разделяя несколько мишеней в одном флуоресцентном канале.
Что это значит для повседневной работы в лаборатории
Проще говоря, эта работа превращает рутинный шаг по устранению неполадок — выполнение серии разведений антител — в количественный инструмент. Гистограммы доступности помогают учёным заметить скрытую сложность в их окрашиваниях, выбирать разведения, уменьшающие вводящий в заблуждение фон, и в некоторых случаях разделять перекрывающиеся сигналы без необходимости дополнительных флуоресцентных меток. Хотя базовая модель намеренно проста и не охватывает каждую молекулярную деталь, она разработана так, чтобы быть удобной в использовании и достаточно надёжной для реальных данных. При широком внедрении этот подход может сделать методы на основе антител — от базовой микроскопии до диагностических тестов — более надёжными, информативными и менее зависящими от метода проб и ошибок.
Цитирование: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Ключевые слова: окрашивание антителами, иммунофлуоресценция, доступность эпитопа, дозово-ответная зависимость, вычислительный мультиплекс