Clear Sky Science · ru
Стратегические шаги для крио-ЭМ исследований структуры малых (<100 кDa) GPCR
Почему маленькие клеточные выключатели важны для медицины
Большая часть современной медицины действует, осторожно воздействуя на крошечные выключатели в мембранах наших клеток — так называемые рецепторы, сопряжённые с G‑белком (GPCR). Эти выключатели распознают гормоны, запахи и лекарства; примерно треть всех одобренных препаратов нацелена на них. Чтобы проектировать более безопасные и эффективные препараты, учёным нужны детальные трёхмерные изображения этих рецепторов, особенно в «выключенном» или неактивном состоянии, на которые многие лекарства ориентированы. В этой статье объясняется, как исследователи учатся видеть некоторые из самых маленьких GPCR с помощью крио‑электронной микроскопии (крио‑ЭМ) — мощного метода визуализации молекул, замороженных в близком к естественному состоянии.
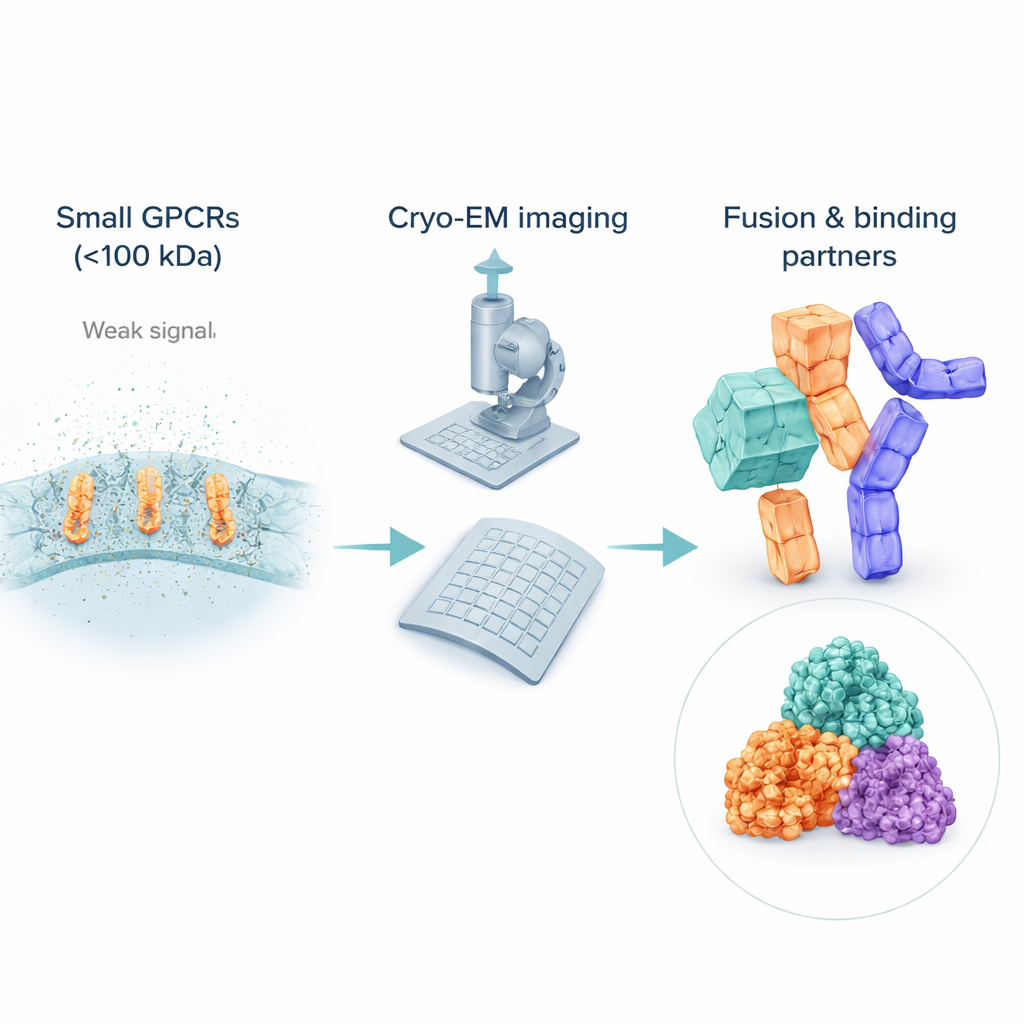
Проблема наблюдения очень маленьких рецепторов
Хотя крио‑ЭМ произвела революцию в структурной биологии, ей по‑прежнему сложно работать с малыми и гибкими молекулами. Многие неактивные GPCR весят значительно меньше 100 килода́льтон, что затрудняет их обнаружение и выравнивание на зашумлённых изображениях. Чтобы сохранить растворимость, учёные оборачивают эти рецепторы в детергентные мицеллы или липидные имитаторы, которые для электронного пучка могут выглядеть «больше», чем сам рецептор, заглушая сигнал белка. В отличие от активных рецепторов, связанных с громоздкими партнёрами, такими как G‑белки, неактивные GPCR часто лишены заметных внешних особенностей, поэтому компьютерам трудно усреднить множество изображений в чёткую трёхмерную картину. В результате большинство структур неактивных GPCR всё ещё получены более старыми методами рентгеноструктурного анализа, оставляя пробел в области крио‑ЭМ именно там, где действуют многие лекарства.
Увеличение массы рецепторов с помощью встроенных помощников
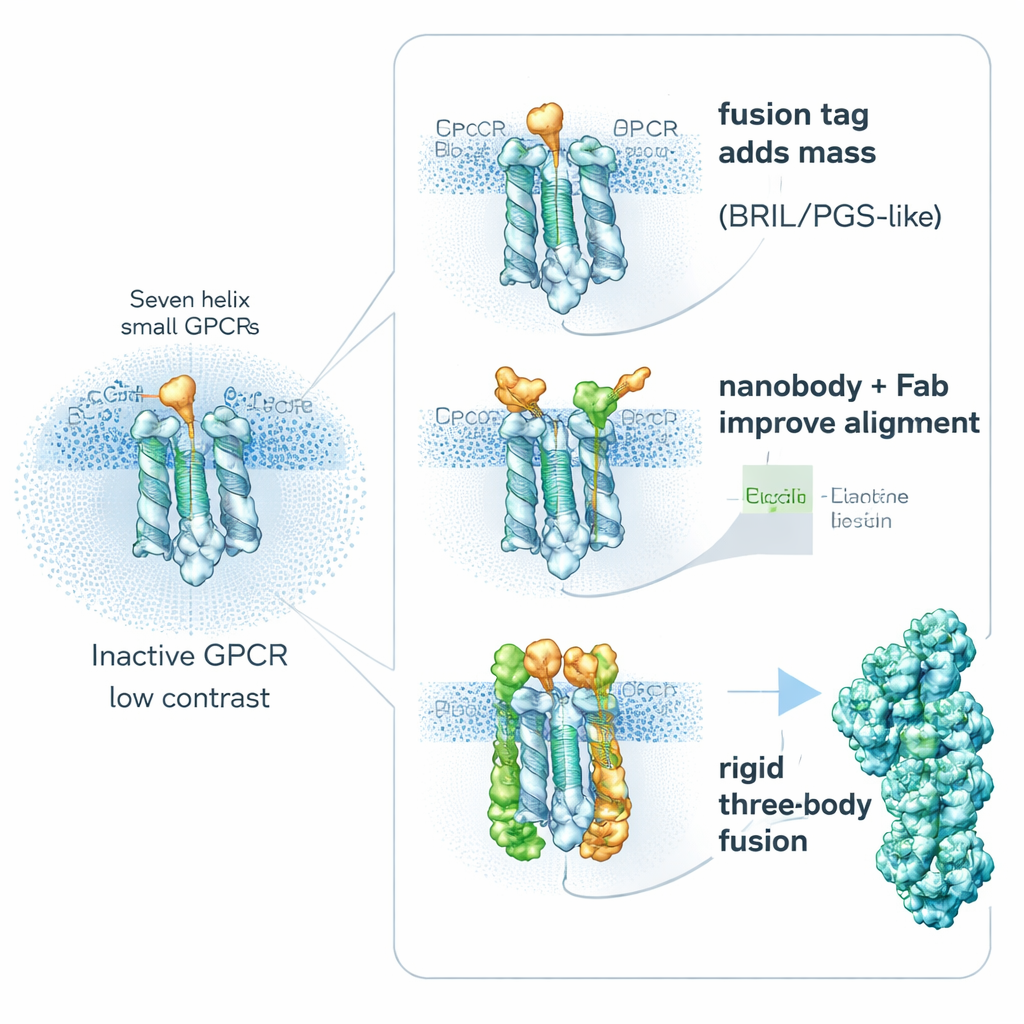
Одна ключевая стратегия удивительно проста: сознательно сделать рецептор «тяжелее». Исследователи генетически сшивают небольшие стабильные вспомогательные белки с гибкими участками GPCR, чтобы увеличить их размер и жёсткость, не закрывая важные области связывания лекарств. Популярные помощники включают BRIL (четырёхспиральный мот��в), PGS (термостабильный фрагмент фермента) и более крупный зажимоподобный белок, похожий на кальцинерин. Эти фьюжн‑партнёры часто вставляют в подвижную внутреннюю петлю, соединяющую две спирали. Упрочняя этот регион, они уменьшают размытие от молекулярного движения и дают распознаваемые формы, помогающие компьютерам выравнивать частицы. Исследования показывают, что точное положение и ориентация вставленного фрагмента могут решить успех проекта: в одном рецепторе по‑другому размещённый PGS‑тег улучшил разрешение с размытых 6 ангстрем до гораздо более чётких 3,7 ангстрема.
Заимствование антител и дизайнерских связывающих молекул в качестве ручек
Второй путь избегает встраивания крупных фьюжнов и вместо этого присоединяет снаружи высокоаффинные «ручки». Крошечные фрагменты антител, называемые нанотелами, и родственные связывающие молекулы можно получить против неактивных GPCR и заставить их захватывать гибкие внутренние петли. Выдающийся пример — Nanobody‑6, изначально созданный как сенсор для одного опиоидного рецептора, а затем повторно использованный с небольшими модификациями для стабилизации нескольких других GPCR в неактивном состоянии. Поскольку он связывается смещённо, он даёт каждой частице ясный ориентир, что делает усреднение изображений более надёжным. Исследователи часто развивают эту идею, добавляя второй слой — обычный фрагмент антитела, распознающий сам нанотело — создавая более громоздкий, жёсткий комплекс, который отчётливо виден в крио‑ЭМ. Другие конструированные связывающие молекулы, такие как DARPins, могут использоваться как модульные распорки или соединители с большими белковыми каркасами, дополнительно усиливая сигнал от очень маленьких целей.
Более умный дизайн образцов и обработка изображений с поддержкой ИИ
Встраивание помощников или добавление связывающих молекул — только часть решения. Обзор подчёркивает, что хорошие структуры начинаются с тщательно спроектированных конструкций рецепторов: отрезание болтающихся хвостов, введение стабилизирующих мутаций и использование современных инструментов предсказания структур для выявления участков, которые могут вызвать проблемы. На стороне визуализации старые приёмы, такие как фазовые пластинки, повышающие контраст слабых частиц, дополняются или даже заменяются инструментами искусственного интеллекта. Программы глубокого обучения могут выцеплять крошечные частицы, скрытые в зашумлённых микрографах, а новые алгоритмы сортируют изображения по разным конформациям, когда рецепторы перебирают множество форм. В сочетании с ориентирующими помощниками эти достижения двигают крио‑ЭМ к надёжному получению структур мембранных белков, которые раньше считали слишком маленькими или слишком динамичными для изучения.
Что это значит для будущих лекарств
Статья делает вывод, что не существует одного «волшебного» помощника, подходящего для всех рецепторов, но растущий набор фьюжн‑партнёров, антителоподобных связывающих молекул и методов на базе ИИ постепенно открывает для крио‑ЭМ неактивный ландшафт GPCR. Для неспециалистов главный вывод таков: делая маленькие рецепторы более крупными и упорядоченными для микроскопа, учёные наконец получают детальные снимки точных форм, к которым предпочитают привязываться многие лекарства. Эти структурные чертежи должны ускорить разработку препаратов, которые точнее выключают эти клеточные выключатели — или тонко настраивают их активность — с меньшим числом побочных эффектов.
Цитирование: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Ключевые слова: Рецепторы, сопряжённые с G‑белком, крио-электронная микроскопия, поиск лекарств, структурная биология, каркасы нанотел