Clear Sky Science · ru
Временная динамика побочного расщепления РНК LbuCas13a в клетках человека
Превращение бактериальной защиты в прецизионный уничтожитель клеток
Исследователи обнаружили способ превратить бактериальный иммунный белок в высокоизбирательный «автобусный» переключатель для человеческих клеток. Используя фермент CRISPR под названием LbuCas13a, они могут опознавать заданное РНК-сообщение внутри клетки и затем разрушать почти всю остальную РНК этой клетки. Для непрофессионалов это интересно тем, что РНК-сообщения контролируют, какие белки синтезирует клетка; умение стирать их по команде открывает пути к новым методам лечения рака, антивирусным стратегиям и мощным инструментам для исследований.
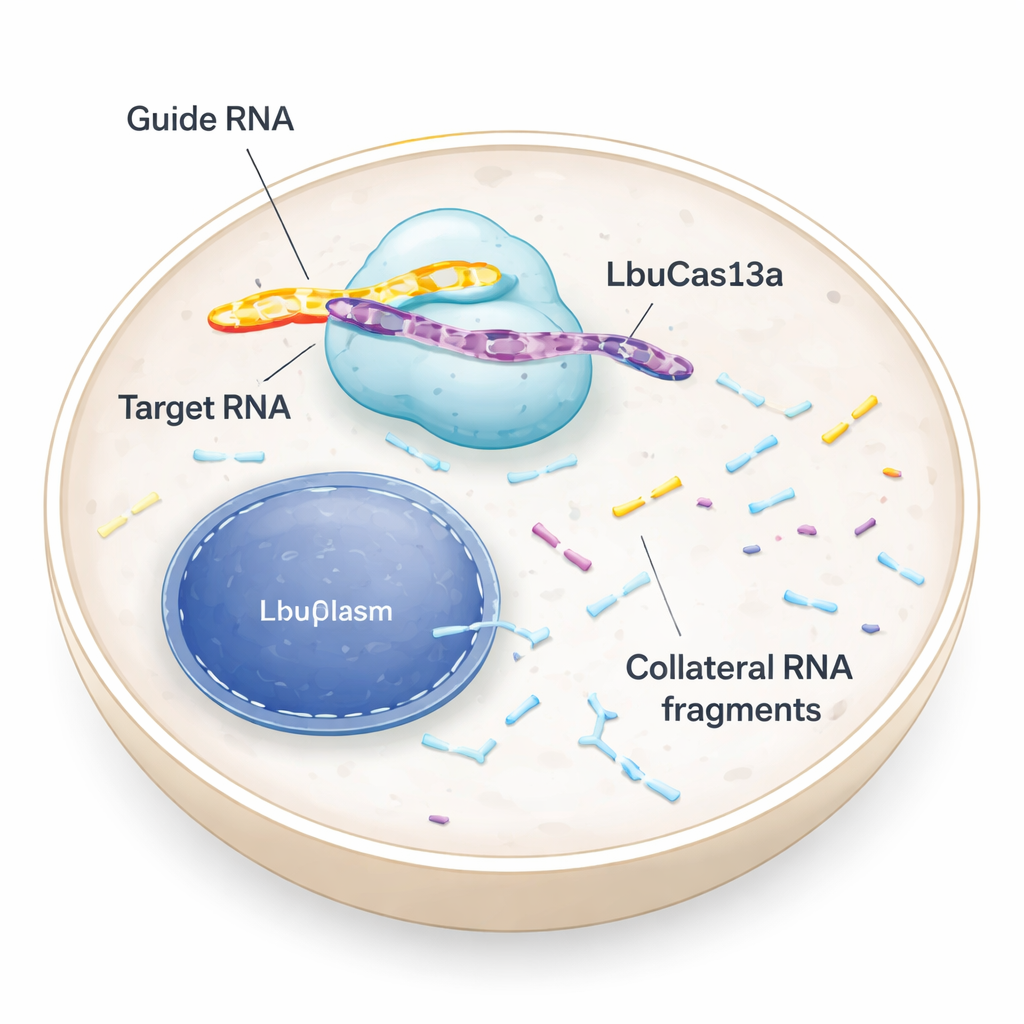
Молекулярные ножницы, нацеленные на РНК, а не на ДНК
Большинство людей слышали о CRISPR-инструментах, которые режут ДНК, переписывая генетический код. LbuCas13a отличается: он узнаёт и разрезает РНК, временные сообщения, несущие инструкции от ДНК к белковым фабрикам клетки. В бактериях ферменты Cas13 входят в антивирусную защиту. Как только они обнаруживают вирусную РНК, они не только разрезают эту цель, но и начинают рубить множество других РНК поблизости. Эта так называемая «коллатеральная» активность может загнать инфицированные клетки в состояние покоя или привести к их гибели, помогая защищать бактериальное сообщество. Ранние тесты на животных и в клетках человека предполагали, что коллатеральное расщепление у Cas13 слабое или отсутствует, поэтому фермент в основном использовали как точный «выключатель» РНК. Новое исследование пересматривает это предположение и показывает, что при правильных условиях коллатеральная активность в клетках человека может быть как сильной, так и полезной.
Развязывание коллатерального расщепления в клетках человека
Команда сравнила несколько вариантов Cas13 и обнаружила, что LbuCas13a особенно мощен. Они доставляли очищенный белок LbuCas13a, предзаряженный короткой направляющей РНК, непосредственно в клетки человека — форму молекулярной «инъекции белка», называемую доставкой рибонуклеопротеинов (RNP). Когда направляющая совпадала с целевой РНК — например, геном флуоресцентного маркера или обильными естественными сообщениями, такими как GAPDH и 18S рибосомальная РНК — фермент сначала разрезал эту цель, а затем начинал пожирать многие другие РНК. Примерно за 50 минут общий профиль РНК в клетке резко изменялся, появлялись характерные фрагменты расщепления. Этот коллатеральный эффект наблюдали при разных методах доставки и в ряде типов клеток, что показывает: это не случайность одной клеточной линии или одного искусственного таргета.
От раздробления РНК к гибели клетки и селекции
Что происходит с клеткой, чьи РНК-сообщения внезапно исчезают? С помощью микроскопии живых клеток исследователи наблюдали, что клетки, экспрессирующие целевую РНК, постепенно вступали в апоптоз — аккуратную форму запрограммированной клеточной смерти, отмеченную характерными «предупредительными» сигналами перед разрушением клетки. Важно, что соседние клетки, не экспрессировавшие целевую РНК, оставались в основном не затронутыми, что демонстрирует специфичность самоуничтжения. Группа затем использовала это свойство как инструмент селекции. Когда они смешивали клетки с целью и нормальные клетки и активировали LbuCas13a, клетки с целью выборочно истощались в течение нескольких дней. Повторные обработки ещё сильнее снижали их долю. Они показали, что это может обогащать успешно отредактированные клетки и также настраиваться на атаку раковых клеток, перепроизводящих онкоген (здесь CDK4), при этом щадя близкие клетки с гораздо меньшим уровнем этой РНК.
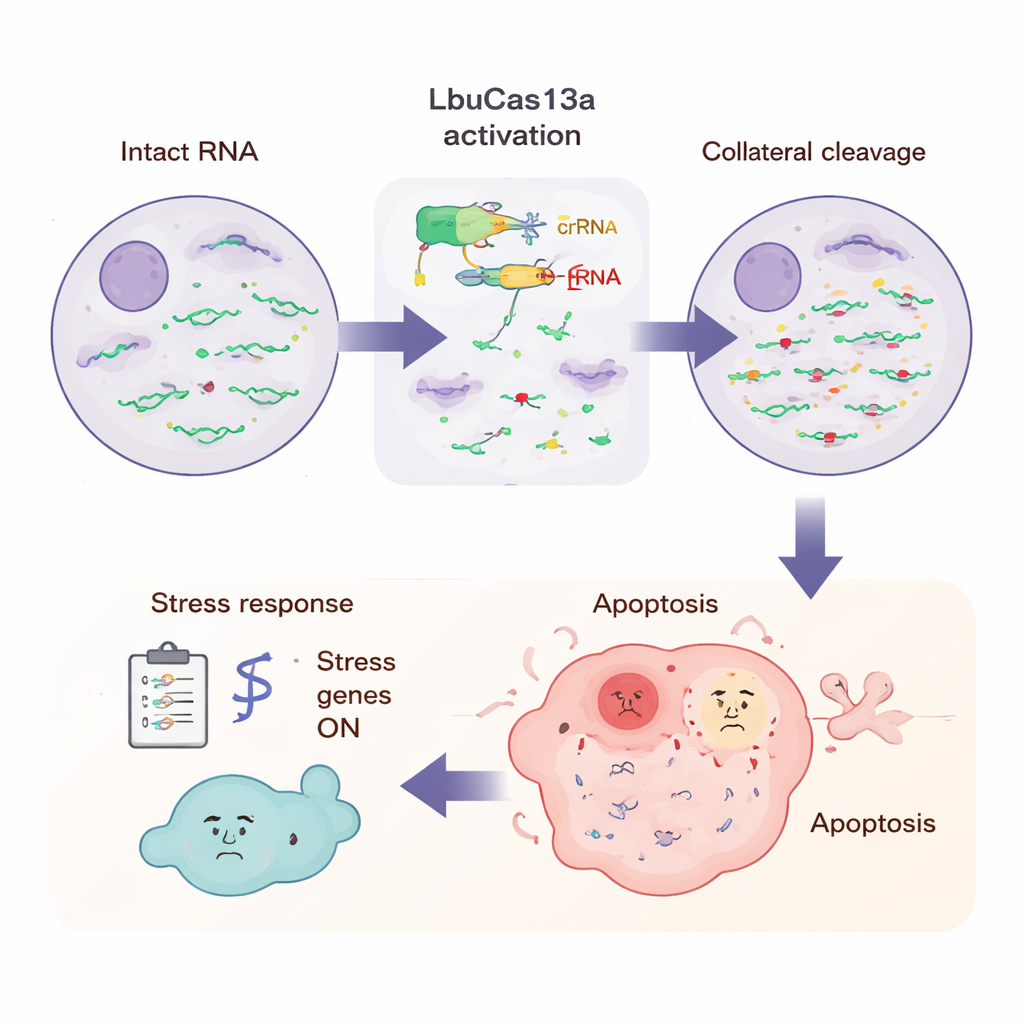
Что переживает клетка во время атаки
Чтобы увидеть общую картину, учёные измеряли все РНК в клетке в несколько временных точек после активации LbuCas13a. Вводя известные стандарты РНК, они смогли показать, что большинство белок-кодирующих РНК в цитоплазме уменьшилось более чем вдвое в течение нескольких часов, тогда как некоторые РНК — например, митохондриальные сообщения и некоторые ядерные некодирующие РНК — в основном сохранялись. Длинночтениевая секвенировка выявила, что разрезание происходило в повторяющихся, специфичных нуклеотидных позициях, часто в гибких петлевых регионах РНК, богатых урацилом, что соответствует паттернам, наблюдаемым в тестовых экспериментах. На более поздних временных точках активировались многие гены стресса и врождённого иммунитета, включая связанные с воспалительными сигналами и антивирусной защитой. Этот паттерн указывает на то, что клетка ощущает внезапный поток сломанных концов РНК подобно распознаванию вирусной инфекции, что запускает сигнальную программу, завершающуюся апоптозом.
Почему это важно и к чему может привести
Говоря проще, исследование показывает, что LbuCas13a можно превратить в направляемый РНК «выключатель смерти» для клеток: если клетка синтетически или патологически производит слишком много определённой РНК, активация LbuCas13a против этой РНК вызывает почти глобальную потерю РНК, иммуноподобный сигнал тревоги и затем контролируемую клеточную гибель. Поскольку эффект сильно зависит от уровня экспрессии целевой РНК, это может быть использовано для устранения клеток, гиперэкспрессирующих вредоносные гены — например, некоторых раковых клеток — или для очистки нежелательных клеток в смешанных культурах при исследованиях или производстве клеточных терапий. В то же время работа служит предостережением: направленные на РНК CRISPR-инструменты могут иметь мощные побочные эффекты, которые необходимо тщательно контролировать. Понимание того, когда и как возникает коллатеральное расщепление РНК, важно для безопасного применения технологий Cas13 в медицине и биотехнологии.
Цитирование: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Ключевые слова: CRISPR-Cas13, расщепление РНК, клеточная гибель, нацеленность на рак, инструменты редактирования генов