Clear Sky Science · ru
Модуляция человеческих B1 GPCR липидами плазматической мембраны
Жиры, тонко подстраивающие приёмники сообщений наших клеток
Наши клетки полагаются на крошечные белковые антенны, называемые рецепторами, чтобы чувствовать гормоны и нейромедиаторы. Многие препараты с крупным клиническим эффектом действуют, направляясь на эти рецепторы. В этом исследовании показано, что обычные жиры во внешнем слое клетки выполняют гораздо большую роль, чем просто пассивный фон: они напрямую хватают и формируют целое семейство ключевых рецепторов, тонко направляя, как сигналы включаются или выключаются. Понимание этого скрытого уровня контроля может помочь в создании более умных лекарств с меньшими побочными эффектами.
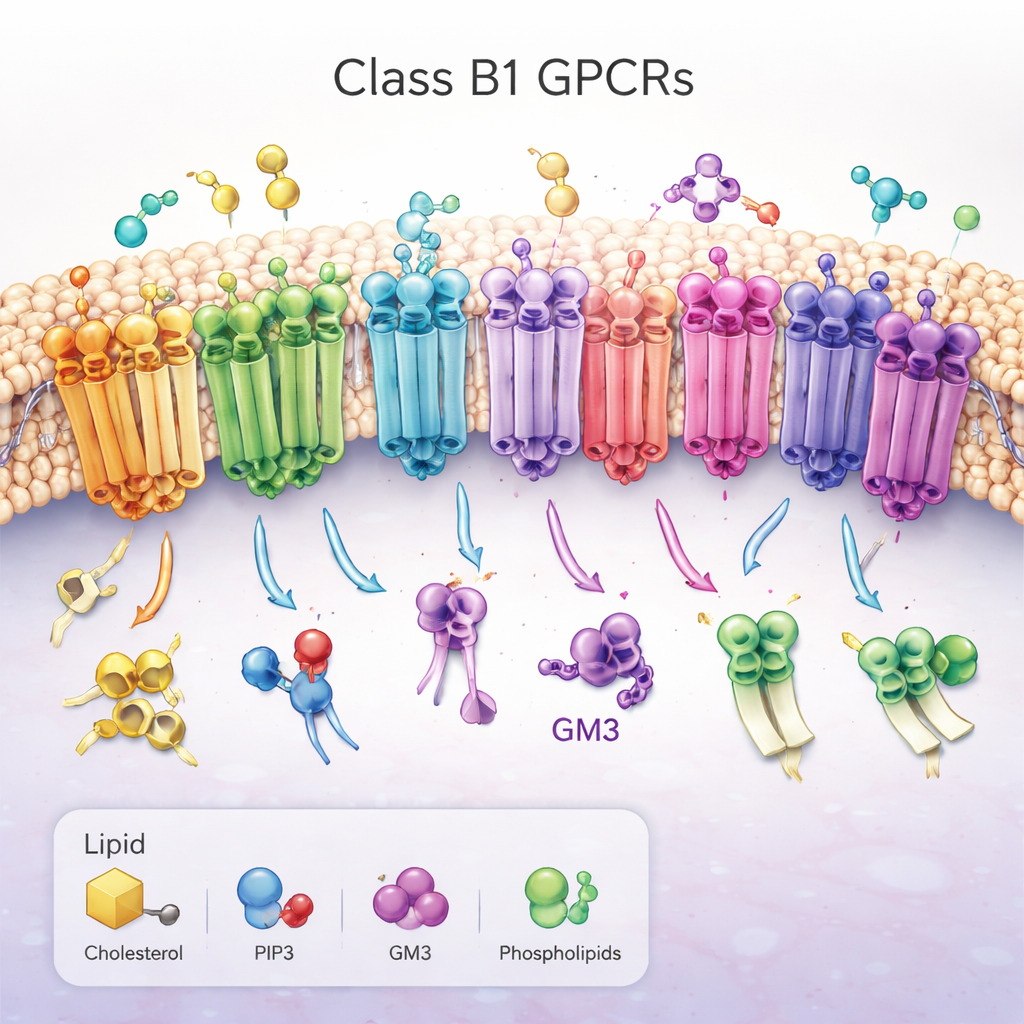
Семейство важных молекулярных антенн
Работа сосредоточена на рецепторах класса B1, сопряжённых с G‑белком (GPCR), наборе из 15 близкородственных рецепторов, которые помогают контролировать уровень сахара в крови, метаболизм, рост и реакции на стресс. Они проходят через внешнюю мембрану клетки, имея большую «головку» снаружи клетки, которая захватывает молекулы, подобные гормонам, и пучок из семи спиралей, проходящих сквозь липидный слой. При активации эти рецепторы изменяют форму на внутренней стороне клетки, открывая желоб, который привлекает партнёрские белки и запускает сигнальные каскады. Из‑за их центральной роли в заболеваниях, таких как диабет и ожирение, рецепторы класса B1 являются важными мишенями для лекарств, однако то, как окружающие мембранные липиды их регулируют, оставалось во многом неизвестным.
Моделирование рецепторов в их естественном окружении
Вместо изучения рецепторов в искусственных детергентных пузырьках исследователи поместили все 15 человеческих рецепторов класса B1 в компьютерно созданные мембраны, имитирующие сложную смесь липидов настоящих клеток. С помощью метода грубозернистой молекулярной динамики они провели несколько длинных симуляций каждого рецептора в активном и неактивном состоянии, суммарно порядка миллисекунды вычисленного времени. Они отслеживали, как три «регуляторных» липида — холестерин, сигнальный липид PIP2 и сахаросодержащий липид GM3 — приближаются, связываются и отсоединяются от разных участков каждого рецептора. Чтобы другие могли воспроизвести и развивать этот огромный набор данных, они зафиксировали каждый шаг настройки и анализа с помощью открытого инструмента рабочего процесса aiida‑gromacs и сравнили свои физически обоснованные результаты с предсказаниями новой ИИ‑модели (Chai‑1), которая предполагает, как белки связывают малые молекулы.
Скрытые карманы и консервативный липидный захват
Симуляции выявили повторяющиеся схемы связывания по всему семейству рецепторов. Холестерин, известный из обсуждений диеты, оказался западающим не только в ранее известном участке на одной из спиралей, но и в «глубинных мембранных» карманах между спиралями, с его полярной головой, погружённой необычно глубоко в мембрану. Один рецептор, рецептор секретина, показал особенно длительное связывание холестерина в отдельных карманах в активной и неактивной формах, что намекает на то, что холестерин может сильно смещать баланс сигнальной активности. PIP2 проявил заметно консервативное поведение: он концентрировался у внутренней стороны рецепторов на стыке двух спиралей и короткого хвостового сегмента (TM6, TM7 и H8), особенно когда рецепторы были в активном состоянии. В этом участке сети положительно заряженных аминокислот захватывали отрицательно заряженную головку PIP2, что предполагает механизм, с помощью которого этот липид может стабилизировать активную форму или помогать в привлечении сигнальных партнёров на внутренней стороне клетки.
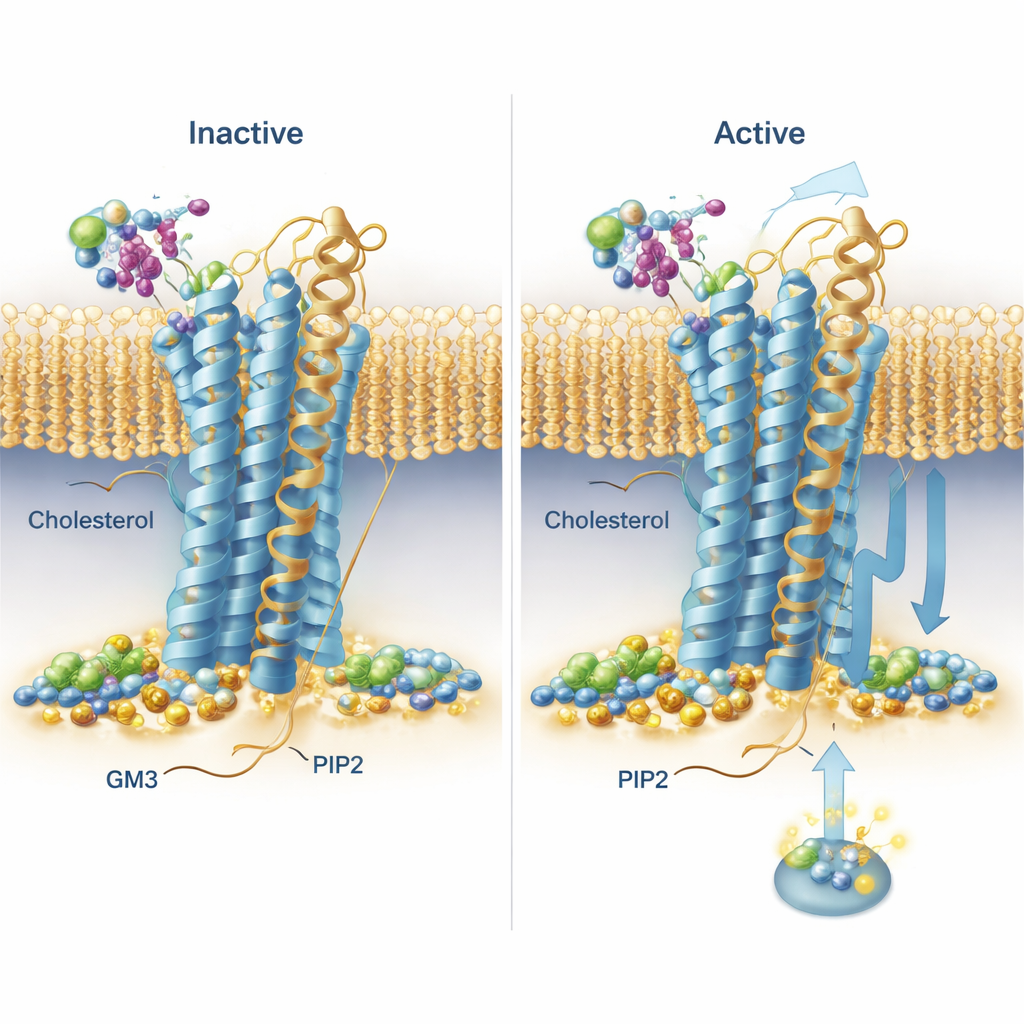
Сахаросодержащий липид, который подталкивает движение рецептора
GM3, сложный липид с сахарной головой, в основном взаимодействовал с большими внешними головами рецепторов. Команда отметила, что внешние домены некоторых рецепторов сильно раскачивались и изгибались относительно мембраны, тогда как у других они были более сдержанными. Для двух рецепторов, важных с фармакологической точки зрения — GLP‑1R и GIPR — они подробно изучили роль GM3. В симуляциях с присутствием GM3 этот липид либо прилегал к основанию внешнего домена и карману для связывания лигандов (GLP‑1R), либо цеплялся за дальнюю вершину внешнего домена (GIPR), в обоих случаях влияя на свободу движений этих доменов. Чтобы проверить эти предсказания в живых клетках, исследователи использовали светочувствительную методику (TR‑FRET), которая показывает, насколько близко помеченная «голова» рецептора находится к мембране. При снижении уровня GM3 с помощью ингибитора малой молекулы они наблюдали измеримые изменения в том, как голова рецептора смещается при стимуляции, в целом согласующиеся с идеей, что GM3 настраивает гибкость рецепторов в зависимости от рецептора и состояния.
Почему важны эти партнёрства липид–рецептор
В совокупности исследование рисует образ рецепторов класса B1 не просто как переключателей гормональных сигналов, а как элементов тщательно скоординированного танца с окружающими липидами. Холестерин может занимать скрытые карманы и склонять баланс в пользу определённых исходов сигнализации, PIP2 формирует консервативную внутреннюю «ручку», которая может фиксировать рецепторы в активной форме и направлять партнёрские белки, а GM3 регулирует, как внешние области рецепторов двигаются и встречают свои лиганды. Для неспециалистов ключевой вывод в том, что мембрана — это активный регуляторный слой: небольшие различия в составе липидов могут изменить поведение одного и того же рецептора в разных тканях или при разных заболеваниях. Картирование этих взаимодействий в деталях и открытие исходных данных симуляций закладывает основу для разработки будущих лекарств, которые могли бы использовать или избегать конкретных липидных контактов, потенциально делая терапии более селективными и эффективными.
Цитирование: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Ключевые слова: Рецепторы, сопряжённые с G‑белком, мембранные липиды, холестерин, PIP2, GM3