Clear Sky Science · ru
Структурные сведения о перемещении металлокластеров в каркасе сборки нитрогеназы NifEN
Как природа создает мощный химический инструмент
Азот вокруг нас в воздухе, но в этой форме его не могут использовать большинство живых организмов. Специальный фермент, называемый нитрогеназой, решает эту задачу, превращая атмосферный азот в аммиак — ключевой компонент для жизни и удобрений. В центре нитрогеназы находится плотный металлический «кластер», выполняющий основную химическую работу, но процесс сборки этой сложной структуры долгое время оставался неясным. В этой статье заглядывают внутрь процесса строительства, показывая, как белковый каркас NifEN действует как гибкая разгрузочная станция и конвейер для металлического груза кластера.
Молекулярная фабрика, стоящая за удобрениями и топливом
Нитрогеназа — природный аналог промышленных процессов по производству аммиака и жидких топлив. Вместо громоздких реакторов микроорганизмы используют компактный белковый аппарат, работающий за счёт клеточной энергии. Его эффективность зависит от уникально сложного металлического центра, собранного из железа, серы, молибдена, углерода и органической боковой группы. Сборка этого ядра слишком деликатна, чтобы оставлять её на волю случая, поэтому клетки задействуют эстафету вспомогательных белков. Один из ключевых участников — NifEN, который принимает почти готовый полностью железный прекурсор (L‑кластер), помогает превратить его в зрелую форму (M‑кластер) и затем передаёт рабочей нитрогеназе. Понимание того, как NifEN управляет этим трафиком, может помочь в попытках инженерно переработать микроорганизмы для более чистого производства удобрений или новых углеродных видов топлива.
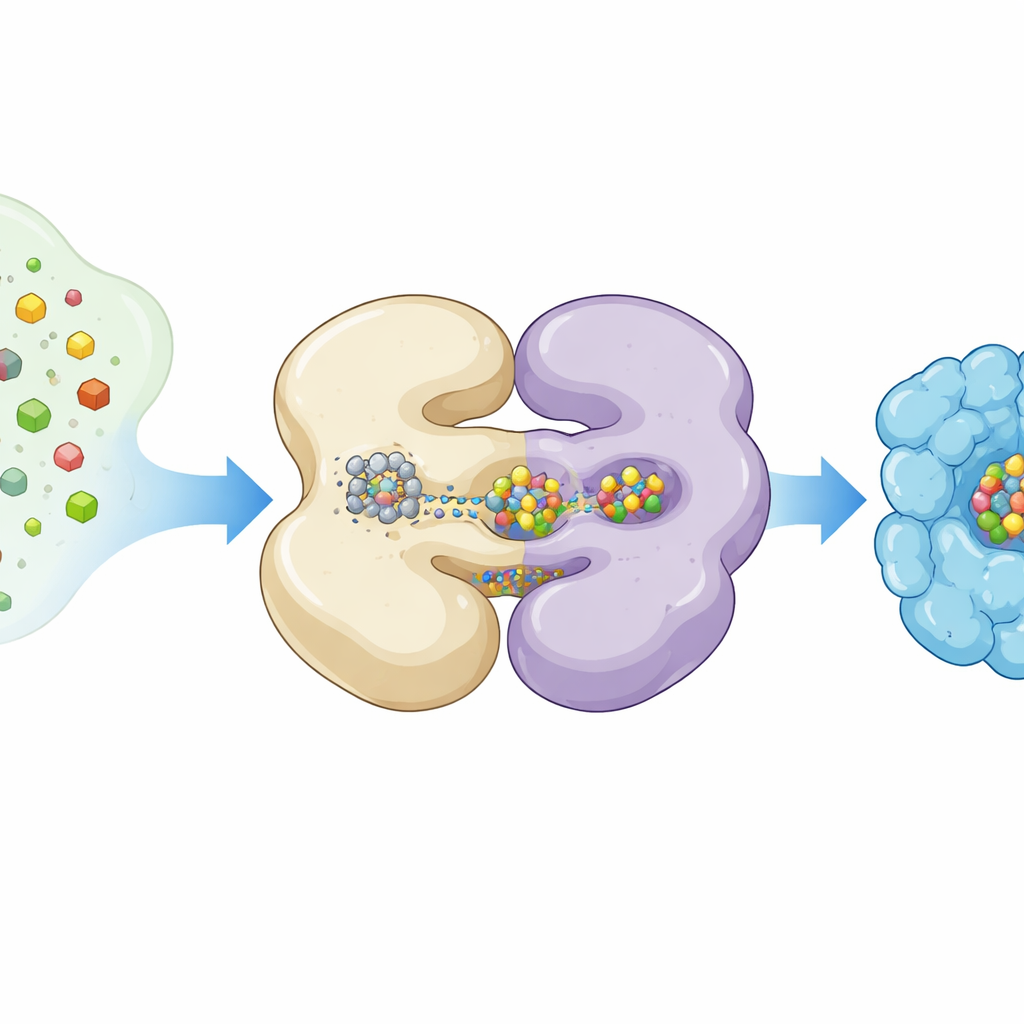
Видеть движущийся механизм в застывших кадрах
Авторы использовали криогенную электронную микроскопию — метод, который изображает белки при чрезвычайно низких температурах, чтобы зафиксировать NifEN в разных рабочих позах. Они экспрессировали NifEN в лабораторных бактериях таким образом, что некоторые копии белка несли L‑кластер, а другие были пустыми. Сортируя миллионы одиночных частиц, они восстановили две основные формы: «апо» форму без подвижного кластера и «холо» форму с кластером, связанным в внутреннем участке. Обе формы имеют аналогичное ядро, состоящее из четырёх субъединиц, собранных в две пары, но при наличии L‑кластера одна половина NifEN становится заметно более упорядоченной, а несколько спиралей поворачиваются внутрь, плотнее обхватывая металлический груз.
Скрытый туннель для металлического груза
Сравнение пустой и загруженной структур выявило поразительную особенность: длинный туннель, проходящий через димер NifEN. В пустом состоянии этот проход широк и открыт; после связывания кластера он сужается, поскольку белок сжимает пассажира. Ранние рентгеноструктурные исследования показали альтернативную «внешнюю» позицию L‑кластера у поверхности белка. Сопоставив все представления, исследователи сделали вывод, что кластер может занимать по крайней мере две станции на NifEN — одну внутреннюю и одну экспонированную — и перемещаться между ними по изогнутому пути, запираемому сдвигами гибкого домена. Это движение кажется более расслабленным, чем в окончательной нитрогеназе, где активный кластер удерживается жёстко, что предполагает, что NifEN создан для передачи, а не для долгосрочного катализирования.
Стыковка партнёров и непрерывный маршрут
Чтобы понять, как NifEN соединяется со своими предшествующими и последующими партнёрами, команда сочетала свои экспериментальные структуры с компьютерными моделями AlphaFold 3 и электронными микроскопическими данными более низкого разрешения о белковых комплексах. Модели указывают, что фермент NifB, который собирает L‑кластер из меньших железо‑серных фрагментов, стыкуется в «долине» на одной поверхности NifEN. Там можно проследить непрерывный туннель от собственных металлических центров NifB прямо в туннель NifEN и далее к внутренней станции L‑кластера. На противоположной поверхности NifEN другое место для стыковки принимает NifH — белок, вводящий молибден и органическую боковую группу для завершения кофактора. В такой конфигурации L‑кластер располагается на поверхностной позиции, идеально подготовленной для доработки. Мутации ключевых аминокислот, выстилающих предлагаемый маршрут, нарушают загрузку кластера, его перемещение или созревание, что даёт экспериментальную поддержку этой модели конвейера.
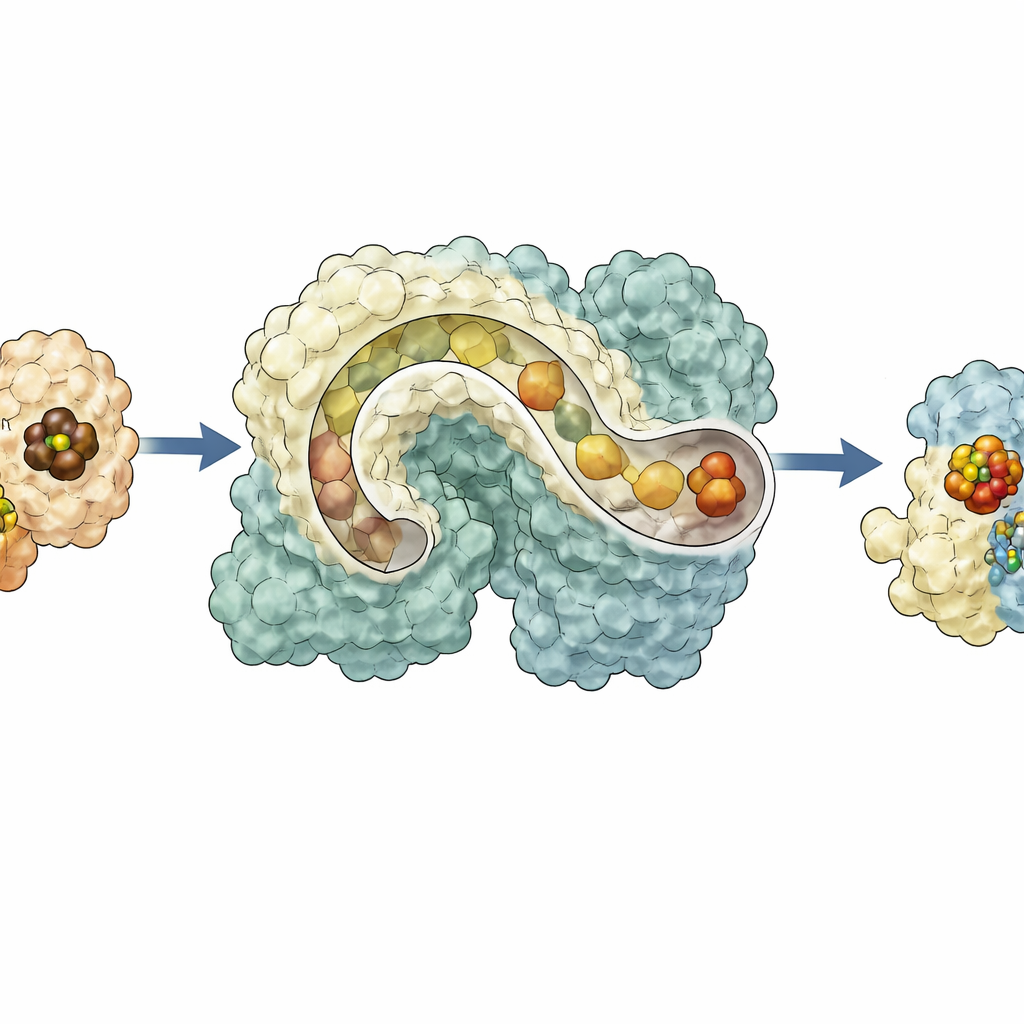
Почему важен гибкий каркас
В совокупности результаты рисуют NifEN как динамичный узел, который принимает металлическое ядро от NifB с одной стороны, перемещает его во внутреннюю приёмную камеру, затем выставляет на противоположной поверхности для доработки NifH, прежде чем вернуть зрелый кластер внутрь для передачи нитрогеназе. Эта схема транспорта, управляемая конформационными изменениями, объясняет, как несколько деликатных шагов могут координироваться внутри единой белковой рамки и даёт представление о том, как древние ферменты могли эволюционировать от более гибких каркасов к сегодняшним высокоспециализированным катализаторам. Для неспециалистов работа показывает, что даже на наноуровне природа использует конвейеры, туннели и движущиеся части, чтобы собирать молекулярные инструменты, лежащие в основе глобальных циклов азота, производства пищи и, возможно, будущих зелёных технологий.
Цитирование: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Ключевые слова: нитрогеназа, сборка металлокластеров, каркас NifEN, криоэлектронная микроскопия, биологическая фиксация азота