Clear Sky Science · ru
Графовая нейронная сеть с физическими ограничениями для прогнозирования гемодинамики внутричерепной аневризмы в реальном времени
Почему это важно для здоровья мозга
Вздутые ослабленные участки артерий мозга, называемые внутричерепными аневризмами, могут разорваться без предупреждения и вызвать угрожающее жизни кровоизлияние. Врачи знают, что то, как кровь течет по этим хрупким стенкам, влияет на то, останутся ли они стабильными или разрушатся, но современные инструменты для моделирования этого потока настолько медленны и специализированы, что редко применяются в повседневной практике. В этом исследовании представлен быстрый метод на основе искусственного интеллекта, который может имитировать детальные численные моделирования кровотока за секунды вместо часов, что открывает путь к более быстрым и персонализированным решениям о том, кому нужна терапия и как её проводить.
От статичных снимков к движущейся крови
Сегодня большинство решений по аневризмам принимают на основе того, что видно на снимках: размер, форма и расположение выпячивания, а также базовые факторы риска — возраст и повышенное давление. Эти статические изображения упускают невидимые силы текучей крови, например, насколько сильно она трёт стенку сосуда или как эта сила меняется в течение сердечного цикла. Традиционная вычислительная гидродинамика может точно вычислять эти величины, но требует экспертной подготовки и долгих расчетов на мощных компьютерах. В результате во многих больницах их нереалистично применять, когда врачу нужен ответ в рамках клинического визита или при экстренной процедуре.
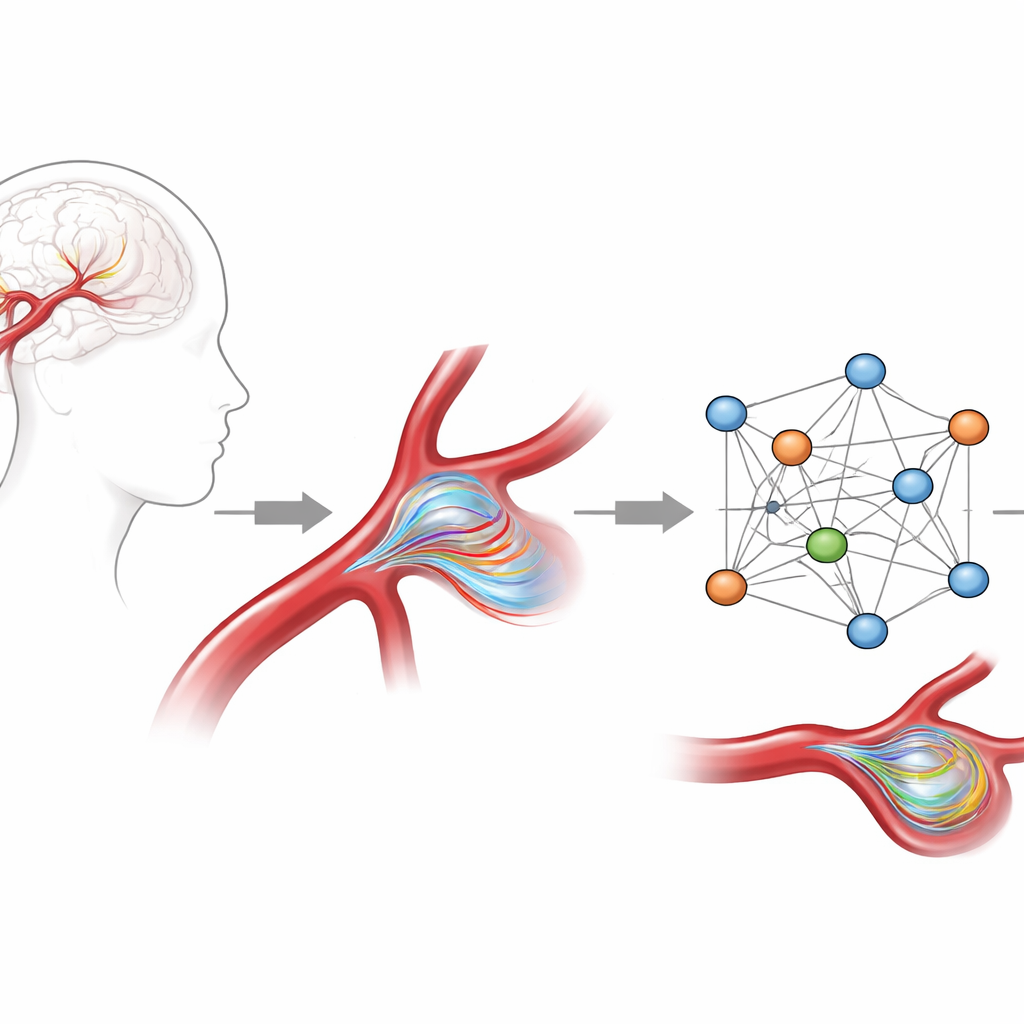
Обучение ИИ уважать законы физики
Исследователи создали модель ИИ на основе графовых нейронных сетей — типа алгоритма, который естественно работает с ветвящимися структурами, такими как сети сосудов, а не с квадратными сетками изображений. Они обучали её на высококачественных численных моделированиях кровотока в 105 формах аневризм, полученных из реальных клинических данных, сосредоточив внимание на распространенном участке важной мозговой артерии. Для каждого случая были доступны полные трехмерные поля скорости и давления за весь сердечный цикл. Чтобы дать модели сильное представление об основной физике, они сделали больше, чем простое воспроизведение скоростей: добавили дополнительные признаки, описывающие скорость входящего в артерию потока и его ускорение, и штрафовали ИИ всякий раз, когда его предсказания нарушали базовые законы гидродинамики, такие как сохранение массы.
Взгляд внутрь опасного выпячивания
После обучения ИИ мог взять один кадр информации о кровотоке и быстро прокручивать его вперед во времени, воспроизводя завихрения и зоны рециркуляции внутри мешка аневризмы. По сравнению с исходными моделированиями его краткосрочные ошибки уже были невелики, но настоящая проверка заключалась в том, не накопятся ли ошибки при прогнозировании десятков шагов вперед. Усиленная версия с физическими ограничениями прошла этот тест: за 50 шагов прогнозирования её ошибки были более чем в шесть раз меньше, чем у простой базовой модели, и она отслеживала изменение потока даже в самые турбулентные фазы сердечного цикла. Когда команда преобразовала эти поля скоростей в клинически релевантные метрики — например, среднюю касательную напряжённость стенки над куполом аневризмы — ИИ оставался примерно в пределах 10 процентов от эталонных значений и воспроизводил области с наибольшими нагрузками.
Обобщение за пределами обучающего набора
Ключевой вопрос для любого медицинского ИИ — сможет ли он справляться с пациентами, которых он никогда не видел. Команда проверила свою модель в двух типах незнакомых ситуаций без дополнительного обучения. Во‑первых, они изменили формы входных волн, чтобы соответствовать паттернам, измеренным в других мозговых артериях. ИИ по‑прежнему следовал новой синхронизации и силе каждого пульса, сохраняя умеренные ошибки и захватывая изменённую структуру потока внутри выпячивания. Во‑вторых, они протестировали её на четырёх полностью пациент‑специфичных геометриях аневризм с разными размерами, шириной шейки и траекторией сосудов. Хотя уровни скоростей иногда отличались, модель воспроизводила основные структуры потока и зоны воздействия, что указывает на то, что она усвоила базовое поведение, а не просто запомнила формы из обучения.
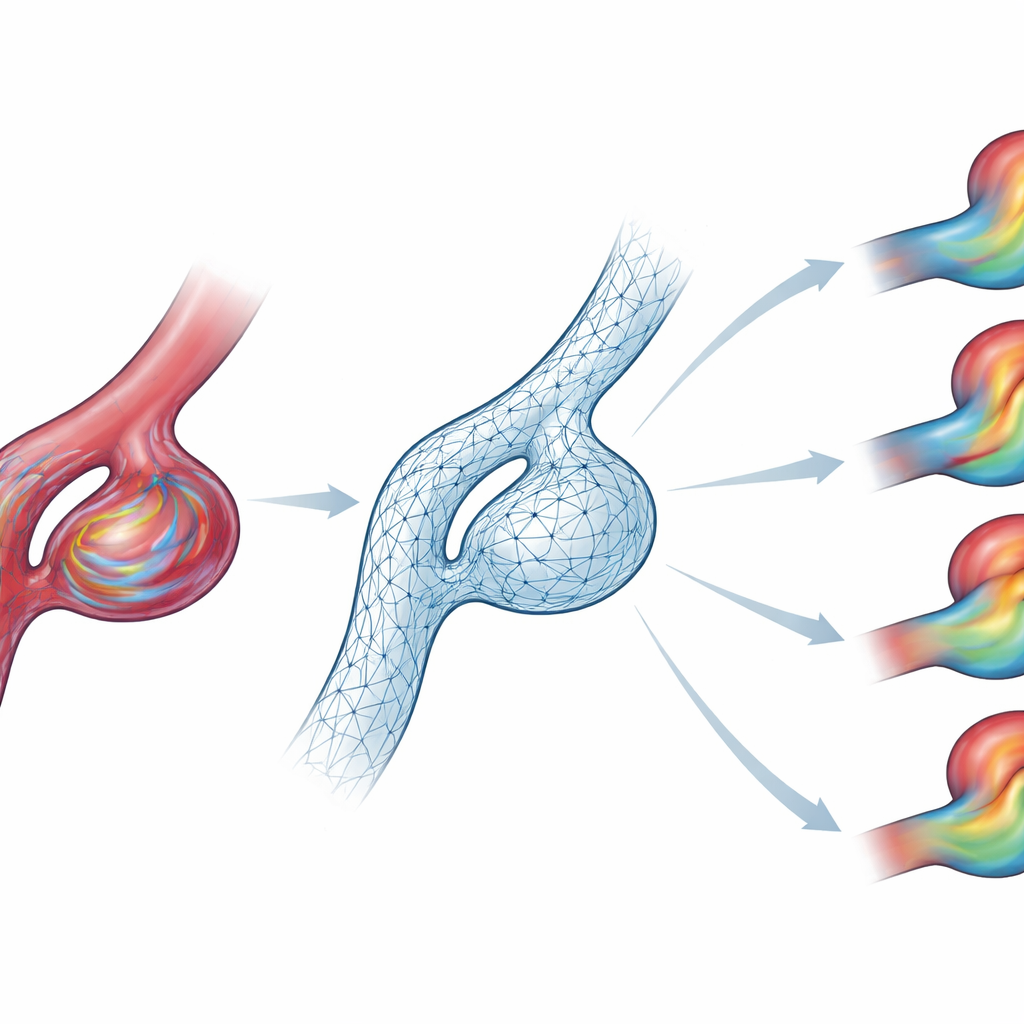
Более быстрые ответы у постели больного
Поскольку этот ИИ работает примерно в шестьдесят раз быстрее традиционных симуляций, на которых он обучался, он становится эффективнее стандартных методов уже после нескольких десятков случаев и в перспективе может выдавать полевые прогнозы кровотока менее чем за минуту. Авторы подчёркивают, что их инструмент не является автономным предсказателем разрыва; скорее, это быстрый движок для генерации физически согласованных карт потока и напряжений на стенке, которые могут использовать другие модели риска. Они также публикуют свой набор из 105 случаев в качестве открытого эталона, чтобы другие группы могли строить и сравнивать улучшенные модели. При дальнейшем обучении на более реалистичных формах сосудов и пациент‑специфичных входных данных этот подход может помочь перенести сложный анализ кровотока из суперкомпьютерной лаборатории в повседневную клиническую практику для людей с аневризмами мозга.
Цитирование: Lannelongue, V., Garnier, P., Jeken-Rico, P. et al. Physics constrained graph neural network for real time prediction of intracranial aneurysm hemodynamics. npj Digit. Med. 9, 212 (2026). https://doi.org/10.1038/s41746-026-02404-z
Ключевые слова: аневризма мозга, кровоток, графовая нейронная сеть, вычислительное моделирование, цифровая медицина