Clear Sky Science · ru
Расшифровка иммунорегуляторной оси ERS–CAF с помощью мультимодального ИИ и её прогностическое и терапевтическое значение в пан‑раке
Заглянуть в опухоль без скальпеля
Онкологи всё чаще признают, что окружение опухоли может быть столь же важно, как и сама опухоль. Но многократные биопсии этого скрытого «соседства» инвазивны и часто непрактичны. В этом исследовании показано, как искусственный интеллект (ИИ) может «читать» рутинные медицинские снимки и микроскопические изображения, чтобы делать выводы о трудноизмеримых иммунных и рубцовых процессах внутри опухолей, потенциально превращая повседневную визуализацию в своего рода «цифровую биопсию», применимую к разным видам рака.
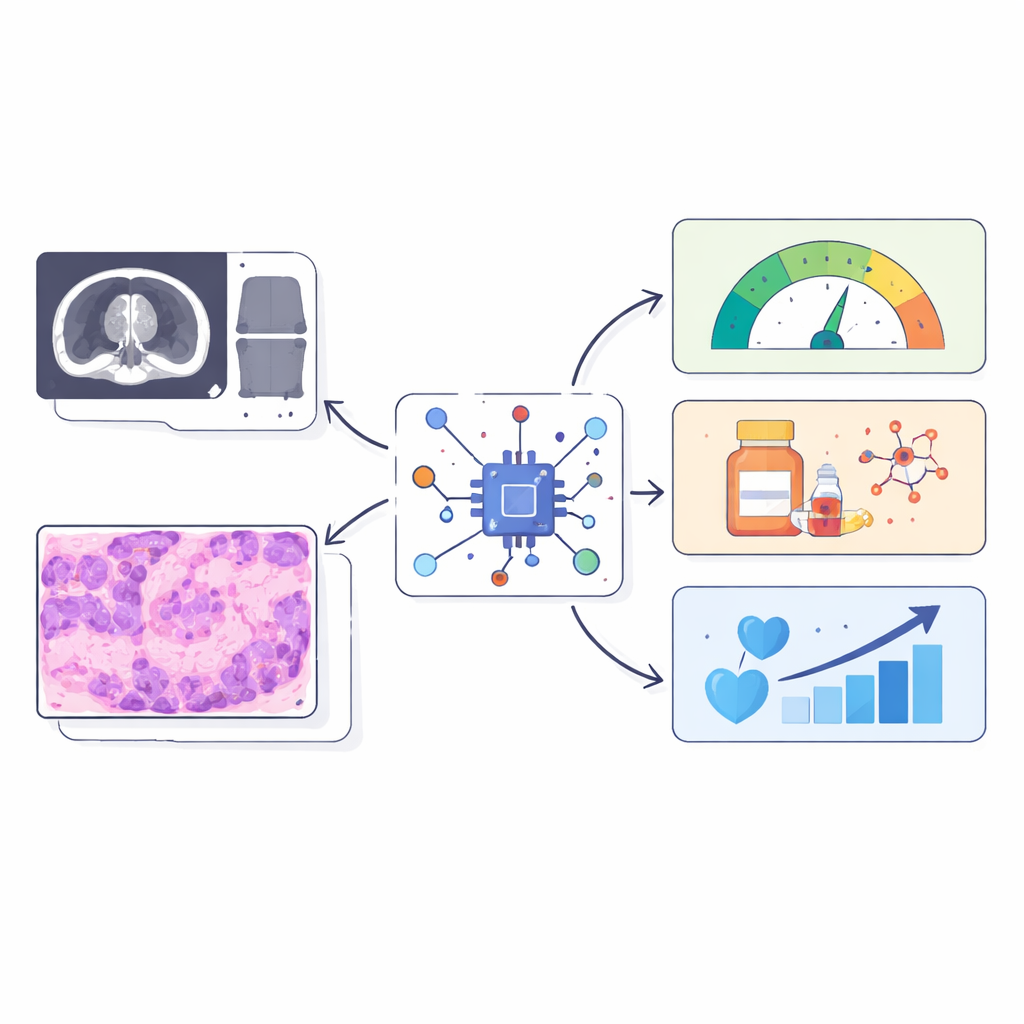
Скрытые клетки‑опора, формирующие течение рака
Многие солидные опухоли окружены плотной фиброзной оболочкой, которую создают специализированные поддерживающие клетки — фибробласты. Когда эти клетки испытывают стресс в белково‑синтетическом аппарате клетки (эндоплазматическом ретикулуме), они переходят в агрессивное состояние, способствующее росту рака. При хордоме, редком опухолевом поражении кости, такие стрессовые фибробласты формируют плотный матрикс и препятствуют проникновению иммунных клеток, что снижает эффективность лечения. Подобные фиброзные, бедные иммунитетом среды наблюдаются и при других видах рака, например при опухолях поджелудочной и толстой кишки, что указывает на то, что эта биология не ограничивается одним заболеванием. Проблема в том, что текущие методы оценки таких стрессовых фибробластов и их иммуноблокирующего поведения опираются на образцы ткани и сложные молекулярные тесты, которые трудно повторять и которые могут не охватывать важные участки опухоли.
Обучение ИИ видеть невидимую биологию
Исследователи поставили вопрос, содержат ли стандартные предоперационные МРТ‑снимки и рутинные патологические срезы H&E визуальные подсказки о барьере из стрессовых фибробластов и исключённого иммунитета. Они создали три числовых «эталонных индекса» на основе РНК‑секвенирования опухолей: один отражает активность стрессовой программы в фибробластах, второй суммирует, насколько сильно эти клетки, по‑видимому, сигнализируют иммунным клеткам, и третий характеризует разнообразие окружающих иммунных и поддерживающих популяций клеток. Вместо прогнозирования тысяч генов, их ИИ обучали предсказывать лишь эти три биологически содержательных показателя по изображениям. Для этого команда объединила два направления: одно анализирует текстуру и форму на МРТ, а другое просматривает тысячи небольших областей на цифровом срезе и использует механизм внимания, направляемый языковыми описаниями, чтобы фокусироваться на участках, соответствующих экспертным описаниям фиброзной, бедной иммунитетом ткани.
Слияние снимков и срезов для более сильного сигнала
На выборке из 126 пациентов с хордомой, у которых были сопоставленные МРТ, патологические срезы, РНК‑данные и наблюдение, объединённая мультимодальная модель ИИ превзошла модели, использовавшие только МРТ или только срезы. Прогнозы трёх молекулярных индексов хорошо согласовывались с измерениями по РНК и оставались корректно калиброванными в разных больницах и на разных аппаратах. Когда патологи независимо отмечали фиброзные и иммунопокинутые области, «горячие точки» ИИ обычно совпадали с этими участками, что наводит на мысль, что модель отслеживает реальную биологию, а не только размер опухоли. Модель также уловила прогностическую информацию: более высокие предсказанные показатели стресс‑фибробластов и сигнализации связывались с худшей выживаемостью, тогда как большая прогнозируемая разнообразность микроокружения частично защищала. Добавление этих ИИ‑показателей к рутинным клиническим факторам улучшало способность отделять пациентов с высоким и низким риском во времени.
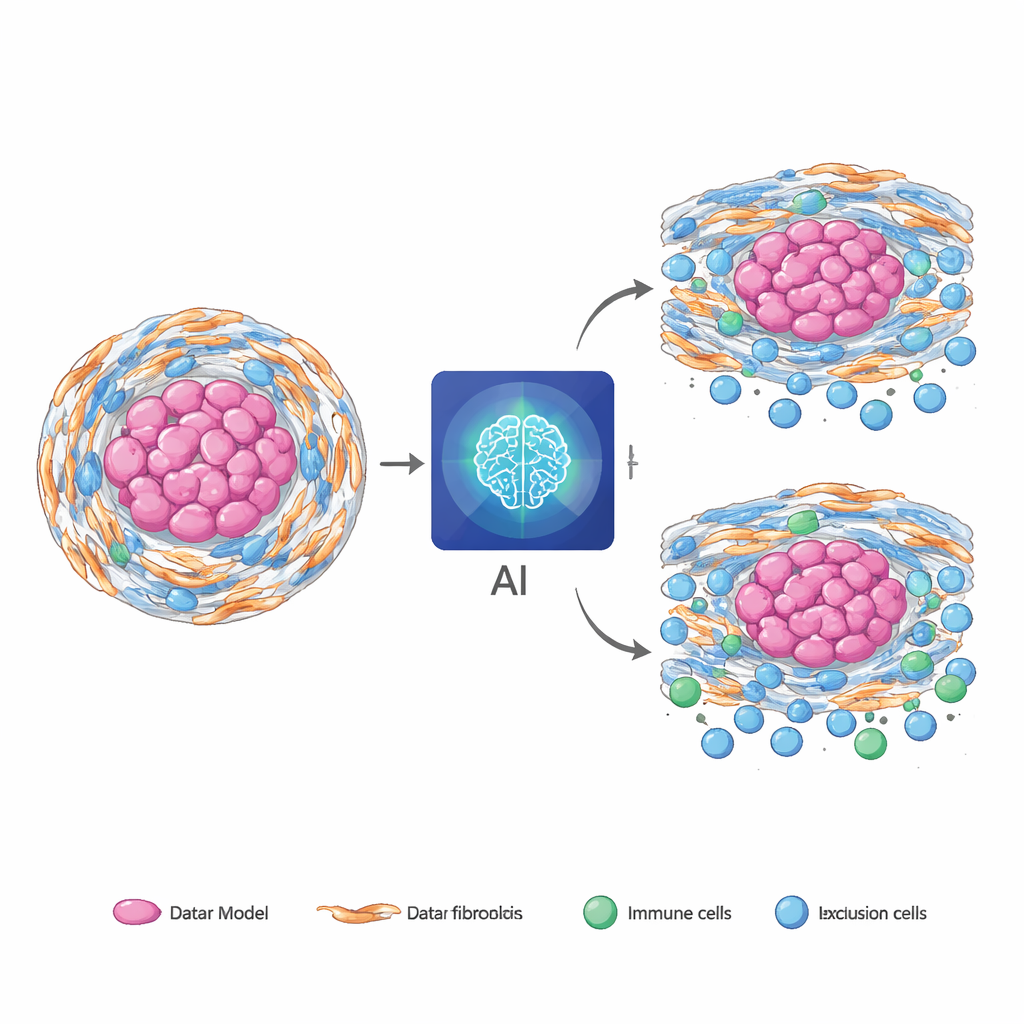
От редких опухолей к распространённым видам рака
Ключевым испытанием было, можно ли модель, обученную полностью на хордоме, применять «как есть» к другим, более распространённым опухолям. При применении без дообучения к опухолям поджелудочной, желудка и толстой кишки из крупных общедоступных наборов данных, версия модели, работающая только с срезами, всё ещё демонстрировала значимое соответствие между её предсказаниями по изображению и заново вычисленными РНК‑показателями. В некоторых из этих опухолей ИИ‑индикаторы улучшали прогноз выживаемости сверх стандартной клинической информации и помогали выделить пациентов, скорее всего получивших выгоду от химиотерапии. Чтобы упростить внедрение там, где цифровая патология ограничена, команда свела полную мультимодальную модель к версии только для МРТ, которая сохранила большую часть прогностической силы при более быстрой работе и меньших вычислительных затратах.
Что это может значить для пациентов
В совокупности результаты поддерживают идею о том, что рутинные медицинские изображения тихо кодируют информацию о стрессовых клетках‑опоре, иммунном исключении и разнообразии микроокружения — признаках, которые обычно требуют дорогих молекулярных тестов. Хотя текущее исследование ретроспективно и требует проспективной валидации, оно указывает на будущее, в котором стандартный снимок и срез могут неинвазивно выявлять опухоли с враждебным, фиброзным иммунным барьером, помогать определить, кому нужны дополнительные тесты или персонализированная терапия, и делать это для нескольких типов рака без дополнительной нагрузки на пациентов.
Цитирование: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Ключевые слова: микроокружение опухоли, изображения рака, искусственный интеллект, фибробласты, иммунотерапия