Clear Sky Science · ru
Алгоритмическое принятие решений при назначении антибиотиков при инфекциях мочевых путей с использованием предсказания пользы лечения, основанного на мнении назначающего врача
Более умный подход к антибиотикам при распространённых инфекциях
Инфекции мочевых путей (ИМП) — одна из самых частых причин назначения антибиотиков. Однако выбор правильного препарата — это баланс: врач должен вылечить инфекцию, избежать серьёзных побочных эффектов и защитить общество от роста антибиотикорезистентности. В этом исследовании представлен новый тип алгоритма принятия решений, который призван помогать клиницистам, сочетая крупномасштабные больничные данные с реальными приоритетами самих врачей, помогая выбирать антибиотики, эффективные для пациента и менее вредные для общества.
Проблема мощных препаратов
Современная медицина опирается на антибиотики, но чрезмерное использование широкого спектра, так называемых «тяжёлых» препаратов, способствует глобальному кризису антибактериальной резистентности. ООН поставила цель: к 2030 году 70% использования антибиотиков во всём мире должно приходиться на более узкие, первичные препараты, известные в классификации ВОЗ как «Access». На практике многие врачи склоняются к более широким препаратам, отмеченным как «Watch» или «Reserve», поскольку боятся, что узкий препарат может оказаться неэффективным против резистентных бактерий, особенно у тяжёлобольных пациентов. В результате мы часто меняем долгосрочные риски резистентности на краткосрочное спокойствие, не имея ясных инструментов для оценки, когда более безопасный узконаправленный препарат действительно сработает не хуже.
Обучение алгоритма думать как клиницист
Исследователи создали алгоритм принятия решений по антибиотикам при ИМП, используя подробные электронные записи почти 94 000 госпитализированных пациентов в Бостоне. Сначала они натренировали модели прогнозирования для оценки, для 13 различных антибиотиков, насколько вероятно, что бактерии, вызвавшие ИМП, будут чувствительны к препарату, и какова вероятность развития таких проблем, как инфекция Clostridioides difficile или серьёзная токсичность лекарства. Затем они попросили 49 клиницистов из Великобритании разных специальностей пройти онлайн-опрос, в котором участники ранжировали вымышленные антибиотики, отличающиеся по таким характеристикам, как риск побочных эффектов, пригодность для ИМП, стоимость, категория Access или Watch/Reserve и форма выпуска (таблетки или внутривенное введение). Анализируя эти ранжирования, команда количественно оценили, насколько сильно врачи ценят каждую характеристику — например, насколько они предпочитают ориентированные на ИМП, с низкой токсичностью, пероральные препараты по сравнению с более рискованными или мощными опциями.
Добавление страховки для очень больных пациентов
Финальный алгоритм объединил эти два компонента: предсказания на основе данных и суждения клиницистов о ценностях. Для каждого пациента он вычислял «ценность лечения» для каждого антибиотика, учитывая предсказанную вероятность эффективности препарата, шанс серьёзных побочных эффектов, категорию Access/Watch/Reserve и форму введения. Важной особенностью была встроенная защитная мера, основанная на степени тяжести состояния пациента в отделении неотложной помощи. По мере роста тяжести болезни алгоритм автоматически придавал больше веса агрессивному лечению и наличию внутривенного варианта. Иными словами, для пациентов с лёгким течением он стремился предпочесть узкие, пероральные препараты, но по мере ухудшения состояния становился более склонен к использованию более мощных внутривенных антибиотиков, чтобы защитить пациента от неудачи лечения.
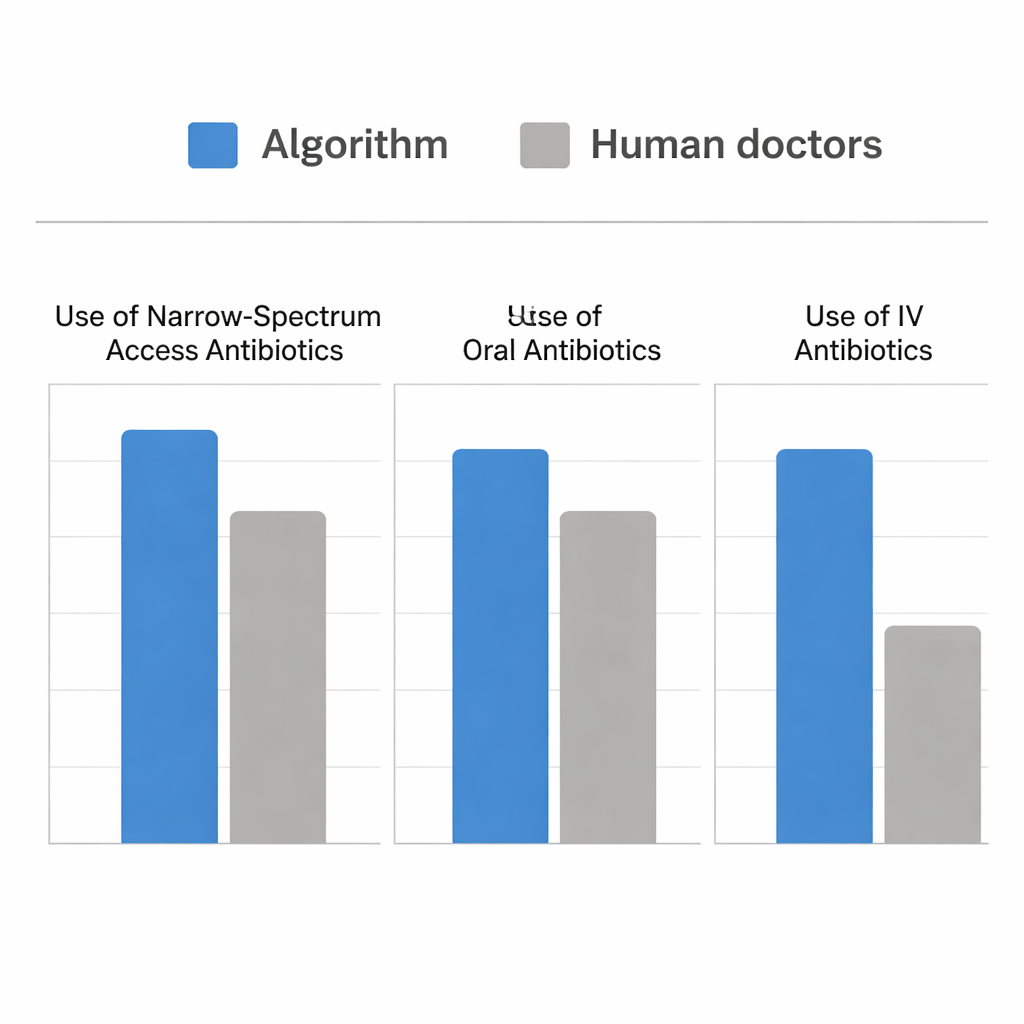
Как алгоритм показал себя по сравнению с врачами
Затем команда провела имитацию на реальных случаях из отделения неотложной помощи, где пациенты имели ИМП и посев мочи. Они сравнили антибиотики, которые реально назначали врачи, с теми, которые алгоритм выбрал бы в момент отправки посева. Обе стратегии одинаково хорошо подбирали антибиотик, покрывающий выделенную у пациента бактерию. Однако алгоритм делал это, при этом выбирая гораздо больше узкоспектральных препаратов категории Access и значительно чаще пероральные формы, используя меньше внутривенных антибиотиков. Для более тяжёлых пациентов алгоритм вел себя похоже на назначающих врачей, соответствующим образом смещаясь в сторону внутривенных и более мощных препаратов. Отличие заключалось в том, что алгоритм выявлял дополнительные возможности — особенно у пациентов со средней степенью тяжести — безопасно лечить пероральными препаратами категории Access, такими как нитрофурантоин и ампициллин-сульбактам, вместо того чтобы по умолчанию переходить к более широким опциям.
Что это значит для повседневной помощи
Для непрофессионального читателя ключевая мысль в том, что эта система не заменяет врачей; скорее, она работает как калькулятор для сложных соотношений риска и выгоды, о которых клиницисты уже задумываются, но которые трудно точно вычислить в уме. Объединив приоритеты самих врачей с крупномасштабными данными о том, как действуют антибиотики, алгоритм может предлагать схемы лечения, столь же эффективные для отдельных пациентов, но более бережные для организма и общественного здоровья — предпочитая таблетки капельницам, когда это безопасно, и узкие препараты вместо крайних вариантов, когда возможно. При подтверждении в других условиях такие инструменты могли бы помочь больницам и системам здравоохранения приблизиться к глобальным целям ответственного использования антибиотиков, не жертвуя безопасностью людей, поступающих с тяжёлыми инфекциями.
Цитирование: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Ключевые слова: инфекция мочевых путей, рациональное использование антибиотиков, поддержка клинических решений, антибактериальная резистентность, машинное обучение в медицине