Clear Sky Science · ru
Применение и перспективы искусственного интеллекта в диагностической визуализации рака предстательной железы
Почему более умные обследования важны для мужского здоровья
Рак предстательной железы — одно из самых распространённых онкологических заболеваний у мужчин; его раннее обнаружение часто определяет разницу между локальной проблемой и опасной для жизни болезнью. В этом обзоре объясняется, как искусственный интеллект (ИИ) внедряется в современные медицинские исследования, чтобы выявлять рак предстательной железы раньше, оценивать его агрессивность и отслеживать эффективность лечения. Для читателя это окно в мир, где компьютеры становятся тихими партнёрами в кабинете рентгенолога, помогая врачам принимать более быстрые и последовательные решения, но одновременно порождая новые вопросы о данных, справедливости и доверии.
От размытых теней к богатым данным изображениям
Врачи пользуются несколькими методами визуализации при подозрении на рак предстательной железы. Ультразвук быстр и недорог, но с трудом отличает опухоль от доброкачественного увеличения или воспаления. Магнитно‑резонансная томография (МРТ) даёт подробные изображения мягких тканей и сейчас является основным тестом для выявления клинически значимого рака, но её интерпретация занимает время и даже специалисты нередко расходятся во мнениях. ПЭТ/КТ с трассерами, связывающимися с белком PSMA на опухолевых клетках, отлично выявляет метастазы в костях и лимфоузлах, но может пропускать очень мелкие очаги и дорого обходится. ИИ не заменяет эти приборы; он работает поверх получаемых изображений. Алгоритмы сначала очищают и сегментируют сканы, затем извлекают тонкие паттерны яркости, текстуры и формы. Эти невидимые признаки в сочетании с лабораторными результатами, например уровнем ПСА в крови, используются для обучения моделей, которые отмечают подозрительные области, оценивают риск рака и подсказывают, где брать биопсию или как оценивать ответ на лечение.
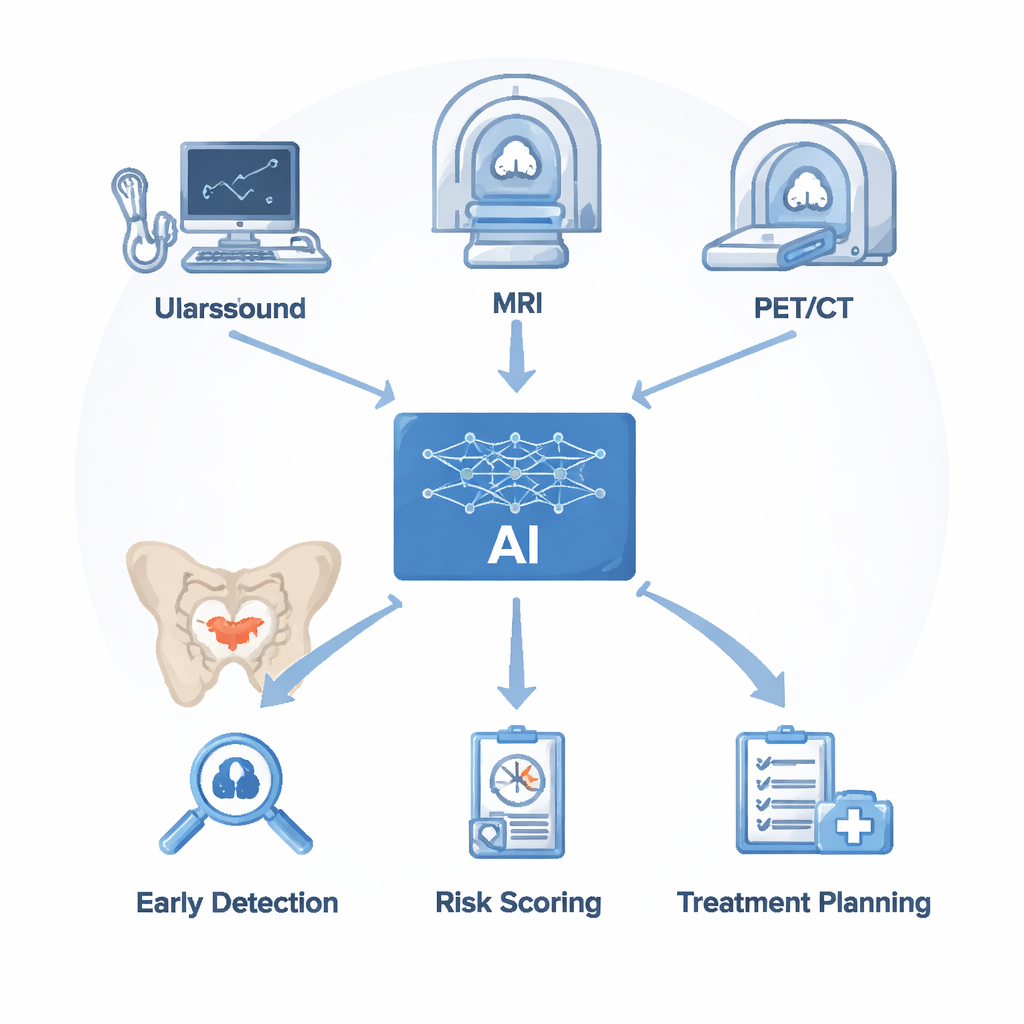
Обучая компьютеры видеть то, что пропускают рентгенологи
В ультразвуке системы ИИ обучаются на сотнях примеров, чтобы обнаруживать раковые зоны, которые могут сливаться с фоном. Модели глубокого обучения автоматически локализуют простату и выделяют вероятные опухоли в реальном времени, иногда сравнимо или превосходя опытных сонографистов, при этом сохраняя скорость и уменьшая число пропущенных мелких очагов. Подходы радиомики идут дальше, преобразуя ультразвуковые изображения в большие наборы числовых признаков, отражающих паттерны ткани, слишком сложные для человеческого глаза. Модели машинного обучения на этих признаках явно превзошли традиционный ультразвук и только ПСА, особенно у мужчин с уровнями ПСА в так называемой «серой зоне», где старые методы часто ошибаются почти в половине случаев. Похожая логика лежит в основе ИИ для МРТ: продвинутые сети автоматически очерчивают простату и её внутренние зоны, сокращая ручную контурную разметку примерно с 20 минут до чуть более минуты и значительно улучшая согласованность между разными ридерами.
Более точные оценки риска и умный мониторинг лечения
ИИ особенно эффективен, когда объединяет данные из нескольких последовательностей МРТ, показывающих анатомию, движение воды и кровоток. Модели на базе трансформеров, заимствованные из обработки естественного языка, синтезируют эти входы и создают карты вероятностей клинически значимых опухолей. При тестировании на больших когортах пациентов такие системы сравнимы или превосходят старших радиологов, особенно в обнаружении мелких опухолей менее сантиметра, которые люди часто пропускают. На динамической контрастной МРТ модели для анализа временных рядов читают кривые изменения яркости при введении контраста, оценивая проницаемость сосудов опухоли — показатель, связанный с более агрессивным течением и высоким риском рецидива. В PSMA ПЭТ/КТ трёхмерные сети, обученные на сканах всего тела, автоматически обнаруживают метастазы в костях и лимфоузлах, измеряют суммарную опухолевую нагрузку и связывают её с временем до прогрессирования заболевания. Другие инструменты ИИ сравнивают сканы до и вскоре после гормональной или химиотерапии, прогнозируя результаты лечения на несколько месяцев раньше, чем традиционные правила, основанные на простых изменениях захвата радиофармпрепарата.
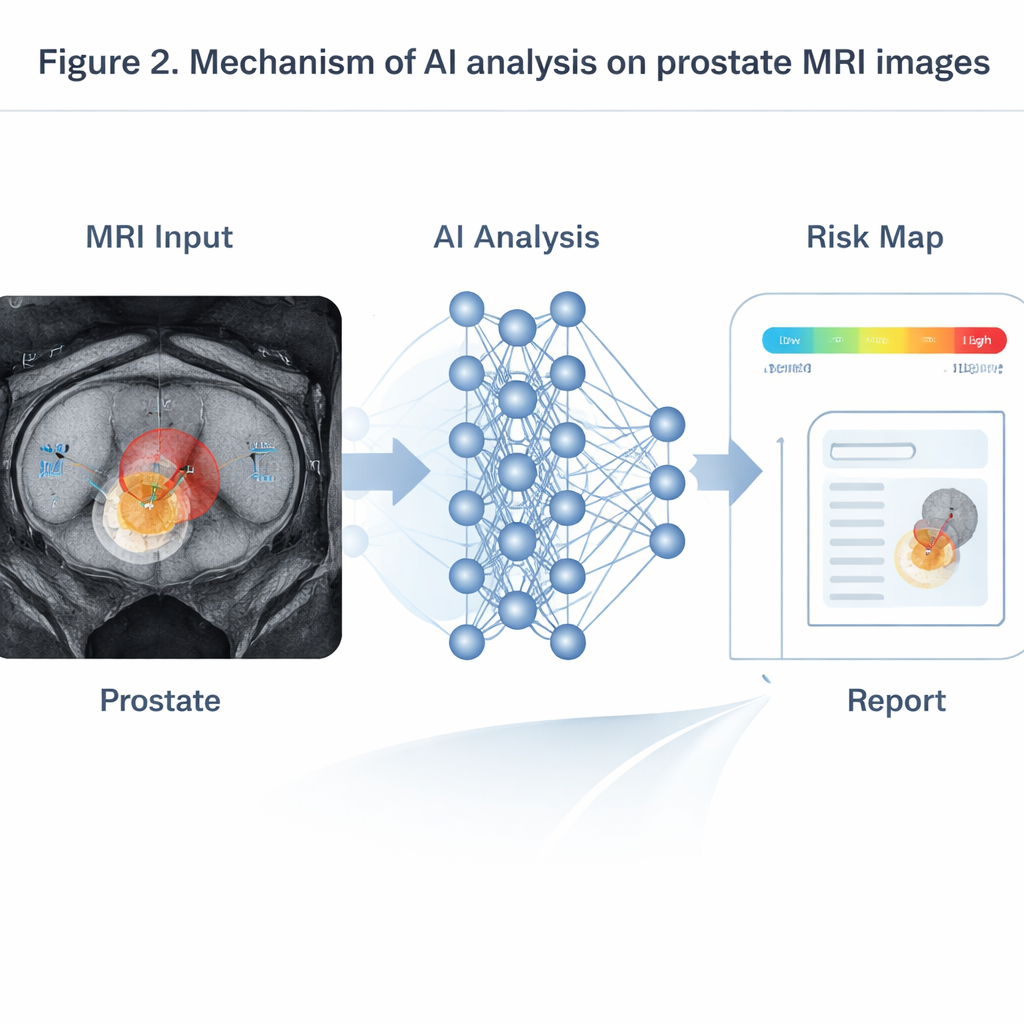
Препятствия: пробелы в данных, «чёрные ящики» и справедливое использование
Несмотря на достижения, внедрение в клинику сталкивается с серьёзными препятствиями. Высококачественных, хорошо размеченных наборов изображений по‑прежнему немного, и они смещены в сторону крупных академических центров, тогда как сканы из небольших клиник и разнообразных популяций представлены слабо. Тонкие различия между производителями томографов, настройками и качеством изображений могут привести к тому, что модели, обученные в одном месте, будут ошибаться в другом. Многие мощные ИИ‑системы функционируют как «чёрные ящики», выдавая риск‑скор без ясного объяснения, что подрывает доверие врачей — особенно когда компьютер расходится с клиническим опытом. Обзор также подчёркивает проблемы конфиденциальности, ограничения на обмен данными и риск того, что модели будут хуже работать для некоторых групп населения, потенциально увеличивая неравенство в здравоохранении, если это не отслеживать и не исправлять.
Создание заслуживающих доверия партнёров в клинике
Взгляд в будущее предполагает, что ИИ станет надёжным партнёром, а не таинственным оракулом. Авторы описывают усилия по созданию крупных совместных наборов данных между больницами при сохранении приватности с помощью методов вроде федеративного обучения, где обмениваются только обновлениями моделей, а не исходными пациентскими данными. Новые инструменты «объяснимого ИИ» призваны показывать, какие области изображения повлияли на решение, и связывать их с известной патологией, давая врачам ощутимые основания соглашаться или не соглашаться с выводом. Вместо универсальных моделей будут создаваться специализированные системы для конкретных задач: скрининг в загруженных клиниках, наведение при биопсии, мониторинг лечения или наблюдение за пациентами высокого риска. Комбинация визуализации с генетическими и клиническими данными может дополнительно уточнить прогноз и персонализировать терапию. Для пациентов итог обнадёживающий: при грамотном решении технических, этических и нормативных вопросов визуализация с поддержкой ИИ может привести к более раннему выявлению, меньшему числу ненужных биопсий, более быстрым ответам и более персонализированным планам лечения рака предстательной железы.
Цитирование: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Ключевые слова: визуализация рака предстательной железы, искусственный интеллект, МРТ и ультразвук, PSMA ПЭТ/КТ, радиомика