Clear Sky Science · ru
Маскированное автоэнкодирование, обобщаемая предобученность и интегрированные эксперты для улучшенной сегментации глиом
Почему более умные сканы важны при опухолях мозга
Глиомы — одни из самых смертоносных опухолей, и врачи по-прежнему тратят много времени на ручную обводку границ опухоли на МРТ. Это тщательное контурирование направляет хирургов и радиационные онкологи, но занимает 15–20 минут на пациента и требует повторений в динамике. В исследовании представлена MAGPIE — система искусственного интеллекта, которая обучается на десятках тысяч МРТ мозга без меток от людей, а затем требует лишь нескольких экспертно размеченных случаев, чтобы надежно выделять глиомы. Для пациентов это может означать более быструю и согласованную подготовку лечения даже в больницах без больших курируемых наборов данных.
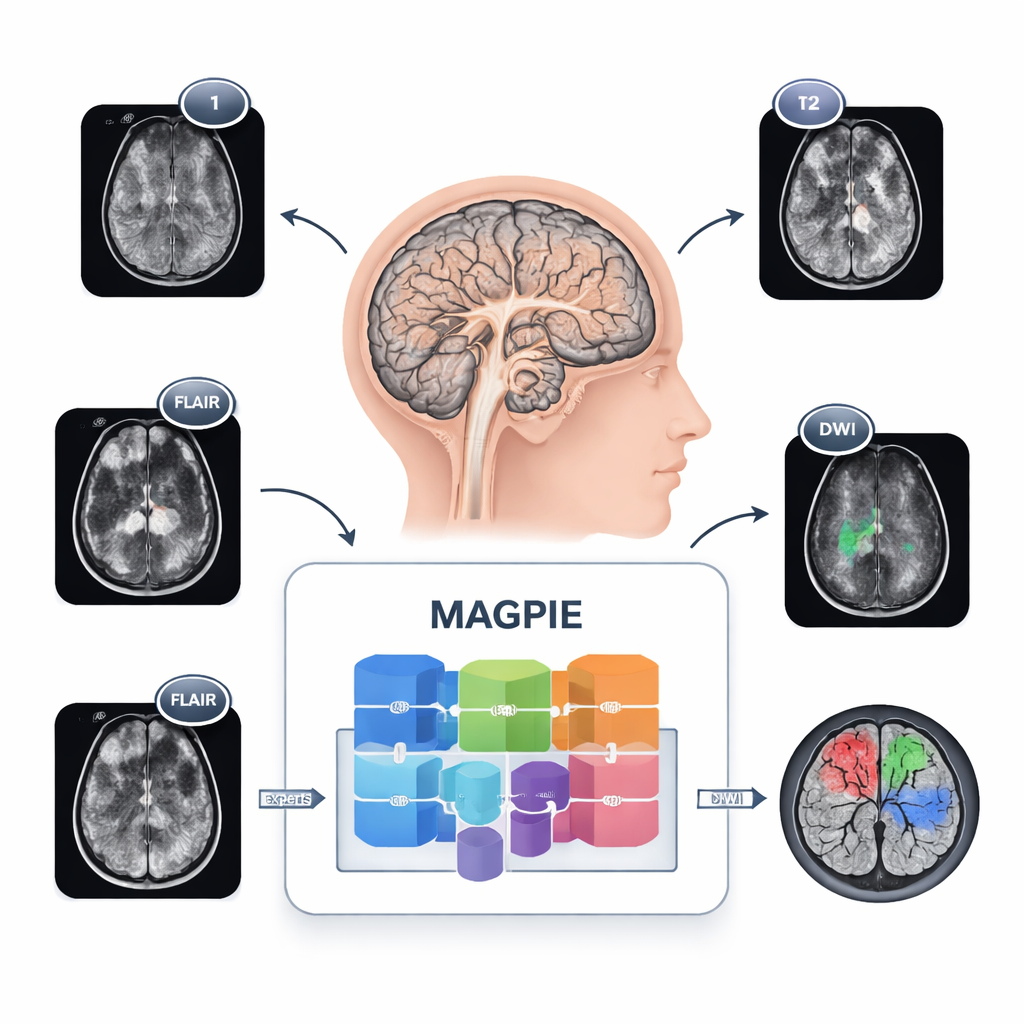
Новый взгляд на опухоли
Глиомы трудно картировать, потому что они не образуют аккуратных шаров. Раковые клетки распространяются вдоль проводящих путей мозга, создавая размытые края и крошечные сателлитные очаги, которые сложно заметить. Разные клиники используют разные настройки МРТ и комбинации последовательностей, поэтому инструмент, натренированный в одном месте, может давать сбои в другом. MAGPIE решает всё это одновременно. Система сначала была показана 43 505 немаркированных МРТ мозга, взятых из разных исследований и с разных сканеров. На этом этапе она изучала общие закономерности здоровой и поражённой ткани, восстанавливая отсутствующие фрагменты изображений и сопоставляя разные аугментированные виды одного и того же мозга — это заставляло модель фокусироваться на стабильных, значимых признаках, а не на хрупких пиксельных деталях.
Когда несколько экспертов делят работу
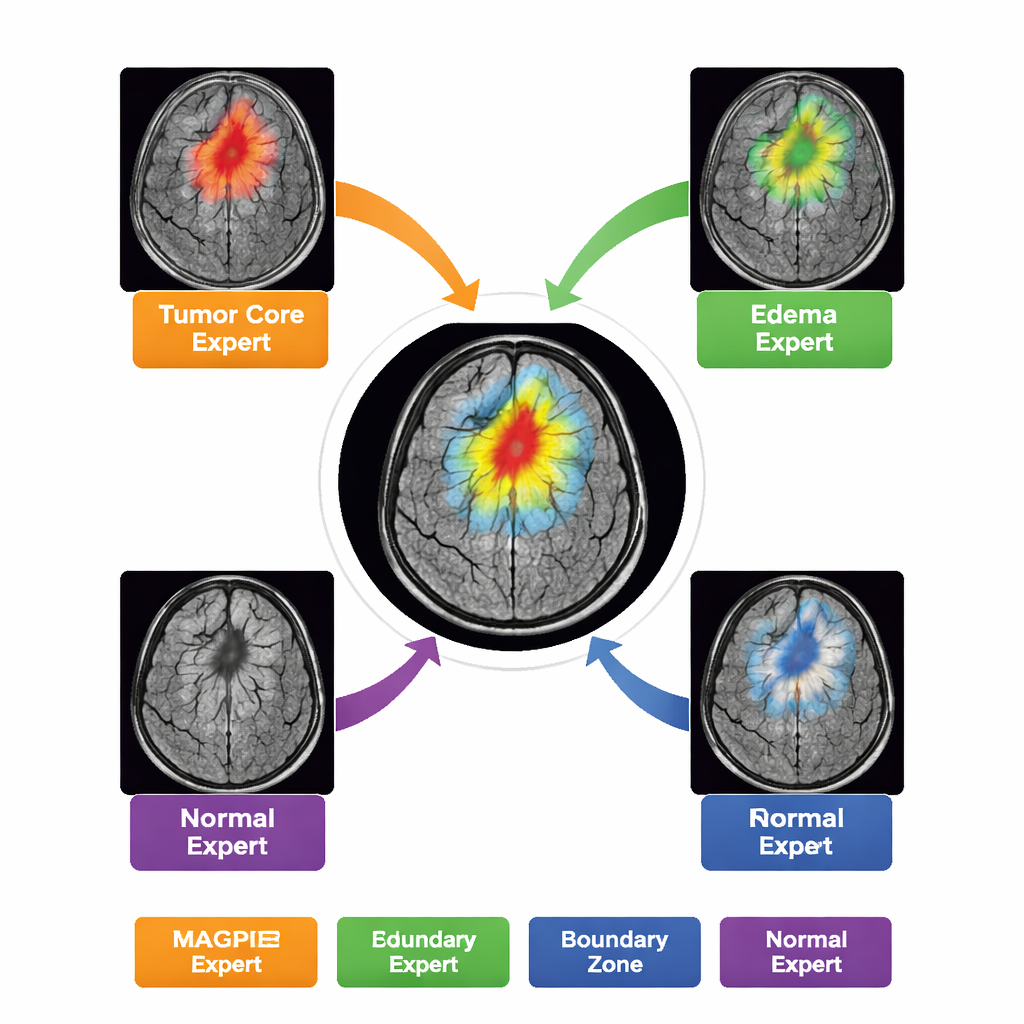
Вместо того чтобы быть монолитной моделью, MAGPIE содержит «смесь экспертов». При анализе нового скана она активирует лишь небольшой подмножество из восьми специализированных подсетей для каждого региона изображения. В процессе обучения эти эксперты естественно разделяют задачу: одни становятся чувствительны к яркому активно растущему краю опухоли; другие — к мёртвому ядру; третьи — к размытым зонам отёка вокруг опухоли; а некоторые сосредоточены в основном на нормальном фоне мозга и его границах. Авторы демонстрируют это, измеряя, насколько сильно активность каждого эксперта пересекается с разными зонами опухоли, размеченными радиологами. Такое разделение труда повышает точность и при этом держит вычисления в разумных пределах — для любого патча активна примерно половина параметров модели.
Работа с шумными, реальными сканами
Клинические МРТ‑протоколы далеки от единообразия. У некоторых пациентов четыре последовательности, у других — меньше; аппараты разных производителей дают слегка отличающиеся изображения. Архитектура MAGPIE рассматривает каждую последовательность МРТ как отдельный «токен» и учится в реальном времени определять, сколько веса давать каждой из них, вместо ожидания фиксированного набора входов в определённом порядке. Такой подход, независимый от каналов, позволяет системе адаптироваться, если, например, отсутствует контрастированная последовательность, но присутствует FLAIR. Модель также использует продвинутые механизмы внимания, которые позволяют ей одновременно «видеть далеко», улавливая дальнее распространение вдоль беломозговых трактов, и «видеть точно», замечая очень маленькие очаги в несколько миллиметров.
Больше результата при гораздо меньшем числе меток
После предобучения исследователи дообучили MAGPIE на всего 20 полностью размеченных случаях глиомы и сравнили её со стандартными моделями, обученными с нуля при тех же условиях. На крупном бенчмарке по опухолям мозга (BraTS21) MAGPIE показала Dice — распространённую метрику перекрытия в медицинской визуализации — около 61%, обойдя лучшую модель, обученную с нуля, примерно на 2,6 процентного пункта и превзойдя сильный предыдущий метод self-supervised без признаков вредного «отрицательного переноса». На сложных данных вне распределения — сканах из других заболеваний, с других сканеров и с другими настройками — она также держалась лучше, превысив 70% Dice на одном наборе с очагами в белом веществе без дополнительной настройки. Важно, что обычно такой уровень требует порядка 400 размеченных случаев; MAGPIE достигает этого при примерно 5% от этой работы.
Что это может значить для пациентов и клиник
Для неспециалистов главный вывод в том, что MAGPIE превращает огромный массив немаркированных МРТ в мощного ассистента, которому нужно очень мало экспертных меток, чтобы стать клинически полезным. Система может очерчивать сложные опухоли с реалистичными границами, обнаруживать мелкие сателлитные очаги, которые упускают другие алгоритмы, и надёжно работать, когда сканы приходят с незнакомых аппаратов или без некоторых последовательностей. Такое сочетание может сократить время аннотаций радиологов примерно на 95%, снизить барьеры для внедрения продвинутого ИИ в небольших больницах и поддержать более точное планирование операций и лучевой терапии. Хотя необходима дальнейшая валидация на редких типах опухолей и низкодифференцированных случаях, исследование показывает, как продуманное self-supervised обучение может приблизить надёжную и эффективную сегментацию опухолей мозга к повседневной клинической практике.
Цитирование: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Ключевые слова: сегментация глиомы, МРТ мозга, самостоятельное обучение (self-supervised), смесь экспертов, ИИ в медицинской визуализации