Clear Sky Science · ru
Ось сигналов AXL–SHC1 способствует адаптивной резистентности к тирозинкиназным ингибиторам, направленным на HER2, при HER2-аномалиях в раке лёгкого и желудка
Почему некоторые раки перехитряют новые лекарства
Таргетная противораковая терапия изменила подход к лечению многих пациентов, нацеливаясь на конкретные молекулы, поддерживающие рост опухоли. Тем не менее даже при этих точных препаратах стойкие и полные ремиссии встречаются редко. В этом исследовании поставлен насущный вопрос для пациентов с раком лёгкого и желудка, вызванным геном HER2: почему опухоли, которые изначально сокращаются под действием препаратов, блокирующих HER2, почти всегда оставляют за собой упорное ядро клеток, впоследствии обеспечивающее рецидив — и как врачи могли бы перекрыть этот путь бегства с самого начала?
Внимательнее к опухолям, управляемым HER2
HER2 — это сигнальный узел, который помогает клеткам расти и выживать. При его изменении или чрезмерной экспрессии нормальные клетки в молочной железе, желудке или лёгком могут превратиться в раковые. Несколько современных препаратов, называемых тирозинкиназными ингибиторами (TKI), разрабатываются для того, чтобы отключать HER2 внутри раковых клеток. Эти лекарства, включая мобоцертиниб и другие, могут уменьшать опухоли и задерживать прогрессирование. Однако при раке лёгкого и желудка их эффект часто оказывается временным. Небольшая часть клеток опухоли выдерживает первоначальную лекарственную атаку в состоянии толерантности к препарату и позднее эволюционирует в полностью резистентную опухоль. Понять, что поддерживает этих уцелевших клеток, важно для разработки более продуманных схем лечения первой линии.
Запасной коммуникационный путь под названием AXL
Исследователи скринировали клеточные линии рака лёгкого и желудка с изменённым HER2, чтобы выяснить, какие другие сигнальные переключатели помогают клеткам выдерживать действие HER2-таргетных TKI. Они выделили рецептор под названием AXL как ключевой элемент. При воздействии препаратов, блокирующих HER2, AXL активировался и оставался включённым, даже когда основные HER2-зависимые сигналы были ослаблены. Эта активация поддерживала важный путь выживания, известный как AKT–mTOR. Подавление AXL генетическими приёмами или блокирование его экспериментальными препаратами делало раковые клетки значительно более чувствительными к нескольким HER2-таргетным TKI, что в лабораторных условиях приводило к снижению роста клеток и увеличению их гибели.
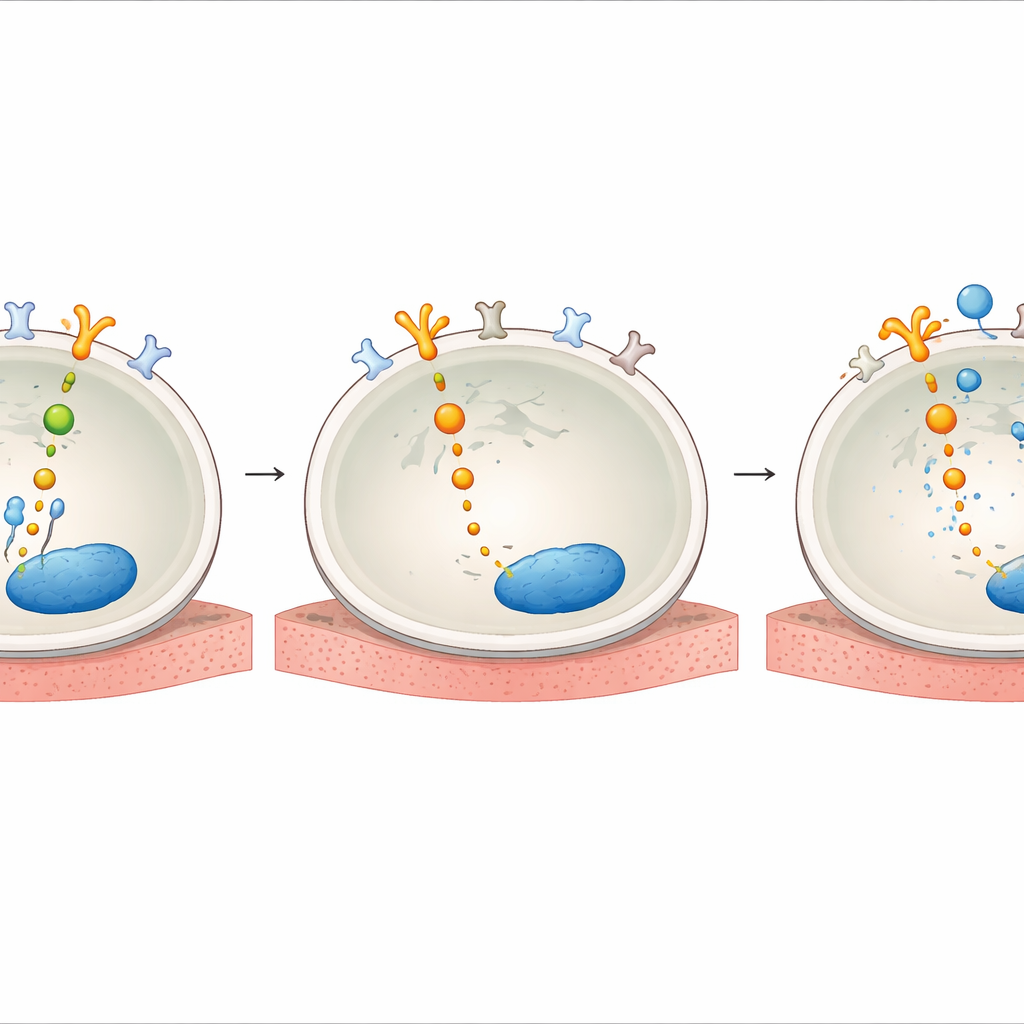
Как вспомогательные белки прокладывают путь к побегу
Далее команда изучала, как AXL становится столь влиятельным под давлением лекарства. Они обнаружили, что лечение HER2-TKI увеличивало уровни GAS6 — естественного лиганда, активирующего AXL на поверхности клетки. Также показано, что после воздействия препарата AXL физически связывался с HER2 и его родственниками EGFR и HER3, по сути подключаясь к той же цепочке выживания, которую обычно контролирует HER2. Внутри клетки адаптерные белки SHC1 и SHCBP1 выступали в роли монтажных узлов. Когда HER2 был блокирован, SHC1 отключался от SHCBP1 и вместо этого связывался с AXL, в то время как SHCBP1 перемещался в ядро, где способствовал продвижению клеточного цикла. Понижение экспрессии SHC1 или SHCBP1 ослабляло сигналы AKT и снижало выживаемость клеток, выявив ось AXL–SHC1–SHCBP1, которая поддерживает рост при ингибировании HER2.
Остановка лекарственно толерантных клеток до их укоренения
Чтобы смоделировать происходящее у пациентов, учёные позволили раковым клеткам расти в присутствии мобоцертиниба в течение нескольких дней, выделив небольшую популяцию, толерантную к препарату. Эти лекарственно толерантные клетки росли медленно, но были явно менее чувствительны к HER2-ингибитору, чем исходные клетки. Их выживаемость по-прежнему в значительной степени зависела от AXL: добавление блокатора AXL резко сократило их рост и подавило активность AKT. В мышиных моделях с HER2-изменёнными, AXL-позитивными опухолями лёгкого сочетание мобоцертиниба и ингибитора AXL сильнее уменьшало опухоли, снижало число делящихся клеток и увеличивало признаки запрограммированной клеточной гибели по сравнению с применением только HER2-препарата — без дополнительной токсичности. Опухоли, генетически модифицированные для сверхэкспрессии AXL, заметно хуже реагировали на мобоцертиниб в одиночку, но снова становились чувствительны при добавлении ингибитора AXL.
Что это может значить для будущего лечения
Важный вывод: образцы тканей пациентов с HER2-изменениями в лёгком и желудке показали, что примерно у четверти был высокий уровень AXL, а у большинства присутствовал хотя бы некоторый его уровень. Это указывает на то, что значительная группа пациентов могла бы получить пользу от стратегии лечения, сочетающей HER2-таргетный TKI с ингибитором AXL с первого дня, а не ожидая появления резистентности. Проще говоря, исследование показывает, что многие опухоли, управляемые HER2, держат запасной выключатель роста — AXL — в режиме готовности. Когда HER2 блокируется, AXL вступает в дело и поддерживает выживание раковых клеток. Одновременное отключение обоих переключателей приводит к гораздо большему числу гибнущих клеток и замедляет или предотвращает появление лекарственно толерантных выживших. Если это подтвердят клинические испытания, такой подход с двойной мишенью может привести к более продолжительному контролю над HER2-изменёнными раками лёгкого и желудка.
Цитирование: Ishida, M., Yamada, T., Katayama, Y. et al. AXL–SHC1 signaling axis mediates adaptive resistance to HER2-targeted tyrosine kinase inhibitors in HER2-aberrant lung and gastric cancers. npj Precis. Onc. 10, 142 (2026). https://doi.org/10.1038/s41698-026-01385-2
Ключевые слова: Терапия, направленная на HER2, ингибитор AXL, лекарственная резистентность, рак лёгкого, рак желудка