Clear Sky Science · ru
Ответ на мидостаурин при ОМЛ определяется состоянием клеток, близким к прогениторному, которые избирательно поражаются миметиками SMAC
Почему некоторые препараты от лейкемии перестают действовать
Для многих людей с видом рака крови, называемым острым миелоидным лейкозом (ОМЛ), новые таргетные препараты принесли надежду — но не все получают пользу, и ответы нередко со временем исчезают. В этом исследовании поставлен простой, но ключевой вопрос: почему некоторые клетки лейкемии игнорируют широко применяемый препарат мидостаурин, и можно ли найти разумную комбинированную терапию, которая заставит эти упрямые клетки погибнуть?
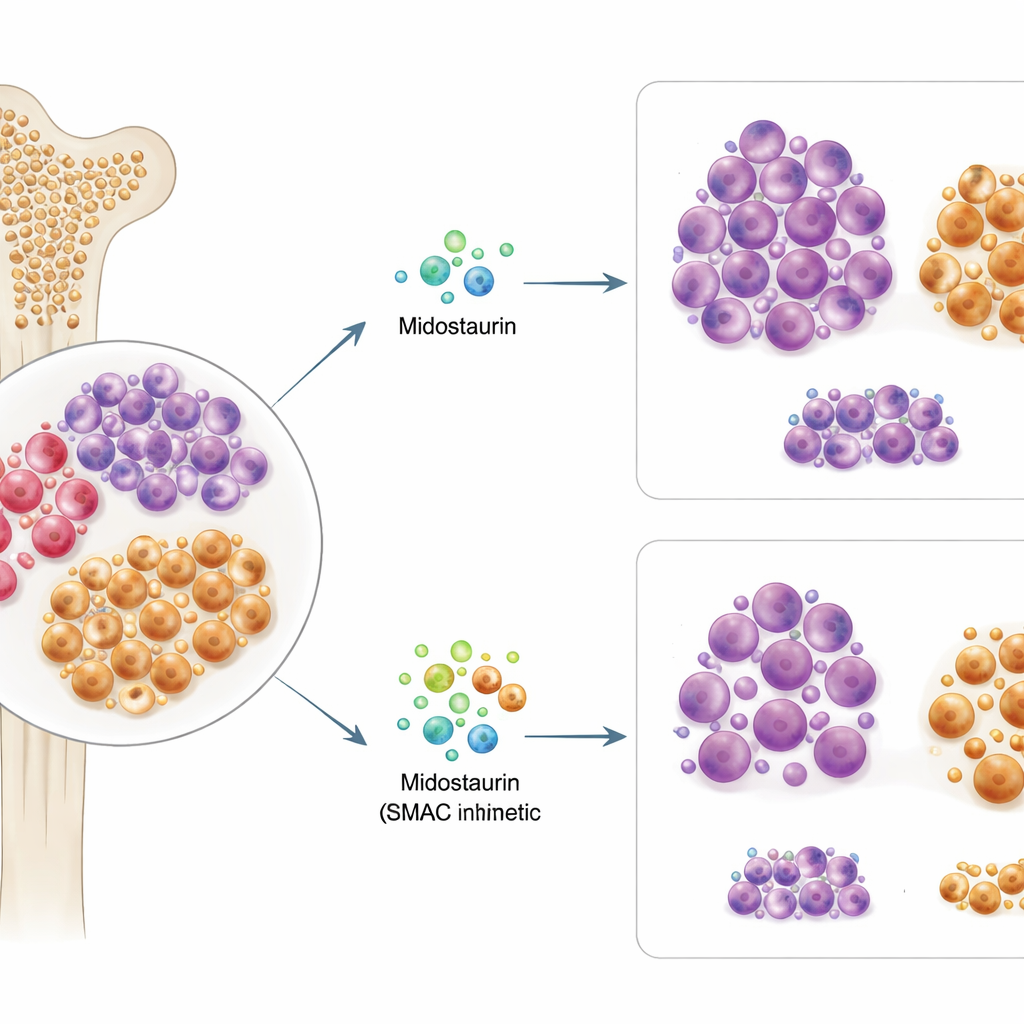
Смотреть дальше, чем на основную мутацию
Примерно у каждого третьего пациента с ОМЛ обнаруживается изменение в гене FLT3, которое стимулирует рост лейкемии и является причиной назначения мидостаурина. Исследователи протестировали образцы костного мозга и крови у 63 пациентов с мутацией FLT3, подвергая клетки воздействию мидостаурина и более чем 500 другим противораковым препаратам in vitro. Они обнаружили, что чувствительность клеток пациента к мидостаурину ex vivo тесно коррелировала с тем, как этот пациент позже ответил на лечение в клинике. Удивительно, но точный тип мутации FLT3 или её доля не могли надежно предсказать успех мидостаурина, что указывает на то, что одних только генетических данных недостаточно для объяснения, кто получит выгоду.
Скрытый пул упрямых «семенных» клеток
Углубляясь, команда сравнила общие шаблоны активности белков и генов между клетками, чувствительными к мидостаурину, и теми, что не отвечали. В образцах, не реагировавших на лечение, были обогащены признаки незрелых, стволоподобных прогениторных клеток — клеток, стоящих ближе к корню образования крови и считающихся «семенами», способными возобновить лейкоз. Напротив, реагировавшие образцы походили на частично зрелые иммунные и миелоидные клетки. С помощью современных методов одиночных клеток учёные выявили конкретную популяцию лейкемических клеток с маркерами поверхности CD38 и CD45RA, которые вели себя как эти прогенитороподобные «семена». Эти клетки демонстрировали необычную организацию наружной мембраны, что намекало на перестановку ключевых сигнальных молекул в пользу выживания.
Схема выживания: переключение сигнальных путей
Мидостаурин разработан для блокирования сигнала FLT3, который обычно запускает каскад сигналов, включающий молекулу STAT5 и способствующий росту клеток. Когда команда изучала сигнальную активность в клеточных линиях и образцах пациентов после лечения мидостаурином, они обнаружили два разных паттерна. В клетках, чувствительных к мидостаурину, активность STAT5 быстро падала, что согласуется с эффективным подавлением FLT3. В резистентных клетках доминировал другой путь: PI3K/AKT, классическая маршрут выживания, помогающий клеткам противостоять гибели. Эти устойчивые клетки сохраняли или даже увеличивали активность AKT после лечения и показывали более высокий уровень белков, блокирующих апоптоз (запрограммированную гибель). Иными словами, проводка внутри этих прогенитороподобных клеток была перенастроена в пользу выживания, даже когда FLT3 был ингибирован.
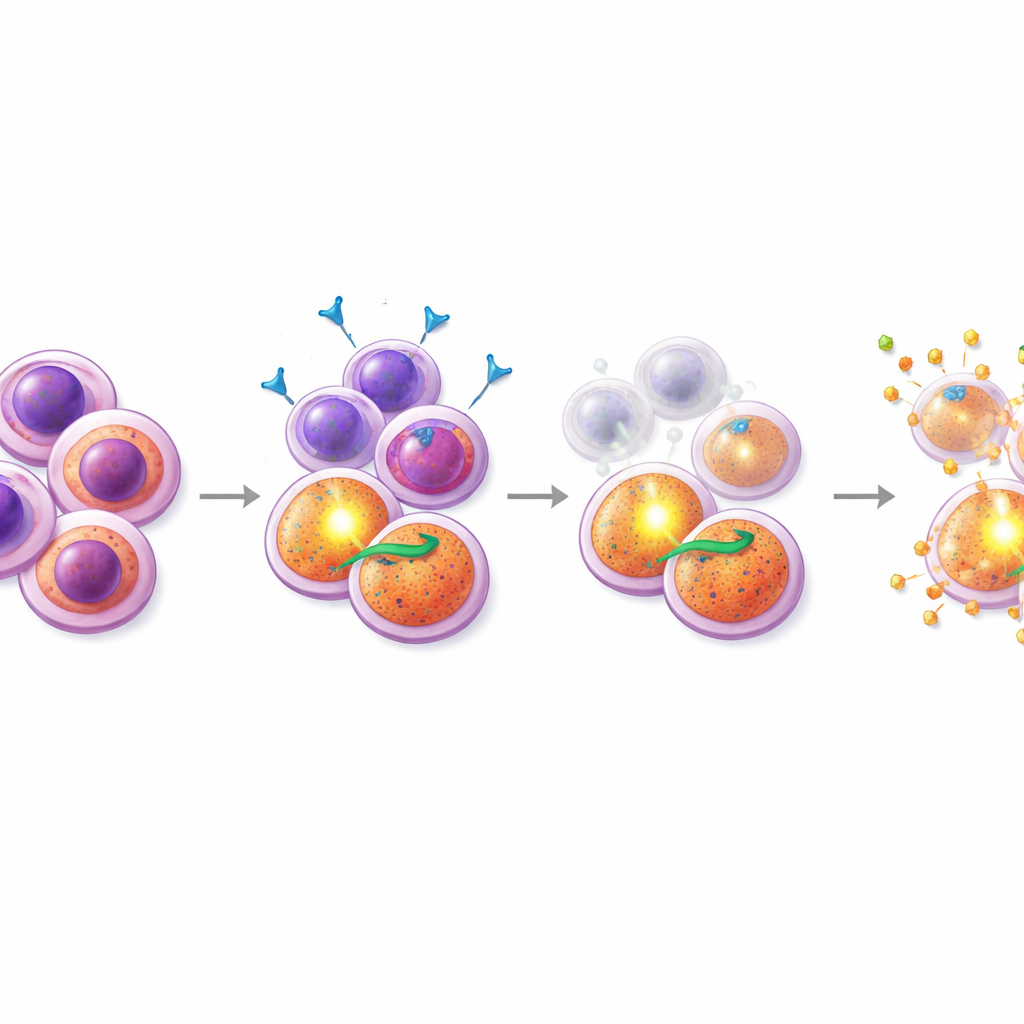
Поиск партнёра по лекарству, поражающего уязвимое место
Вооружённые этим пониманием, исследователи просcreenировали комбинации мидостаурина с сотнями других соединений, сосредоточившись на препаратах, влияющих на клеточную гибель. Одной из выделяющихся групп стали миметики SMAC — препараты, которые нейтрализуют белки «ингибиторы апоптоза», от которых зависят клетки с активированным PI3K/AKT. В резистентных образцах пациентов и в резистентной клеточной линии с мутацией FLT3 добавление миметиков SMAC, таких как биринапант, к мидостаурину давало сильный синергический эффект: вместе препараты убивали намного больше клеток, чем каждый по отдельности. Важно, что подробные эксперименты с проточной цитометрией показали, что комбинация мидостаурина и миметика SMAC избирательно истощала популяцию прогенитороподобных клеток CD38+CD45RA+ и снижала характерные уровни маркеров на поверхности, что указывает на то, что эта терапия специфически нацелена на трудноубиваемые «семена». В отличие от этого, комбинации с одобренным ингибитором BCL-2 венето кликсом (venetoclax) были более эффективны против другой популяции с высоким уровнем CD34 и не демонстрировали такого сфокусированного эффекта на резистентные клетки.
Что это означает для пациентов
Эта работа указывает на то, что резистентность к мидостаурину — это не только вопрос самой мутации FLT3, но и «состояния» лейкемических клеток — их уровня зрелости, организации мембраны и предпочитаемых путей выживания. Прогенитороподобная субпопуляция CD38+CD45RA+ представляется ключевым резервуаром резистентности, переключающим сигналы с обычного пути STAT5 на программу выживания PI3K/AKT. Сочетание мидостаурина с миметиками SMAC позволило восстановить чувствительность этих клеток и запустить их гибель в лаборатории. Хотя для клинического применения необходимы более крупные исследования, результаты указывают на будущее, в котором врачи могут использовать функциональное тестирование и профилирование состояния клеток, а не только секвенирование ДНК, чтобы выбирать комбинированные терапии, направленные и на массовую популяцию лейкемии, и на её наиболее устойчивые «семена».
Цитирование: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Ключевые слова: острый миелоидный лейкоз, ингибиторы FLT3, лекарственная устойчивость, лейкемические стволовые клетки, миметики SMAC