Clear Sky Science · ru
КФОЗА1высокие фибробласты, связанные с раком, координируют метаболические и иммунные микроокружения, обеспечивая хеморезистентность при раке молочной железы
Почему некоторые опухоли молочной железы игнорируют химиотерапию
Химиотерапия может спасать жизни при раке молочной железы, но у многих пациенток опухоли перестают отвечать на лечение или изначально плохо реагируют. В этом исследовании внимание обращено не только на сами раковые клетки, но и на их окружение: какие соседние клетки помогают опухоли пережить терапию и как именно? Ответ сосредоточен на особой группе клеток поддержки, которые перестраивают и питание опухоли, и местный иммунитет, защищая раковые клетки от химиотерапии.
Скрытые помощники вокруг опухоли
Опухоли молочной железы — это не только раковые клетки; это смешанные сообщества, включающие кровеносные сосуды, иммунные клетки и клетки соединительной ткани — фибробласты. Когда фибробласты находятся в опухоли, их называют фибробластами, ассоциированными с раком (ФАР, CAFs), и они могут как сдерживать, так и способствовать прогрессии рака. Совместив несколько мощных методов генетического профилирования на образцах пациентов — одиночно-клеточный, пространственный и бульковый анализы — а также лабораторные и животные эксперименты, исследователи выделили подгруппу ФАР, которая продуцирует высокие уровни молекулы COL3A1, компонента тканевого каркаса. У пациенток, чьи опухоли содержали больше таких COL3A1-высоких ФАР, чаще наблюдались плохие ответы на химиотерапию и худшие показатели выживаемости.
Двухсторонний щит: питание и защита
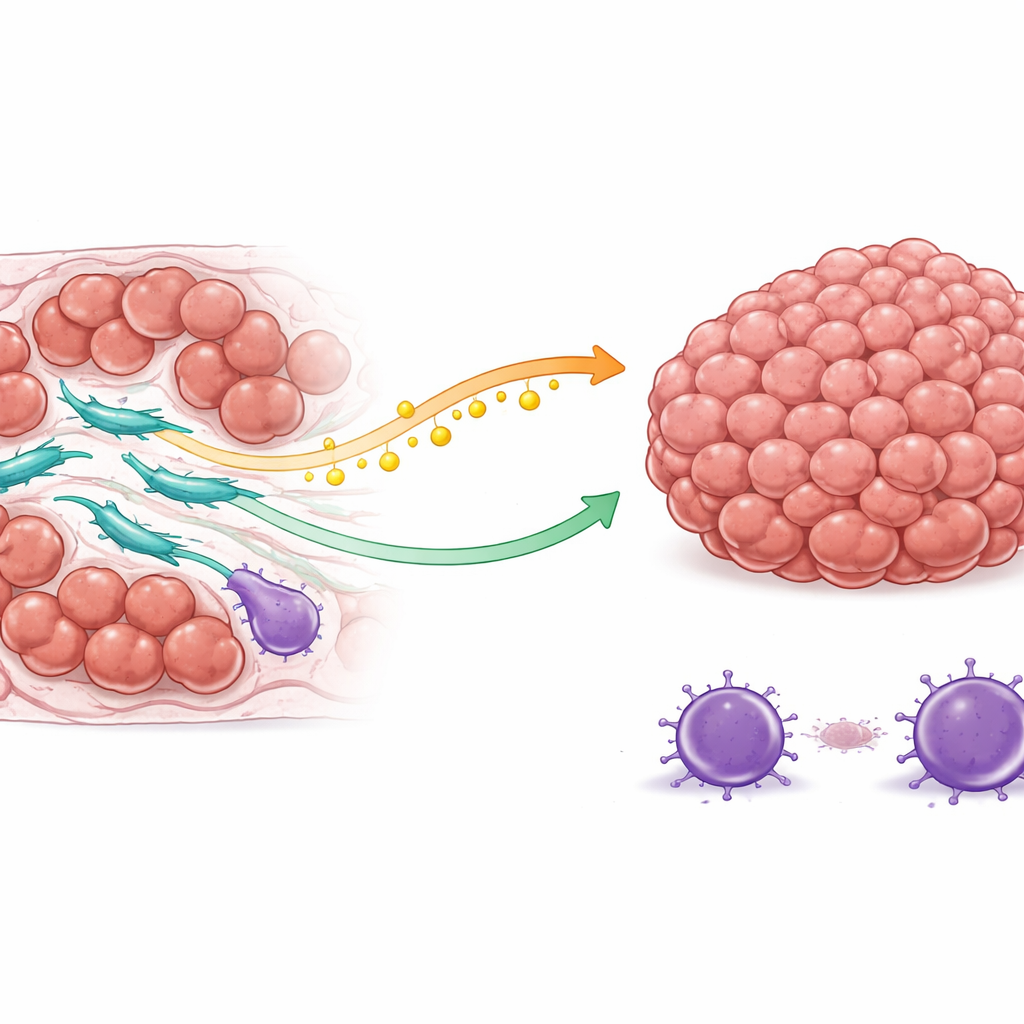
Команда обнаружила, что COL3A1-высокие ФАР защищают раковые клетки двумя основными способами. Во‑первых, они меняют обращение с жирами. Эти фибробласты увеличивают активность фермента, синтезирующего олеиновую кислоту — тип жира. Вместо того чтобы удерживать этот источник энергии, они выделяют её в опухолевое микроокружение. Раковые клетки захватывают олеиновую кислоту через белок на поверхности и в ответ активируют внутри себя сигнальный путь выживания, известный своей ролью в сопротивлении апоптозу. В результате, когда химиотерапия пытается запустить программы самоуничтожения в раковых клетках, эти клетки оказываются лучше подготовлены, чтобы сопротивляться и продолжать делиться.
Формирование враждебного иммунного окружения
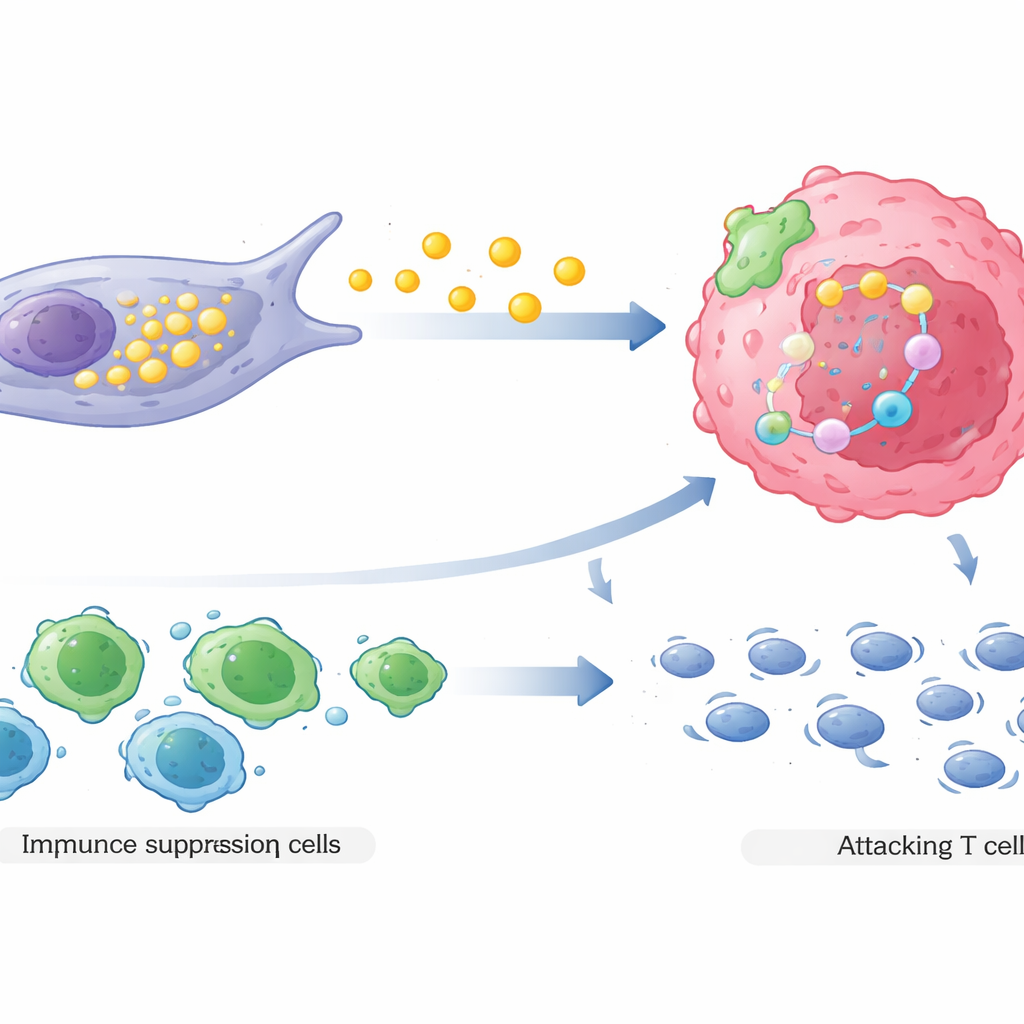
Во‑вторых, COL3A1-высокие ФАР перестраивают местный иммунный ландшафт в пользу опухоли. Через сложные сигнальные взаимодействия они притягивают регуляторные T‑клетки, тип иммунных клеток, приглушающих иммунную атаку, и одновременно отталкивают или ослабляют киллерные T‑клетки, которые обычно атакуют рак. Пространственное картирование реальных опухолей пациентов показало, что эти фибробласты склонны располагаться вблизи как лекарственно‑устойчивых раковых клеток, так и супрессивных иммунных клеток, в то время как эффективные киллерные T‑клетки отодвинуты дальше. Такая организация создаёт защищённую зону, где раковые клетки сталкиваются с меньшим количеством иммунных угроз одновременно с тем, что они становятся труднее убиваемыми препаратами.
Доказательства из клеток, мышей и пациентов
Чтобы проверить причинно‑следственную связь, исследователи уменьшили экспрессию COL3A1 в ФАР, выращенных в лаборатории. Когда раковые клетки молочной железы выращивали рядом с этими изменёнными фибробластами, они формировали меньше инвазивных структур, легче погибали под действием химиопрепарата паклитаксела и демонстрировали больше признаков программируемой клеточной смерти. У мышей, имплантированных смесями раковых клеток и ФАР, блокада COL3A1 в фибробластах замедляла рост опухолей при химиотерапии и снижала уровни фермента синтеза жиров и рецептора в раковых клетках, связанного с олеиновой кислотой. В когорте из 72 пациенток, получавших химиотерапию до операции, более высокие уровни COL3A1 и связанных с ним компонентов липидного обмена тесно коррелировали с худшими ответами на лечение и более коротким временем до рецидива.
Что это значит для будущего лечения
Проще говоря, исследование показывает, что конкретный набор клеток поддержки в опухолях молочной железы действует как отряд телохранителей: они кормят раковые клетки защитной жировой «диетой» и привлекают иммунных союзников, которые притупляют защиту организма. Совокупно эти действия делают химиотерапию менее эффективной. Измерение количества COL3A1-высоких фибробластов улучшает способность врачей прогнозировать, кто отреагирует на лечение, а используемые ими пути — синтез жиров, сигналы выживания внутри раковых клеток и иммунная супрессия — предлагают новые терапевтические мишени. В будущем терапии, которые обезвреживают или перепрограммируют эти фибробласты, можно будет сочетать со стандартной химиотерапией, чтобы предотвратить развитие резистентности опухолей.
Цитирование: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Ключевые слова: рак молочной железы, хеморезистентность, микроокружение опухоли, фибробласты, связанные с раком, липидный метаболизм