Clear Sky Science · ru
Прогнозирование дефицита гомологичной рекомбинации и ответа на лечение на основе компьютерной томографии с использованием фундаментальной модели: доклиническое исследование
Почему это важно для пациентов и врачей
Лечения рака, которые повреждают ДНК — например, некоторые химиопрепараты и новые таргетные препараты — могут быть особенно эффективны против опухолей с уже нарушенными системами репарации. Задача состоит в том, чтобы выявить такие «скрытые» слабости опухолей без множества инвазивных биопсий. В этом исследовании изучали, могут ли рутинные медицинские сканы у мышей, интерпретируемые мощной моделью искусственного интеллекта, выявлять уязвимость опухоли и прогнозировать, как хорошо она ответит на новый экспериментальный препарат.
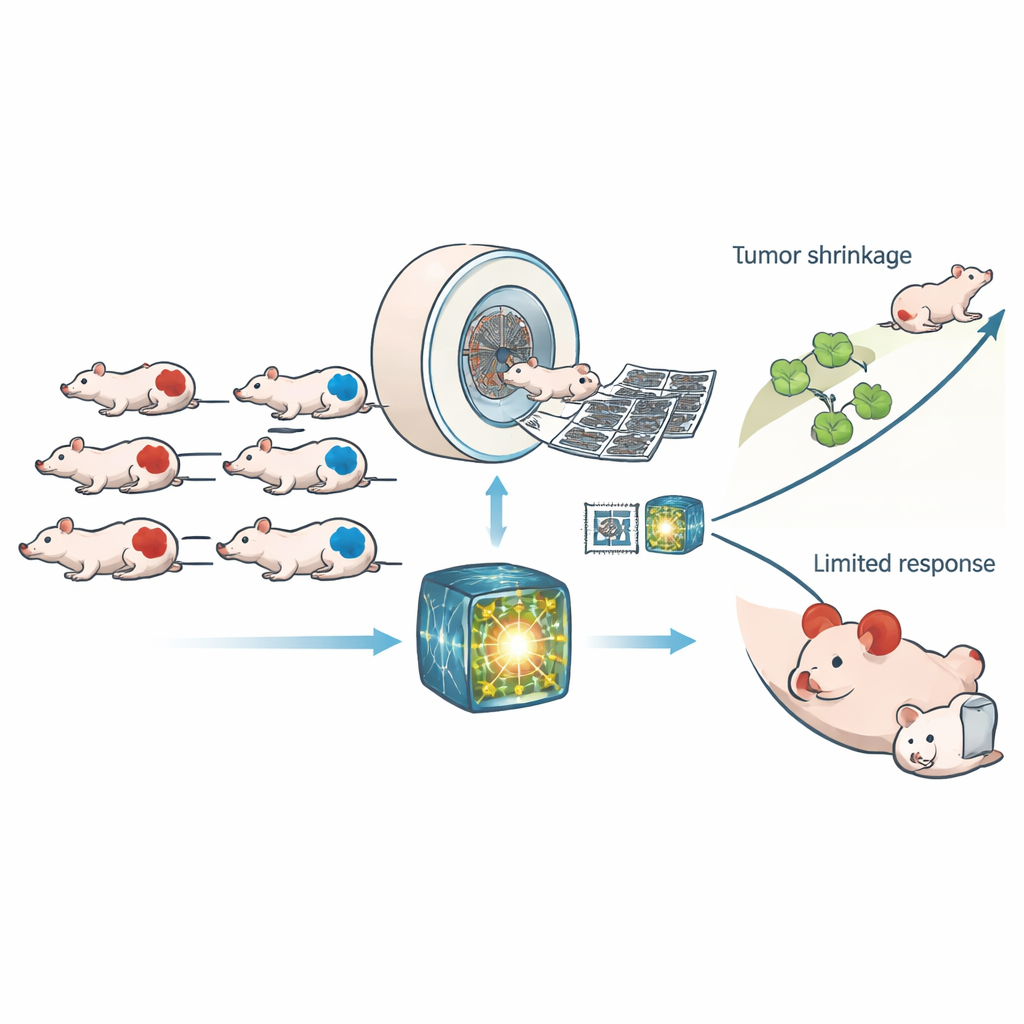
Скрытая уязвимость в клетках рака
Во многих опухолях имеются дефекты в ключевом пути репарации ДНК, называемом гомологичной рекомбинацией. При сбое этого пути в клетках накапливаются повреждения генетического материала — состояние, известное как дефицит гомологичной рекомбинации (HRD). HRD может способствовать развитию рака, но одновременно становится его ахиллесовой пятой: препараты, дополнительно повреждающие ДНК, способны вывести такие уже ослабленные клетки из строя, убивая их эффективнее, чем здоровые клетки. Сегодня идентификация HRD обычно требует генетических тестов или специализированных лабораторных анализов, которые дорогостоящи, занимают время и часто требуют взятия образцов опухоли. Авторы задали вопрос, может ли визуализация — те же трёхмерные рентгеновские сканы, широко применяемые в клиниках — предоставить быстрый, неинвазивный взгляд на наличие HRD.
Умные сканы вместо дополнительных биопсий
Исследователи работали с 307 мышами с трансплантатами человеческих опухолей, которые были либо с HRD, либо с нормальной репарационной активностью. Всем животным выполняли высокоразрешающую компьютерную томографию (КТ) до и после введения либо контрольного препарата, либо CP‑506 — экспериментального средства, активирующегося в гипоксических участках опухолей и образующего кросс‑ссылки в нитях ДНК. Вместо опоры на ограниченный набор вручную разработанных измерений изображения команда использовала современную «фундаментальную модель», обученную на больших наборах человеческих КТ‑данных, чтобы извлечь тысячи тонких паттернов из каждого скана. На этих признаках был обучен простой классификатор для определения, является ли опухоль HRD, а те же извлечённые признаки использовали для прогноза того, насколько много повреждений ДНК и задержки роста вызовет CP‑506.
Насколько хорошо модель по изображениям справилась с задачей
Фундаментальная модель явно превосходила как традиционную радиомику, так и стандартную глубокую сеть, обученную с нуля. На новых тестовых сканах она отличала опухоли с HRD от таковых без HRD с площадью под кривой примерно 0,88 — уровень точности, который держался при разных настройках энергии КТ. Когда оба подхода ИИ сходились во мнении о типе опухоли, показатель ещё возрастал. Оценка HRD по изображениям тесно коррелировала с истинным генетическим статусом в нескольких линиях опухолей предстательной и кишечной железы, хотя одна линия с необычным поведением репарации оставалась трудной для классификации. Важно, что признаки КТ, связанные с HRD, были не просто статистическими артефактами: они также прогнозировали, сколько стойких повреждений ДНК вызвал CP‑506 через 48 часов после лечения, и как долго опухолям требовалось, чтобы восстановиться до четырёхкратного размера в параллельном эксперименте.
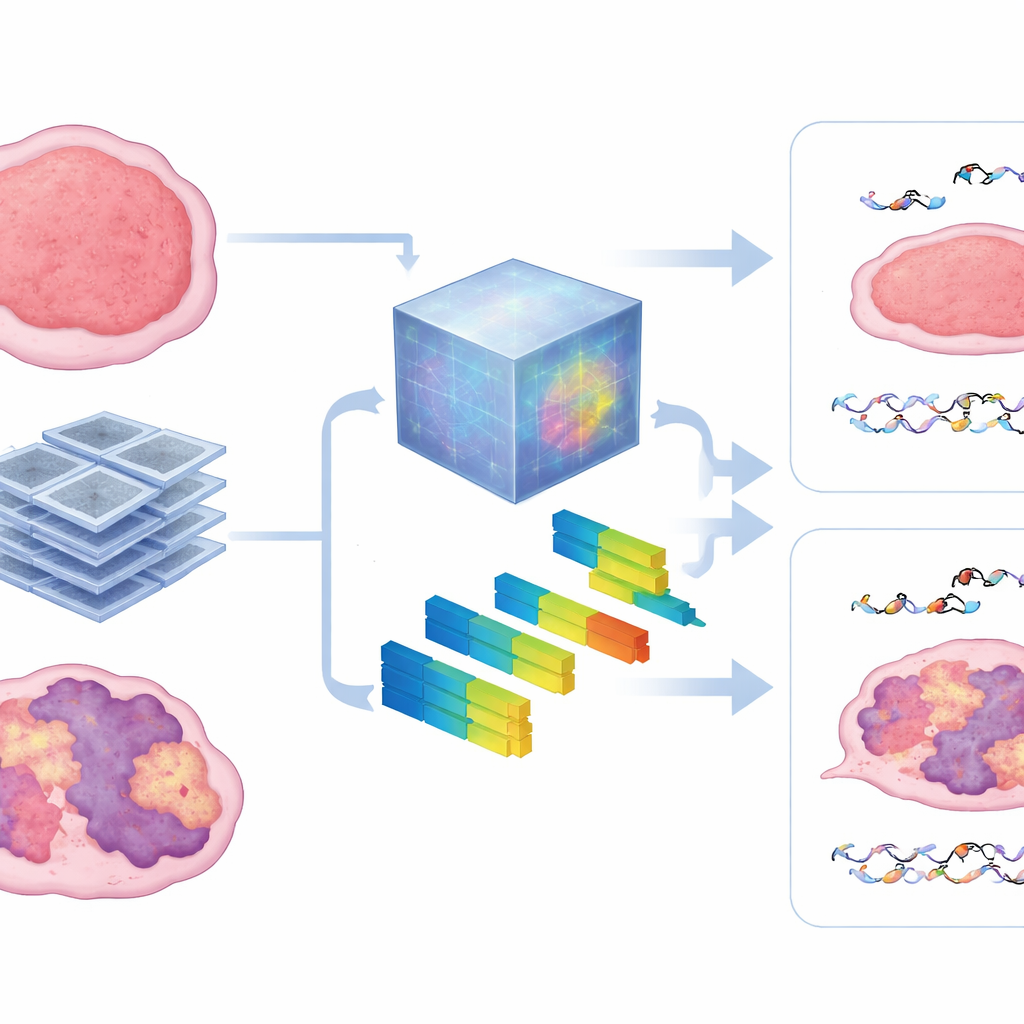
Что сканы показывают внутри опухоли
Чтобы заглянуть внутрь «чёрного ящика», авторы сопоставили паттерны, изученные фундаментальной моделью, со стандартными радиомическими признаками, описывающими текстуру и интенсивность изображения. Они обнаружили, что модель в значительной степени опирается на меры гетерогенности — на то, насколько пятнистой, грубой или нерегулярной выглядит опухоль на КТ. Опухоли с более сильными сигнатурами HRD, как правило, демонстрировали более дисорганизованную текстуру, и эти же признаки помогали предсказывать как микроскопические повреждения ДНК, так и макроскопический контроль опухоли. Подход оставался устойчивым при сокращении объёма обучающих данных, что указывает на то, что такие предварительно обученные модели могут преодолеть главное препятствие в доклинических исследованиях, где сбор больших наборов изображений затруднён.
От экспериментов на мышах к будущей помощи пациентам
Это доклиническое исследование показывает, что один КТ‑скан, интерпретируемый с помощью мощного предварительно обученного ИИ, может фиксировать сигналы о дефекте репарации ДНК и предсказывать, насколько сильно опухоль ответит на препарат, повреждающий ДНК. Для непрофессионала вывод прост: обычные на вид сканы вскоре могут выполнять двойную функцию — локализовать опухоль и показывать её уязвимость — без дополнительных процедур. Прежде чем это станет частью рутинной практики, метод необходимо испытать и валидировать на пациентах. Если эти усилия увенчаются успехом, КТ‑основанные ИИ‑отпечатки HRD могут помочь врачам точнее подбирать людям такие терапии, как CP‑506 и родственные препараты, улучшая исходы и ограждая других от неэффективных и токсичных средств.
Цитирование: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Ключевые слова: дефицит гомологичной рекомбинации, визуализация рака, радиомика, фундаментальные модели, терапия, повреждающая ДНК