Clear Sky Science · ru
Разработка и валидация модели на базе искусственного интеллекта для диагностики доброкачественных, пограничных и злокачественных аднексальных образований
Почему это важно для женского здоровья
Образования яичников и другие аднексальные узлы часто обнаруживаются при тазовом УЗИ, но отличить безвредные образования от ранних признаков рака по‑прежнему непросто, даже для специалистов. В этом исследовании описана новая система на базе искусственного интеллекта (ИИ), названная Clinical‑OMTA, которая анализирует ультразвуковые изображения и помогает врачам распределять такие образования по трём ключевым группам — доброкачественные, пограничные и злокачественные — чтобы женщины получали адекватное лечение и избегали ненужных операций.
Три типа новообразований — три совершенно разных тактики
Не все аднексальные образования одинаковы. Доброкачественные опухоли часто можно наблюдать или удалить простой операцией. Злокачественные новообразования — это угрожающие жизни раковые опухоли, требующие специализированной хирургии и химиотерапии. Пограничные опухоли занимают промежуточное положение: они могут рецидивировать, но часто встречаются у более молодых женщин, желающих сохранить фертильность, поэтому хирурги стремятся удалить только необходимое. К сожалению, на УЗИ эти три категории могут выглядеть очень похоже. Пограничные опухоли особенно склонны имитировать либо безобидную кисту, либо агрессивный рак, что делает принятие решений тяжёлым и для пациенток, и для врачей.
Превращая сложные снимки в более ясные ответы
УЗИ обычно является первым и самым доступным методом исследования при аднексальных образованиях, но интерпретация зернистых и сильно варьирующих изображений требует значительного опыта. Существующие шкалы оценки и калькуляторы риска, такие как широко применяемая модель ADNEX, объединяют конкретные ультразвуковые признаки с простыми клиническими данными — например, возрастом и маркером крови CA125 — но они всё ещё зависят от правильного описания снимков человеком. Недавние работы в области глубинного обучения — ветви ИИ, которая учится распознавать паттерны прямо по пикселям — дают шанс уменьшить эту субъективность, обучив компьютеры распознавать тонкие признаки разных типов опухолей на изображениях.
ИИ‑ассистент, обученный на данных многих больниц
Опираясь на предыдущие разработки, авторы создали Clinical‑OMTA — двухпутевую модель ИИ, которая сначала отделяет доброкачественные образования от недоброкачественных, а затем различает пограничные и злокачественные. Система анализирует изображения в оттенках серого и дополнительно может принимать возраст и значения CA125 как необязательные входные данные. Для обучения и тестирования команда собрала крупный и разнообразный набор данных: 2381 женщина из 23 больниц Китая, обследованных на 38 моделях ультразвуковых аппаратов. Большинство случаев имели гистологическое подтверждение после операции; меньшая группа явно доброкачественных кист была подтверждена не менее чем шестимесячным УЗ‑наблюдением. Данные были разделены на обучающие наборы, внутренние тестовые наборы и два полностью независимых внешних тестовых когорты, включающие как статичные изображения, так и короткие видеозаписи сканирования яичников. 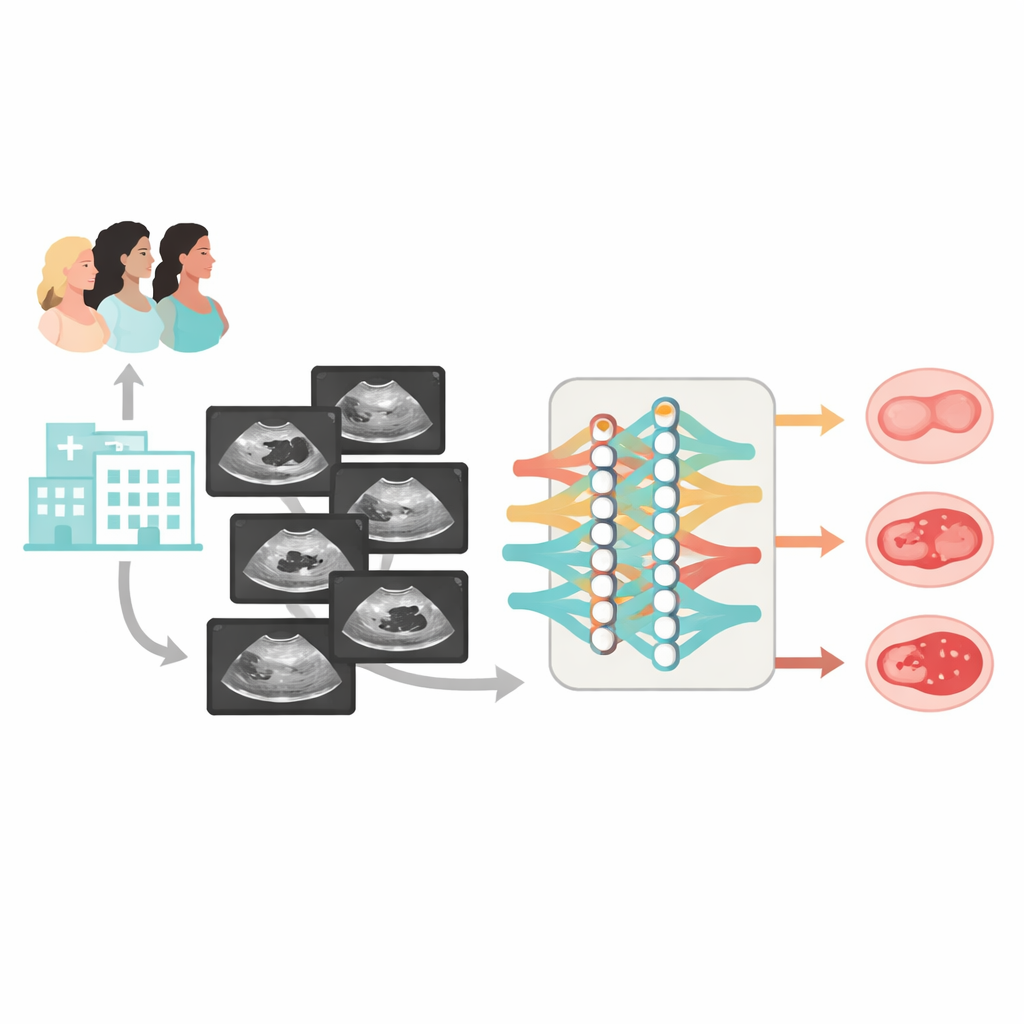
Как ИИ показал себя в реальных условиях
На внешних тестовых изображениях Clinical‑OMTA корректно разделяла доброкачественные, пограничные и злокачественные образования с точностью, сопоставимой как с моделью ADNEX, так и с решением эксперта‑УЗИстa. Его работа была стабильна при использовании аппаратов разных марок, при разных методах сканирования (через брюшную стенку или трансвагинально) и в двух внешних больницах, что говорит о том, что модель не чрезмерно привязана к одному конкретному устройству или центру. Система также успешно работала с видеоклипами, а не только со статичными кадрами. Примечательно, что добавление возраста и CA125 не улучшало её решений по сравнению с использованием одних только УЗ‑изображений, что согласуется с предыдущими исследованиями, показывающими небольшой вклад этого маркера при наличии качественной визуализации. 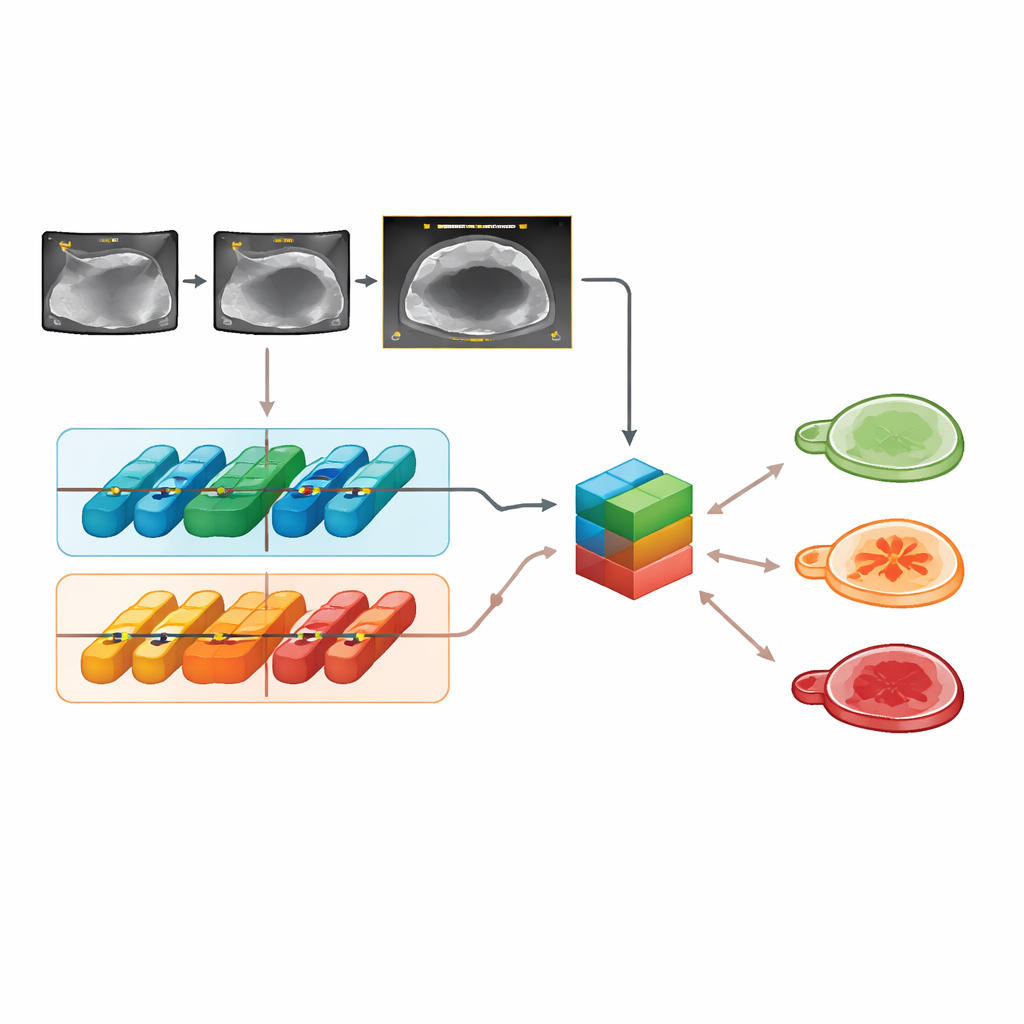
Помощь менее опытным врачам и ограничения
Исследователи затем привлекли 11 рентгенологов — начинающих, среднего уровня и очень опытных — попросив их классифицировать те же случаи сначала без помощи, а затем с выводами ИИ и тепловыми картами, выделяющими области изображения, важные для модели. С помощью Clinical‑OMTA точность начинающих врачей выросла примерно на 18–20 процентных пунктов, а у промежуточных читателей также наблюдалось существенное улучшение, доводя их до уровня, близкого к экспертному. Согласованность между читателями, ранее колебавшаяся от удовлетворительной до умеренной, выросла до очень высокого уровня при использовании инструмента. Вместе с тем авторы отмечают, что такая сильная конвергенция может отражать «автоматизацию смещения» (automation bias), когда клиницисты чрезмерно полагаются на ИИ, особенно в самых неоднозначных пограничных случаях. Поэтому авторы подчёркивают, что тепловые карты служат исследовательским инструментом, а не полноценными объяснениями, и что руководство ИИ должно аккуратно интегрироваться в клиническое обучение и процесс принятия решений.
Что это означает для пациенток
В целом Clinical‑OMTA демонстрирует, что система ИИ, обученная на разнообразных УЗ‑данных, может сопоставимо с экспертами классифицировать аднексальные образования на доброкачественные, пограничные и злокачественные, одновременно существенно повышая уровень навыков и согласованность менее опытных радиологов. Поскольку модель работает на разных аппаратах и в разных центрах, её потенциально можно встроить в сканеры или использовать как автономное программное обеспечение для поддержки врачей в загруженных или слабо обеспеченных клиниках. Авторы предостерегают, что прежде чем внедрять её повсеместно, требуются дополнительные перспективные и международные исследования, особенно в условиях оборудования низшего класса или при операторах без узкой специализации. Тем не менее работа указывает на будущее, в котором больше женщин, независимо от места лечения, смогут получить экспертную интерпретацию УЗ‑сканов яичников и более персонализированное, своевременное лечение.
Цитирование: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Ключевые слова: ультразвук яичников, искусственный интеллект, аднексальные образования, пограничные опухоли яичников, поддержка клинических решений