Clear Sky Science · ru
ACACA модулирует гомеостаз R-петлей, усиливая липидный метаболизм и взаимодействия с микроокружением при ясноклеточном РКК
Почему эта история о раке почки важна
Ясноклеточный рак почки известен тем, что он одновременно распространён и труден для лечения после распространения. Одной из его характерных черт является то, что опухолевые клетки становятся необычайно «жирными», накапливая липиды и перестраивая энергетический обмен. В этом исследовании задают неожиданный вопрос: как изменения генетических сигналов стресса в клетке связаны с этой липидной трансформацией и с тем, как опухоль взаимодействует с окружающей средой? Проследив за одним ферментом — ACACA, — авторы обнаруживают молекулярную связь между геномным стрессом, изменением жирового обмена и образованием благоприятного для роста опухоли микроокружения.
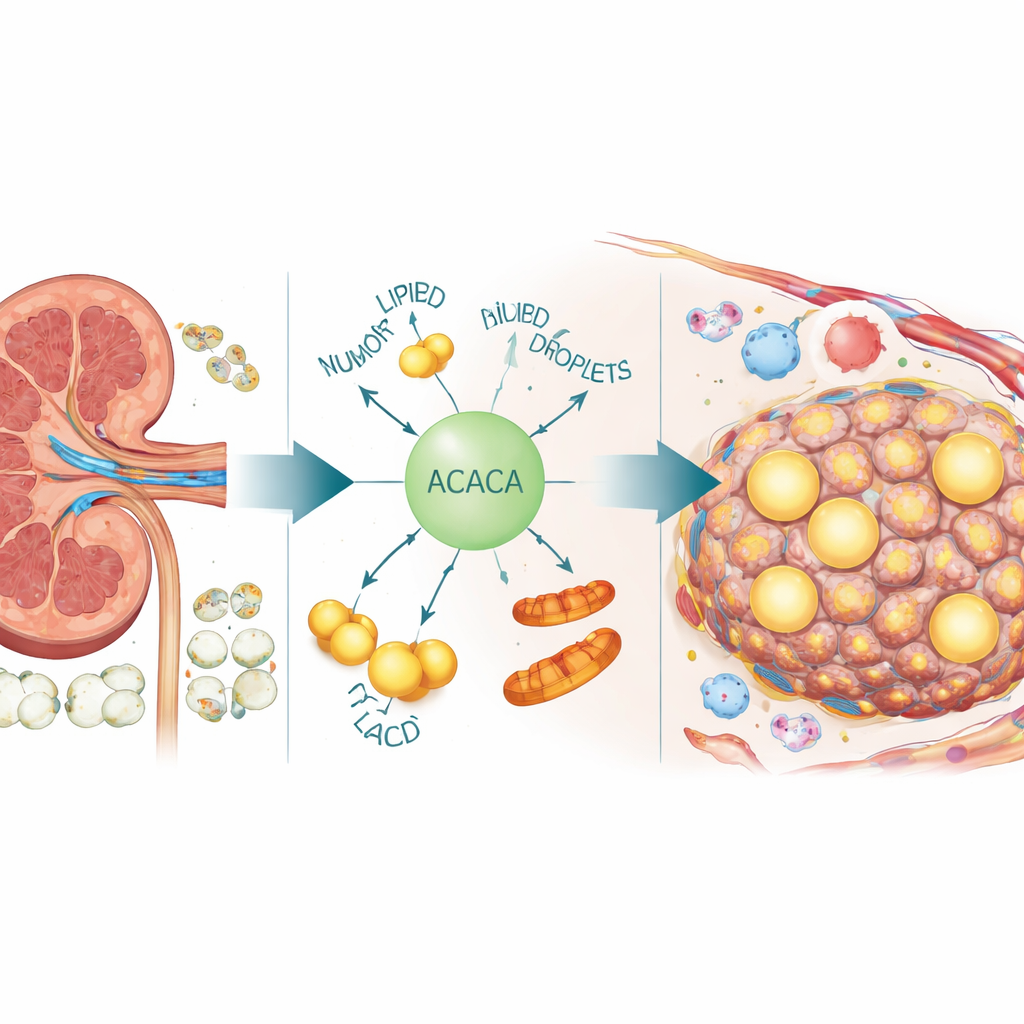
Скрытые трёхцепочечные узлы в ДНК опухоли
Внутри клеток ДНК и РНК во время чтения генов могут временно образовывать трёхцепочечные структуры, называемые R‑петлями. В умеренных количествах эти структуры участвуют в регуляции генома, но в избытке они могут тормозить копирование ДНК и вызывать повреждения. Используя крупные общедоступные наборы данных по опухолям почки и здоровой ткани, команда построила скор, отражающий активность генов, связанных с R‑петлями, у каждого пациента. Они обнаружили, что эта активность явно выше при ясноклеточном раке почки, чем в нормальной ткани, и ещё более возрастает в прогрессирующих и метастатических опухолях. У пациентов с более выраженным R‑подписью выживаемость была в целом хуже, что указывает на связь между нарушением контроля этих структур и более агрессивным течением болезни.
Один фермент выделяется из общей массы
Из более чем тысячи генов, ассоциированных с R‑петлями, исследователи сузили список до 44, которые были нарушены в опухолях и связаны с исходами пациентов. Затем они использовали несколько линейных моделей машинного обучения, чтобы выяснить, какая комбинация лучше всего предсказывает выживаемость. Во всех методах и в независимых когортах одно имя постоянно оказывалось вверху списка: ACACA — ключевой фермент, запускающий первый необратимый шаг синтеза новых жирных кислот. Высокий уровень ACACA помогал выделять пациентов с более высоким риском рецидива или смерти. Комбинируя экспрессию ACACA со стандартными клиническими данными — размером опухоли, стадией распространения и микроскопическим грейдом — авторы построили практический скоринговый инструмент, который хорошо соответствовал реальным показателям выживаемости пациентов на протяжении многих лет.
Липидный центр внутри злокачественных клеток
Чтобы посмотреть, где именно экспрессируется ACACA в опухоли, авторы обратились к одно‑клеточной и пространственной транскриптомике — методам, позволяющим считывать активность генов по отдельным клеткам и сопоставлять её с тканевыми срезами. Эти анализы показали, что ACACA выражён неравномерно: он сосредоточен в злокачественных клетках, где совпадает с программами активного деления и признаками повреждения и ремонта ДНК. Клетки с высоким уровнем ACACA выступали в роли коммуникационных узлов, шлифуя множество сигналов с ближайшими иммунными и эндотелиальными клетками. Многие из этих сигналов проходят через липид‑связываемые пути с участием молекул ANGPTL, известных координировать обращение с жирами, воспаление и сосудистый рост. В тканевых срезах области, богатые ACACA, совпадали с плотными участками опухоли, а не с прилежащей нормальной тканью.
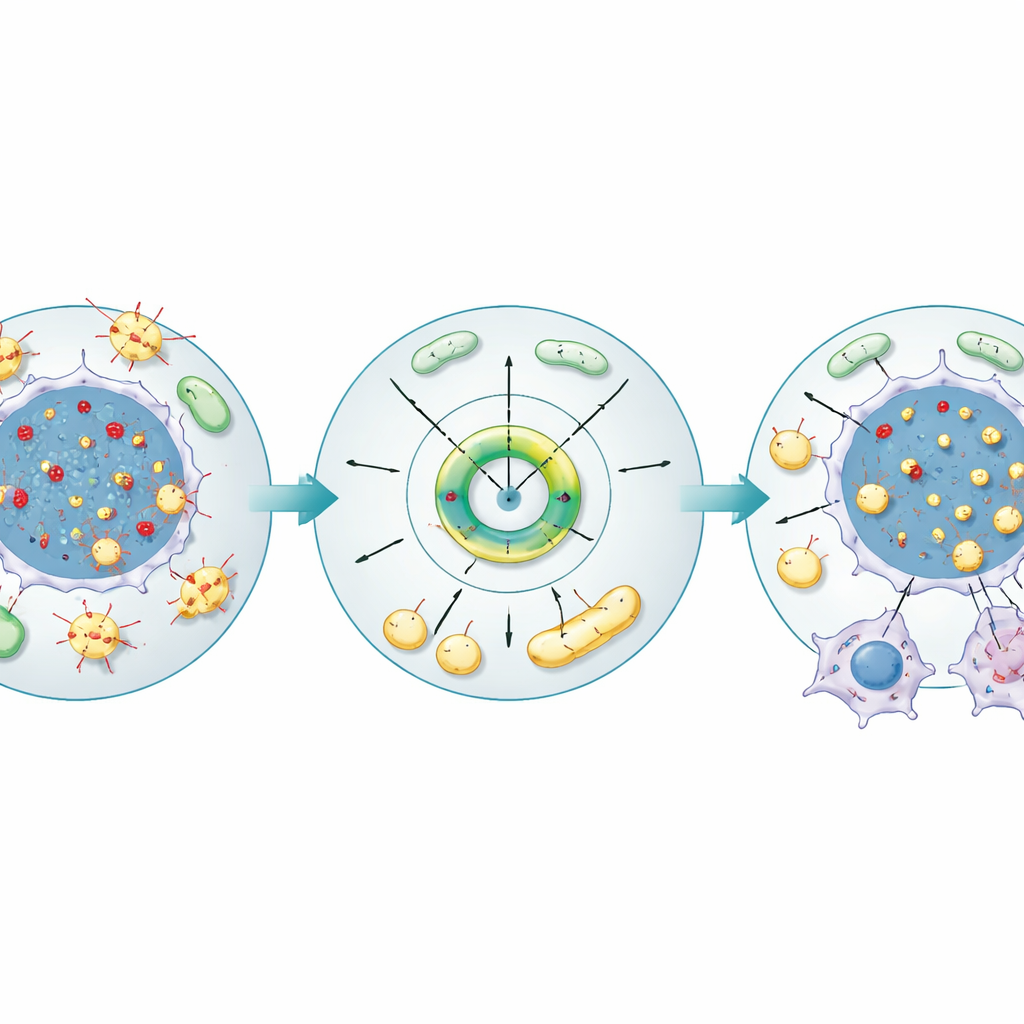
От генетического стресса к топливному снабжению и росту опухоли
Далее авторы протестировали роль ACACA непосредственно в клеточных линиях рака почки и в опухолях у мышей. Понижение активности ACACA замедляло рост клеток, снижало их подвижность и увеличивало апоптоз, в то время как повышение ACACA давало противоположные эффекты. Микроскопия показала, что при низком ACACA накапливаются R‑петли и усиливаются признаки повреждения ДНК, тогда как при высоком ACACA эти структуры уменьшались. Одновременно ACACA увеличивал количество липидных капель в клетках, повышал уровни жирных кислот и триглицеридов и улучшал здоровье митохондрий — судили по более высокому мембранному потенциалу, увеличенному числу митохондрий и сниженным уровням реактивных кислородных молекул. У мышей блокирование ACACA в имплантированных клетках рака почки замедляло рост опухолей, усиливало сигналы повреждения ДНК, уменьшало запасы липидов и ослабляло функцию митохондрий, связывая фермент как с устойчивостью генома, так и с энергетическим бюджетом опухоли.
Что это значит для будущего лечения
В совокупности исследование изображает ACACA как молекулярный переключатель, который помогает ясноклеточному раку почки выживать при генетическом стрессе, перестраивая липидный метаболизм и усиливая взаимодействия с микроокружением. Повышенная активность R‑петель отмечает более опасные опухоли, а ACACA выступает центральным звеном, связывающим этот стресс с липидонасыщенными, энергоэффективными раковыми клетками, которые легче растут и метастазируют. Поскольку ACACA — это фермент, потенциально доступный для лекарственного вмешательства, полученные данные предлагают новые подходы как к прогнозированию пациентов с высоким риском, так и к разработке терапий, которые одновременно нарушают стратегии защиты генома опухоли и её метаболические опоры.
Цитирование: Zhang, D., Chen, X., He, X. et al. ACACA modulates R-loop homeostasis to enhance lipid metabolism and microenvironmental interactions in ccRCC. npj Precis. Onc. 10, 102 (2026). https://doi.org/10.1038/s41698-026-01319-y
Ключевые слова: ясноклеточная почечноклеточная карцинома, R‑петли, ACACA, липидный метаболизм, туморное микроокружение