Clear Sky Science · ru
Натуральный полисахарид риклин выступает иммунным адъювантом и усиливает эффективность химиотерапии при НМРЛ
Почему это важно для онкологических пациентов
Химиотерапия может быть палкой о двух концах: с одной стороны она атакует опухоли, с другой — ослабляет собственные защитные силы организма, делая пациентов уязвимыми к инфекциям и утомляемости. В этом исследовании изучают натуральное сахароснóвное соединение риклин, вырабатываемое «дружественными» бактериями и принимаемое перорально. У мышей с распространённым типом рака лёгкого риклин помог восстановить иммунную и кроветворную системы, повреждённые химиотерапией, одновременно повышая эффективность противоракового препарата. Работа намекает на возможность, что простой пероральный добавка в будущем может сделать жёсткие терапии и безопаснее, и эффективнее.
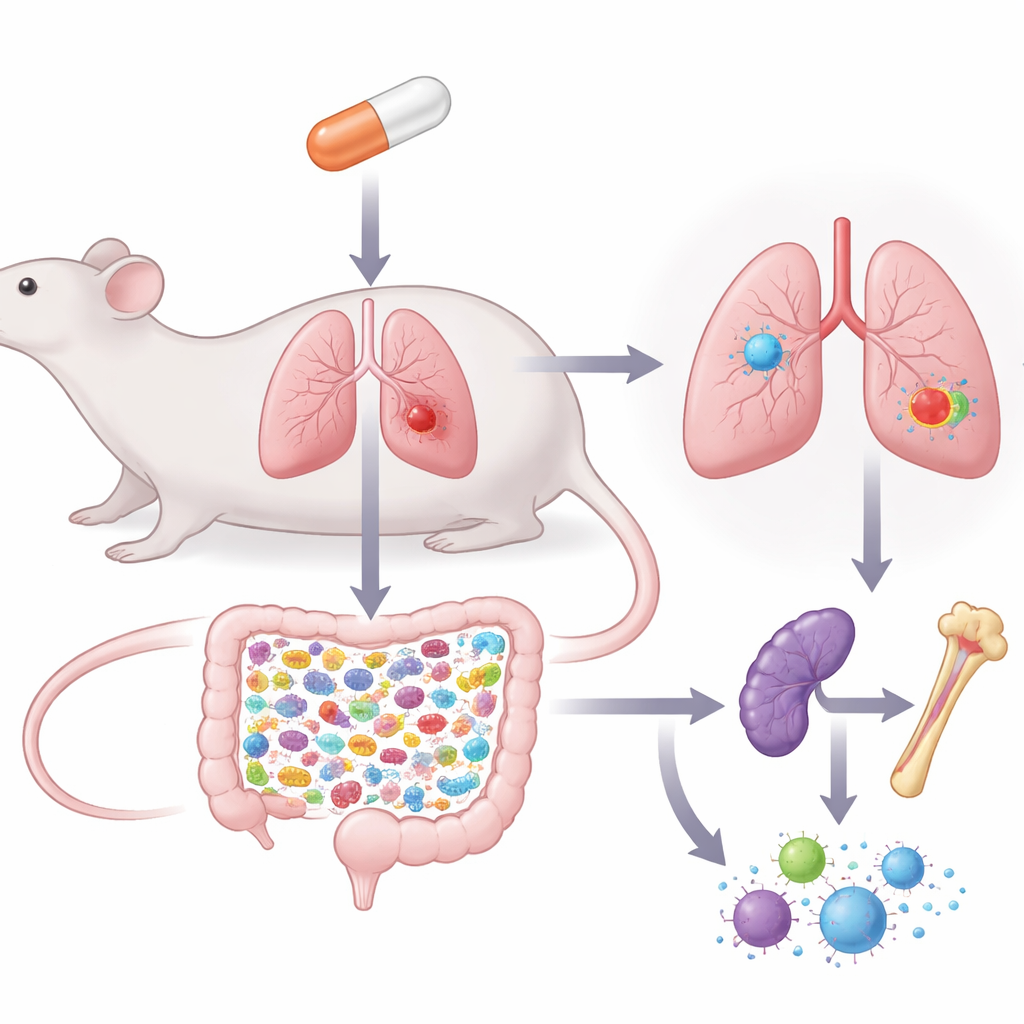
Помощник для стандартного препарата при раке лёгкого
Исследователи сосредоточились на немелкоклеточном раке лёгкого — самом распространённом и смертоносном виде рака лёгкого. Стандартный препарат при этом заболевании, гемцитабин, может уменьшать опухоли, но часто подавляет иммунную систему и костный мозг, где образуются новые кровяные клетки. Команда поставила вопрос: может ли риклин, длинноцепочечный сахар (полисахарид), ранее показавший безопасность и нетоксичность, служить «иммунным бустером», чтобы противостоять этим побочным эффектам. Применяя риклин перорально у мышей, получавших гемцитабин, они проверяли, сможет ли сочетание снизить объём опухоли, избегая при этом типичного падения числа лейкоцитов, тромбоцитов и нарушений в таких ключевых иммунных органах, как селезёнка и тимус.
Как реагируют микробы кишечника и кровяные клетки
Путь риклина начинается в кишечнике. У здоровых мышей, которым давали риклин перорально, состав кишечной микробиоты сместился целенаправленно: увеличилась доля групп, связанных с благоприятным влиянием на иммунитет, а потенциально вредные бактерии сократились. Одновременно изменились химические «отпечатки» в кишечнике. Увеличились уровни нескольких короткоцепочечных жирных кислот и других метаболитов, известных тем, что они влияют на иммунные клетки по всему телу. Эти изменения указывают, что риклин перестраивает как типы микроорганизмов в кишечнике, так и полезные сигнальные молекулы, которые они вырабатывают, усиливая коммуникацию между кишечником, иммунными органами и костным мозгом.
Пробуждение защитников организма
Далее команда изучила непосредственно передовые иммунные клетки. В культурах клеток риклин делал макрофаги — клеток-«санитаров», патрулирующих ткани — крупнее, более активными и лучше способными фагоцитировать частицы. Эти клетки выделяли больше сигнальных белков, которые мобилизуют более широкие иммунные ответы. У живых мышей риклин включал генетические программы в селезёнке и костном мозге, связанные с активацией иммунитета и продукцией новых кровяных клеток. Были задействованы ключевые регуляторные пути, координирующие воспалительные сигналы и рост вновь образующихся иммунных и кроветворных клеток; блокирование этих путей препаратами ослабляло эффект риклина. В совокупности результаты показывают, что риклин делает не просто небольшой толчок иммунитету, а фактически перезапускает механизмы, формирующие и поддерживающие его.
Защита от повреждений химиотерапией
Когда мышей лечили только гемцитабином, они теряли вес, их селезёнки и тимусы уменьшались, а показатели крови падали — классические признаки сильной токсичности лечения. Добавление риклина изменило эту картину. Мыши, получавшие и гемцитабин, и риклин, сохраняли более стабильный вес и более нормальные размеры иммунных органов, а их лейкоциты, лимфоциты, нейтрофилы и тромбоциты восстанавливались ближе к норме. Внутри костного мозга риклин поддерживал выживание и деление ранних кроветворных клеток, уменьшал гибель клеток и сохранял тонкую структуру ткани. Одновременно риклин восстанавливал число и активность иммунных клеток в селезёнке, включая ключевые популяции Т‑клеток, центральные для координации атак на опухоль.
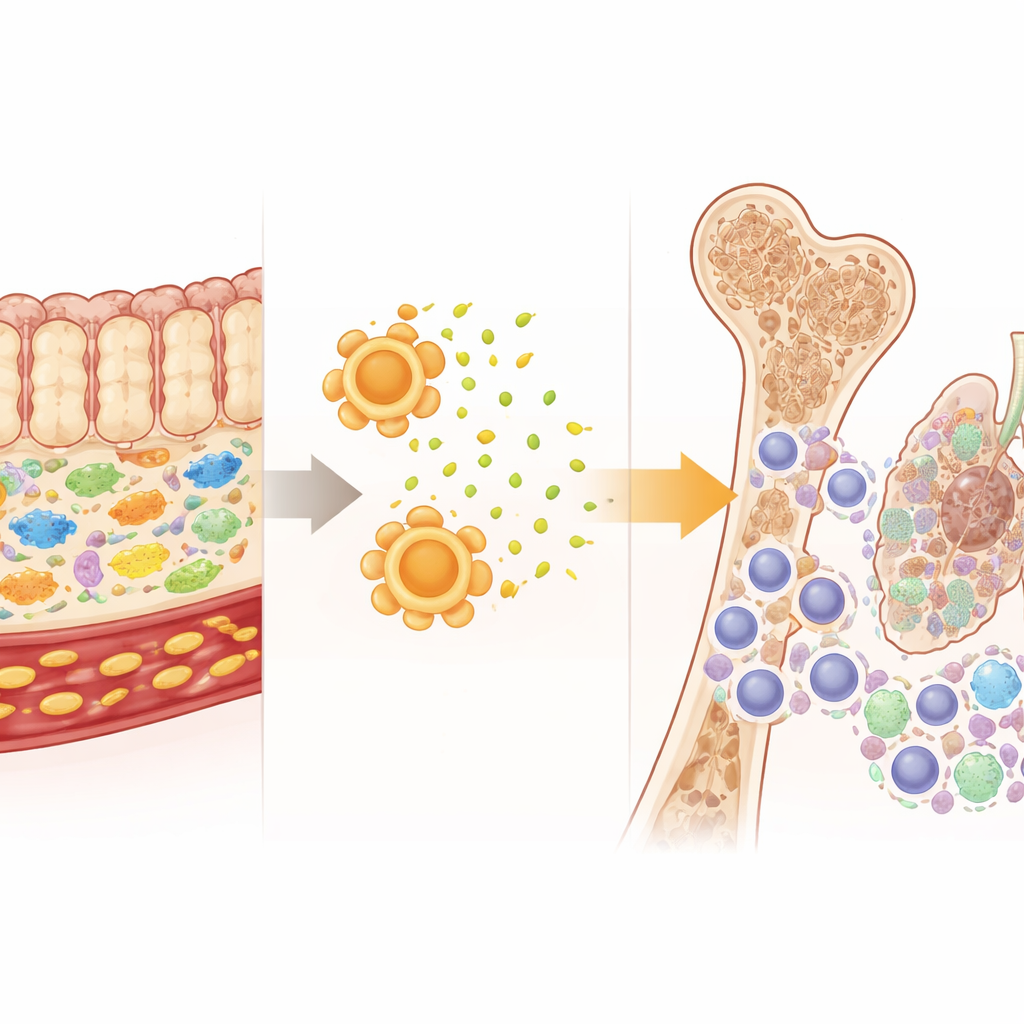
Усиление противоопухолевого действия химиотерапии
Самое заметное: в модели рака лёгкого у мышей риклин сделал гемцитабин более эффективным против опухолей. Комбинированная терапия сокращала опухоли значительно сильнее, чем только гемцитабин — в некоторых случаях уменьшив общую массу опухоли почти полностью — при этом продолжая защищать иммунную систему от тяжёлого подавления. У мышей с опухолями, получавших риклин, наблюдались более сильные Т‑клеточные ответы в селезёнке и повышенные уровни провоспалительных и проиммунных сигнальных молекул в крови, что указывает на привлечение собственных защитных сил организма для помощи препарату в уничтожении раковых клеток. Этот двойной эффект — более жёсткий контроль опухоли при меньшем системном вреде — редкость среди доступных сейчас добавок к лечению.
Что это может значить для будущей терапии
Для непрофессионального читателя основная мысль такова: риклин действует как умный щит и усилитель для химиотерапии — он помогает микробам кишечника и иммунным органам работать сообща, чтобы организм лучше переносил и даже усиливал эффект стандартного противоракового препарата. Поскольку эти результаты получены на мышах и проверялся только гемцитабин, необходимы дополнительные исследования: проверить риклин с другими лекарствами, детально изучить безопасность и определить подходящие дозы. Если эти шаги окажутся успешными, риклин или подобные соединения могут войти в состав комбинированных терапий, призванных сделать лечение рака не только более мощным, но и более щадящим для организма.
Цитирование: Miao, Y., Liu, X., Tao, J. et al. Natural polysaccharide riclin acts as an immune adjuvant to enhance chemotherapy efficacy in NSCLC. npj Precis. Onc. 10, 108 (2026). https://doi.org/10.1038/s41698-026-01318-z
Ключевые слова: немелкоклеточный рак лёгкого, побочные эффекты химиотерапии, микробиом кишечника, иммунный адъювант, полисахариды