Clear Sky Science · ru
Обобщение автоматической сегментации опухолей на гистопатологических изображениях всего слайда для нескольких типов рака
Почему это важно для онкологической помощи
Диагностика рака по‑прежнему опирается на экспертов, внимательно рассматривающих стеклянные препараты окрашенных тканей под микроскопом — трудоёмкую процедуру, усложняемую ростом числа случаев и нехваткой патологов. В этом исследовании поставлен простой, но важный вопрос: может ли одна система искусственного интеллекта надёжно находить раковые участки на цифровых микроскопических изображениях для множества типов опухолей, вместо того чтобы создавать отдельный инструмент для каждого вида рака? Если да, это могло бы снизить нагрузку, ускорить постановку диагноза и расширить возможности продвинутого анализа даже для редких форм рака, где данных мало.
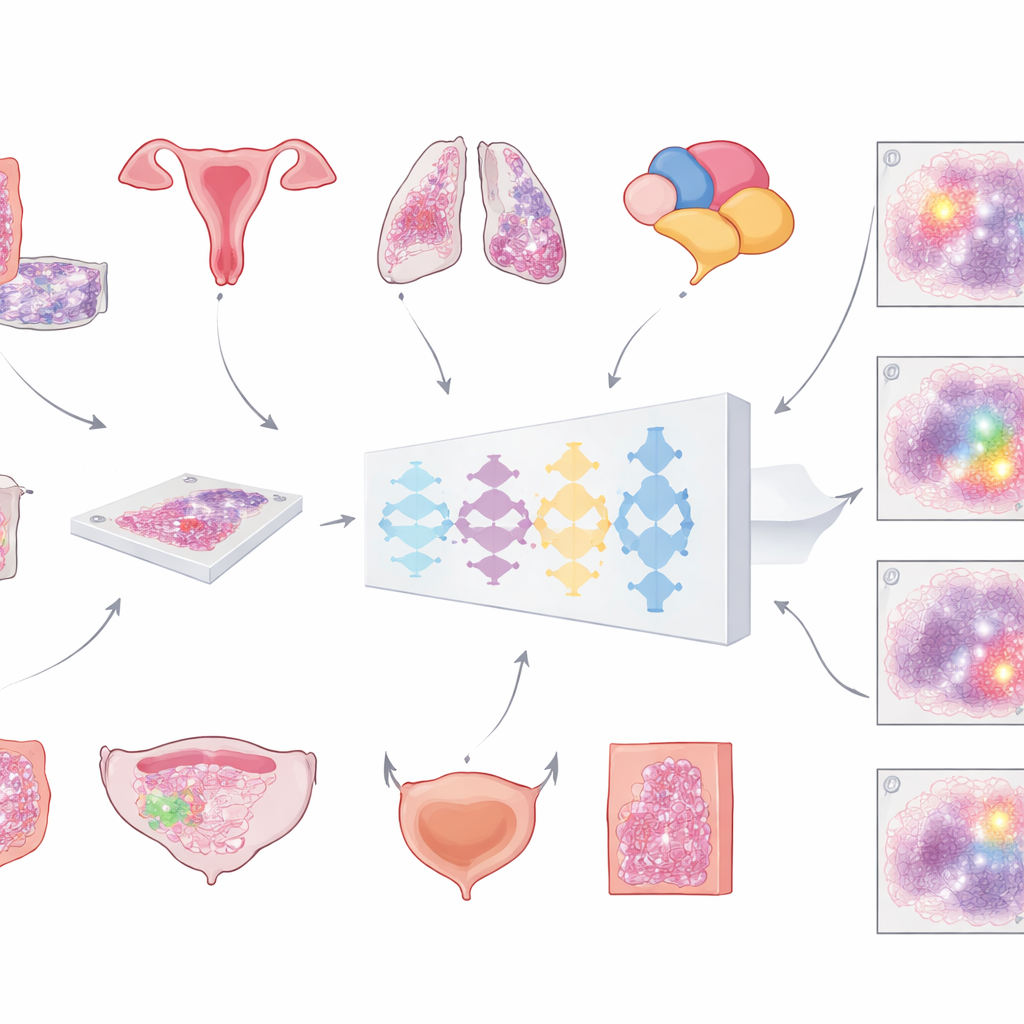
От стеклянных препаратов к цифровым помощникам
Современные больницы всё чаще сканируют микроскопические слайды, создавая гигантские подробные «изображения всего слайда» опухолей. Первый ключевой шаг для любой компьютерной аналитики — отделить раковую ткань от всего прочего — нормальных клеток, жировой ткани, пустого стекла и артефактов. До сих пор большинство автоматизированных инструментов обучались на одном типе рака, что ограничивало их применение. Авторы работы поставили цель создать одну универсальную модель, способную обнаруживать области опухоли в слайдах, окрашенных стандартными гематоксилином и эозином, для нескольких распространённых типов рака. Их идея — универсальный инструмент, который можно интегрировать в разные диагностические рабочие процессы без повторной разработки для каждого случая.
Обучение одной модели для распознавания многих опухолей
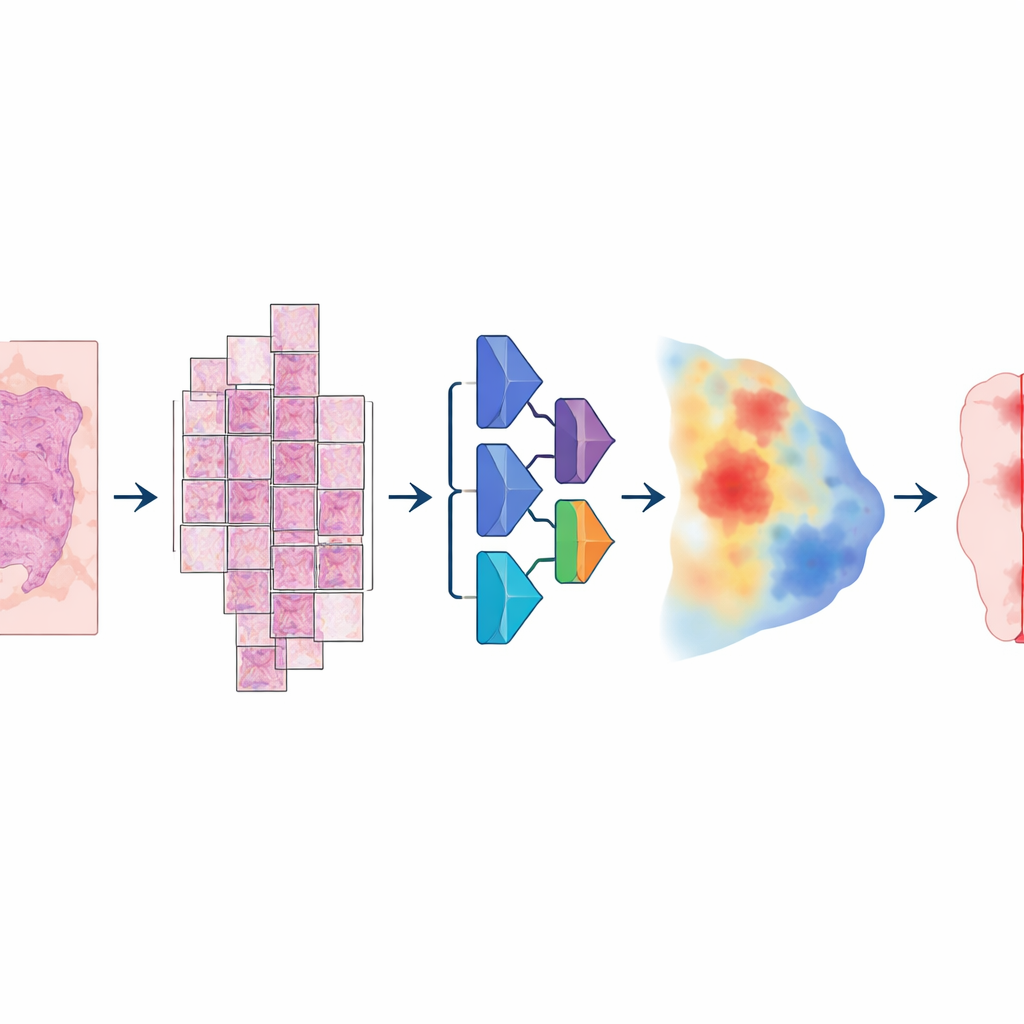
Для создания модели исследователи собрали необычно большую и разнообразную коллекцию цифровых слайдов: более 20 000 изображений всего слайда от более чем 4 000 пациентов с колоректальным, эндометриальным, лёгочным и предстательной железы раком. Все образцы были стандартными формалиново‑фиксированными, парафинированными тканями и отсканированы на двух разных высокоразрешающих сканерах. Патолог аккуратно обвел области опухоли на каждом слайде, предоставив «истинные» метки, на которых училась модель. Модель работала по многошаговому конвейеру: каждое огромное изображение разбивалось на большие перекрывающиеся плитки, проходило через глубокую нейронную сеть, оценивающую для каждого пикселя вероятность опухоли, после чего результаты собирались в гладкую карту и в конце преобразовывались в чистую маску «опухоль против не‑опухоли».
Проверка системы в действии
Важный момент — команда не остановилась на показателях обучения. Они протестировали ту же модель на более чем 3 000 дополнительных пациентов по шести типам рака — включая рак молочной железы и мочевого пузыря, которые не использовались при обучении — и на слайдах из нескольких больниц и со сканеров разных производителей. Точность оценивали главным образом стандартной мерой перекрытия (коэффициент Дайса), который достигает 100%, когда контур опухоли, предложенный компьютером, полностью совпадает с контуром патолога. Для больших, цельных образцов опухоли при колоректальном, эндометриальном, лёгочном, предстательной и грудном раке среднее перекрытие превышало 80% и часто достигало 90%+ . В крупных внешних наборах из The Cancer Genome Atlas, собранных в разных лабораториях и на разных сканерах по всему миру, результат также оставался выше 80%, что указывает на хорошую обобщаемость модели вне родной институции.
Где модель испытывает трудности и как она сравнивается
Главная слабость проявилась при ранних стадиях рака мочевого пузыря, когда материал берётся процедурой, дающей очень мелкие и фрагментированные кусочки ткани. В таких случаях модель часто не помечала вообще никакой опухоли, особенно когда площадь поражения была очень мала. Тем не менее, когда модель обнаруживала опухоль, перекрытие с контурами патолога было высоким, а простая корректировка порогов на этапе постобработки улучшала результаты — что намекает на то, что базовая сеть распознавала паттерн, но постобработка была чрезмерно строгой. Исследователи также создали четыре «специализированные» модели, каждая обученная на одном типе рака, и обнаружили, что ни одна из них существенно не превосходит общую модель в своей области. При этом специализированные системы в значительной степени терпели неудачу при применении к другим типам рака, тогда как общая модель оставалась стабильной. По сравнению с популярным более общим инструментом для медицинской сегментации, требующим подсказок от пользователя, новая модель обычно показывала равное или лучшее качество при полностью автоматической работе.
Что это значит для пациентов и врачей
Для непрофессионалов главное — одна хорошо продуманная система ИИ может надёжно выделять раковую ткань на цифровых слайдах для нескольких основных типов опухолей, без необходимости создавать отдельные версии для каждого заболевания или сканера. Она не заменяет патолога, но может предварительно маркировать вероятные области опухоли, поддерживать согласованные измерения и освобождать специалистов для работы с наиболее сложными случаями. Текущая версия всё ещё пропускает очень маленькие или ранние опухоли — особенно фрагментированные образцы мочевого пузыря и, вероятно, другие биопсийоподобные ткани — поэтому пока не подходит для обнаружения самых слабых следов рака. Тем не менее исследование показывает, что широкая «пан‑раковая» сегментация опухолей выполнима в реальных условиях и может послужить надёжным первым шагом для будущих автоматизированных инструментов, оценивающих степень злокачественности, предсказывающих ответ на лечение или направляющих прецизионную терапию.
Цитирование: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
Ключевые слова: цифровая патология, глубокое обучение, сегментация опухоли, сканирование всего слайда, пан-раковая модель