Clear Sky Science · ru
Масштабный одно-клеточный анализ и in silico‑воздействия выявляют динамическую эволюцию ГЦК: от инициации до терапевтического таргетирования
Почему внутренний мир рака печени важен
Гепатоцеллюлярная карцинома, самая распространённая форма рака печени, известна своей высокой устойчивостью к лечению. Многие пациенты плохо отвечают на доступные препараты, а опухоли часто рецидивируют или дают метастазы. Одна из основных причин — каждая опухоль представляет собой хаотичную смесь различных клеток, которые со временем эволюционируют и постоянно взаимодействуют с окружением. В этом исследовании используются мощные одно‑клеточные и пространственные методы считывания генетической активности, чтобы проследить эту эволюцию по клетке: от раннего роста опухоли до продвинутой, лекарственно‑устойчивой болезни, и выявить уязвимые места, которыми могли бы воспользоваться новые терапии.
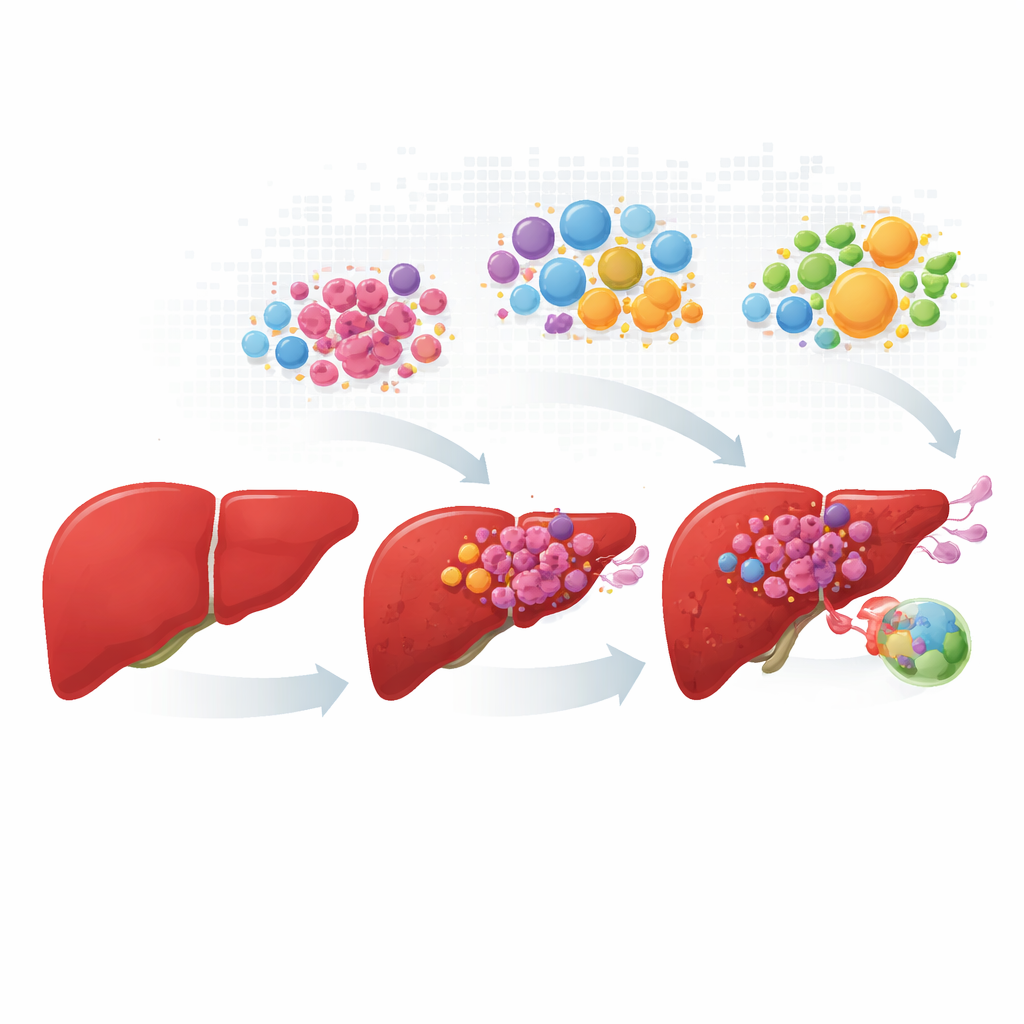
От ранних изменений к распространению: слежение за раковыми клетками
Исследователи собрали и синхронизировали данные более чем сотни пациентов, охватив нормальную печень, первичные опухоли, роста в кровеносных сосудах и метастазы в лимфоузлах. Вместо того чтобы рассматривать каждую опухоль как однородную массу, они профилировали сотни тысяч отдельных клеток и затем сопоставили, где эти клетки располагаются в тканевых срезах. Раковые клетки печени разделились на четыре повторяющиеся «персоналии». Одна группа сохраняла множество нормальных печёночных функций и метаболических задач; остальные три демонстрировали стресс‑индуцированный рост, высокую активность сигнального пути MYC или инвазивное поведение, связанное с воспалением. Доля этих четырёх состояний менялась по мере прогрессирования болезни: быстро растущие и инвазивные клетки доминировали в поражениях сосудов и лимфоузлов.
Четыре «персоналии» опухоли и разные прогнозы
Эти четыре состояния раковых клеток были не просто академической классификацией — они коррелировали с исходом у пациентов. Опухоли, обогащённые печёночным, метаболически активным состоянием, связывались с лучшей выживаемостью, тогда как опухоли, доминируемые тремя агрессивными состояниями, как правило, имели худший прогноз. Однако даже «благоприятное» состояние имело свою особенность: оно было сильно представлено у пациентов, не получивших пользы от препарата сорофениб, вероятно потому, что эти клетки сохраняют детоксикационные механизмы, которые могут инактивировать лекарства. Воспроизводя пути перехода клеток вдоль их развития, команда показала, что инвазивные воспалительные клетки могут ветвиться в сторону более дифференцированных или более пролиферирующих состояний, что указывает на способность опухолевых клеток менять идентичность и потенциально уходить от терапии, направленной на одно состояние.
Поддерживающий состав: иммунные и стромальные соучастники
Раковые клетки не действуют в одиночку. В исследовании выявили специализированные иммунные клетки и клетки‑опоры, которые либо борются с опухолью, либо незаметно ей помогают. Среди макрофагов — «мусорщиков» и стражей ткани — одни типы продуцировали провоспалительные сигналы, способствующие антитуморному иммунитету, тогда как другие были метаболически перенастроены, подавляли полезные сигналы и способствовали ангиогенезу и инвазии. Эти «вредоносные» макрофаги расширялись в продвинутых образцах. Аналогично, определённые эндотелиальные клетки, выстилающие сосуды, и фибробласты, формирующие соединительную ткань, образовали подмножества, связанные с плохим прогнозом. В продвинутой болезни один эндотелиальный подтип и два типа фибробластов формировали тесно связанные узлы, перестраивавшие внеклеточный матрикс, стимулировавшие формирование новых сосудов и коррелировавшие с наиболее агрессивными состояниями раковых клеток.
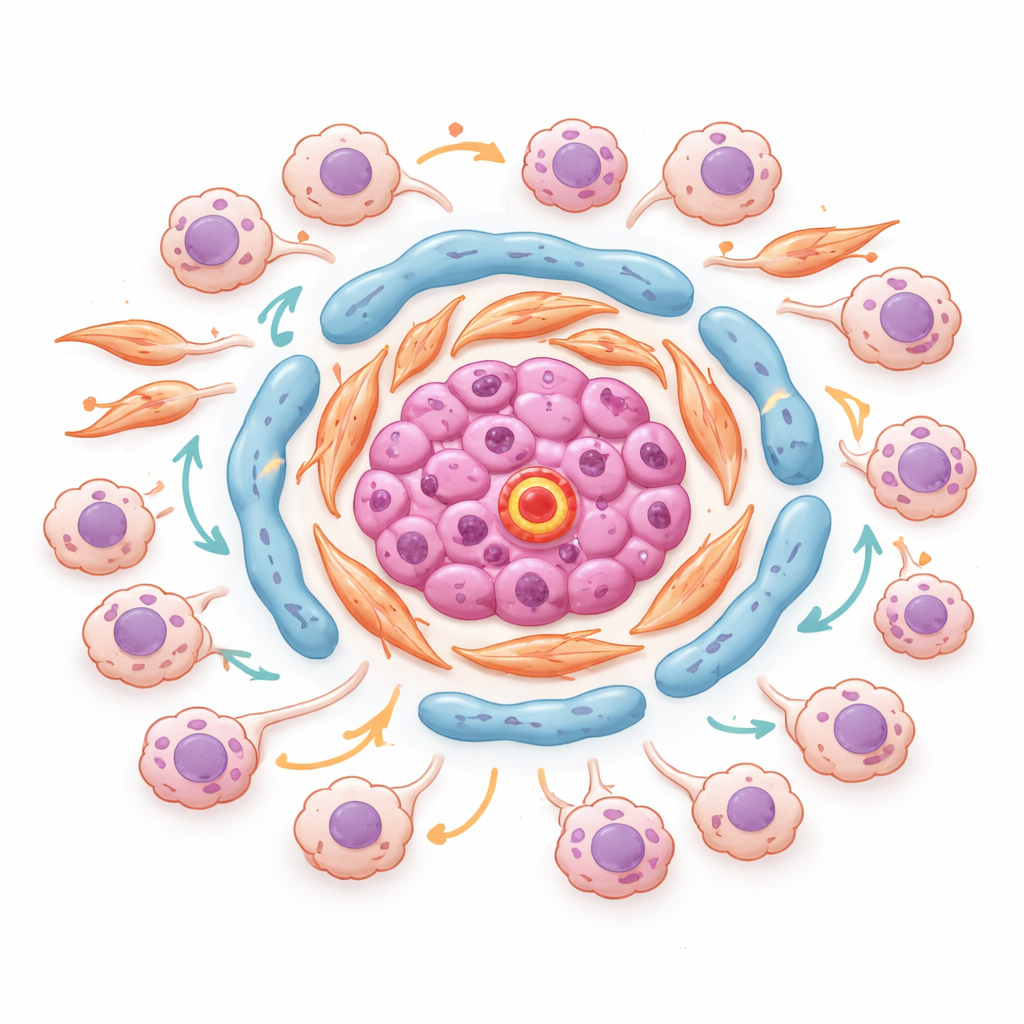
Опасные кварталы внутри опухолей
С помощью пространственной транскриптомики, которая измеряет активность генов, не теряя карту расположения каждого участка в ткани, авторы идентифицировали организованные «районы» внутри опухолей. В одной характерной опухоли эндотелиальные клетки, богатые молекулой ESM1, сгруппировались с липид‑оголодавшими и продуцирующими матрикс фибробластами в ядре стромальных островков. Вокруг этих ядер накапливались стресс‑индуцированные и инвазивные раковые клетки в областях с сильной активностью TGF‑beta и признаками низкого кислорода. Ключевые факторы транскрипции, контролирующие ответ клеток на стресс и воспаление, были общими для этих раковых состояний и наиболее активны именно там, где опухолевые клетки соприкасались со стромальными узлами. Это позволяет предположить, что специфические микрониши на границе опухоль–строма активно поощряют переход клеток в новые состояния, делая их более агрессивными и устойчивыми к терапии.
Поиск общей уязвимости для новых лечений
Для перехода от описания к вмешательству команда использовала модель машинного обучения, обученную на миллионах клеток, чтобы симулировать «виртуальные нокауты» генов и предсказать, какие изменения могут вернуть вредные клетки к более здоровым состояниям. Сравнивая макрофаги, эндотелиальные клетки и раковые клетки, они обнаружили небольшой набор генов, удаление которых способствовало нормализации всех трёх типов. Среди них выделялся HSP90B1: на него сильно зависят клеточные линии рака, он сверхэкспрессирован в опухолях печени, особенно в тех, которые резистентны к таргетной терапии и иммунотерапии, а высокий уровень его экспрессии предсказывает худшую выживаемость. HSP90B1 кодирует шаперон, участвующий в обработке стресса в фабрике свёртывания белков клетки, который поддерживает многие поверхностные рецепторы и сигнальные пути. Поскольку селективные ингибиторы этого шаперона уже существуют и могут также перестроить иммунную среду, исследование предлагает HSP90B1 как перспективную мишень для преодоления резистентности, особенно в сочетании с нынешними методами лечения рака печени.
Что это значит для пациентов и терапии
В совокупности работа показывает, что рак печени — это не единое заболевание, а динамичная экосистема клеточных состояний и ниш, которые меняются по мере роста и распространения опухоли. Связав конкретные «персоналии» раковых клеток, клетки‑помощники и пространственные районы с исходом пациентов и ответом на лекарства, исследование предлагает дорожную карту для более точной терапии: подбирать лечение под доминирующие клеточные состояния, разрушать стромальные узлы, которые взращивают агрессивность, и таргетировать общие зависимости, такие как HSP90B1, от которых зависят многие клетки опухоли и микроокружения. Хотя необходимы дальнейшие лабораторные и клинические испытания, созданный учёными атлас предоставляет подробный план по превращению внутренней сложности опухоли из препятствия в возможность для более умных и долговечных методов лечения рака печени.
Цитирование: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Ключевые слова: гепатоцеллюлярная карцинома, одно-клеточный анализ, опухолевое микроокружение, пространственная транскриптомика, HSP90B1