Clear Sky Science · ru
Клонотипное разнообразие и специализация Т-клеточных рецепторов при раках органов пищеварения
Почему это исследование важно для пациентов с раком
Иммунотерапия трансформировала лечение многих пациентов с раком, но она действует не одинаково хорошо для всех. В этом исследовании внимательно изучаются «штрихкоды» иммунных клеток — Т-клеточных рецепторов — внутри опухолей органов пищеварения, включая колоректальный и желудочный рак. Масштабное чтение этих штрихкодов показывает, как иммунная система узнаёт опухоли, чем это распознавание отличается между типами рака и как оно меняется при метастазировании колоректального рака. Эти выводы могут помочь врачам точнее прогнозировать исход и разрабатывать более точные, персонализированные иммунотерапевтические подходы.
Отпечаток иммунной системы внутри опухолей
Т-клетки — это направленные защитники организма, каждая из которых несёт уникальный рецептор, позволяющий распознавать специфические аномальные клетки, в том числе раковые. Авторы секвенировали Т-клеточные рецепторы в 415 образцах опухолей от 145 пациентов с колоректальным, желудочным и печёночным раком и сопоставили эти данные с детальной клинической информацией. Они анализировали несколько цепей рецепторов, определяющих две ключевые семьи Т-клеток: традиционные αβ-Т-клетки, которые управляют большинством адаптивных иммунных ответов, и γδ-Т-клетки, действующие скорее как быстро реагирующие дозорные. Выяснилось, что αβ-Т-клетки склонны формировать крупные, высокоразнообразные клоны, тогда как γδ-Т-клетки образуют более мелкие, специализированные популяции. У пациентов с более продвинутой стадией заболевания, инвазией кровеносных сосудов или отдалёнными метастазами наблюдались более сложные паттерны Т-клеточных рецепторов, что указывает на то, что прогрессирование опухоли переводит иммунную систему в более широкую и сложную борьбу.
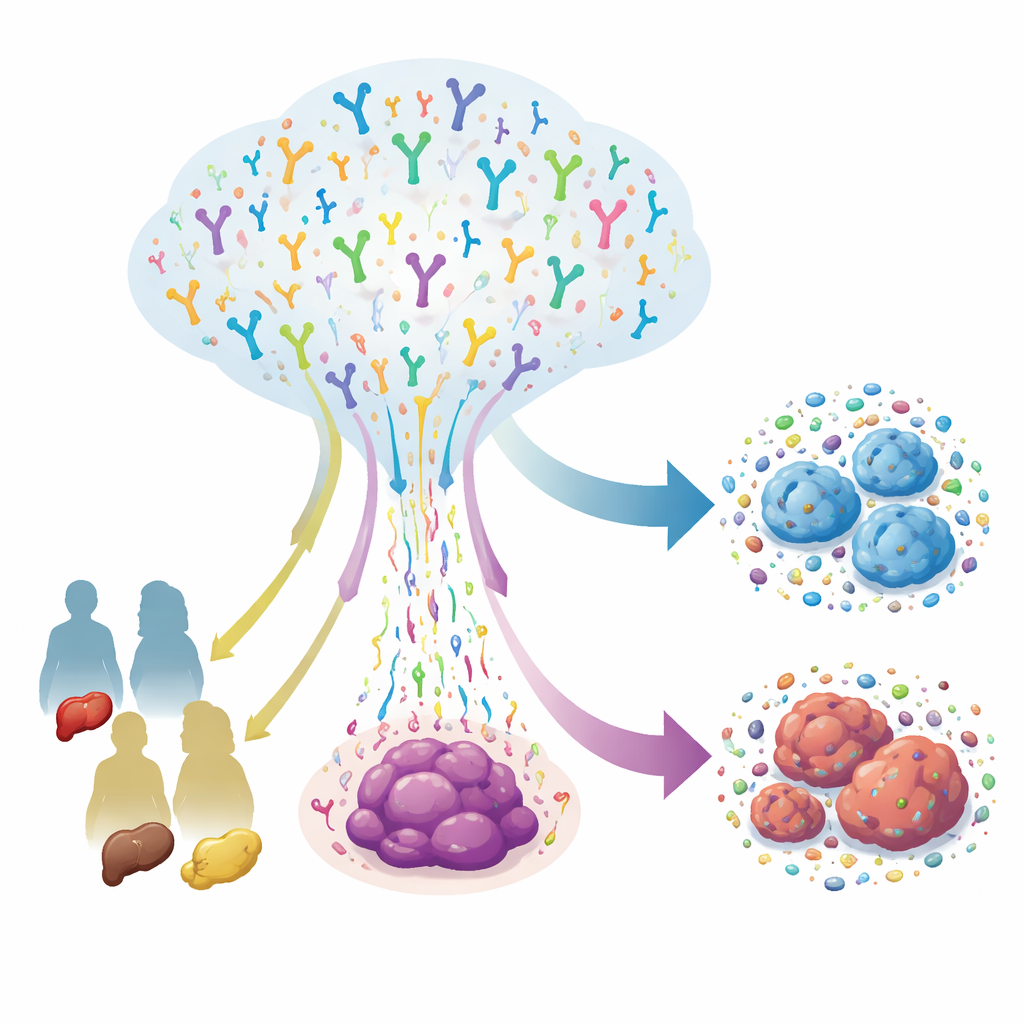
Разные раки — разные иммунные стратегии
Хотя все эти опухоли возникают в органах пищеварения, они не привлекают и не формируют Т-клетки одинаково. Колоректальные раки были обогащены определёнными сочетаниями генетических сегментов рецепторов в классической β-цепи, что указывает на значимую роль традиционных Т-клеток. Гастрические раки, напротив, демонстрировали более широкое использование γδ-Т-клеточных рецепторов, что намекает на особую роль этих менее изученных дозорных в опухолях желудка. При анализе самой критичной части рецептора — короткой петли, которая непосредственно контактирует с мишенью — обнаружились общие последовательностные паттерны между типами рака, что говорит о том, что Т-клетки направляются схожими селективными давлением. Вместе с тем наблюдались и чёткие различия в длине, составе аминокислот и мелких повторяющихся «мотивов», что подразумевает, что каждый тип опухоли заставляет Т-клетки решать немного разные задачи распознавания.
Общие и уникальные мишени для иммунной атаки
Используя глобальную базу данных известных пар «рецептор — антиген», авторы соотнесли определённые паттерны рецепторов с их вероятными целями. Некоторые антигены встречались и в колоректальном, и в гастрическом раке, включая известные драйверы и иммунно-связанные белки, такие как KRAS, SF3B1, BST2 и несколько классических онко-тестикулярных антигенов. Эти общие мишени могут поддерживать «пан-канцерные» стратегии, использующие одни и те же иммунные инструменты для разных типов опухолей. Вместе с тем каждый тип рака имел и свои частные мишени. Колоректальные опухоли были связаны с антигенами, такими как MAGEA10, WT1 и слияниевым геном, обнаруженным только в раковых клетках, тогда как в гастрических опухолях уникально выделялся PABPC1 — белок, участвующий в регуляции мРНК. Такие опухелеспецифичные антигены представляют интерес как кандидаты для высокоселективных вакцин или генетически модифицированных Т-клеточных терапий, щадящих здоровые ткани.
Как имунные сигнатуры меняются при распространении рака
Исследование уделило особое внимание колоректальному раку с уже произошедшими метастазами, сравнив опухоли у пациентов с отдалённым распространением и без него. Метастатические опухоли были крупнее, чаще прорастали в кровеносные сосуды и сопровождались повышенным уровнем стандартных опухолевых маркёров в крови. Их репертуары Т-клеточных рецепторов тоже были богаче и сложнее, особенно в β-цепи, что согласуется с более жёстким и разнообразным иммунным противостоянием. Отслеживая клоны, общие для неметастатических и метастатических условий, исследователи сгруппировали их как стабильные, сокращающиеся или расширяющиеся популяции. Поразительным оказалось то, что некоторые γδ-Т-клеточные клоны, изначально редкие в первичных опухолях, значительно расширялись при метастазировании и становились более многочисленными по мере роста опухолей. Среди традиционных Т-клеток особенно расширенная группа клонов несла специфический последовательностный мотив в β-цепи и часто нацеливалась на MLANA, опухолево-ассоциированный антиген. Высокая экспрессия MLANA в колоректальных опухолях была связана с лучшей выживаемостью пациентов, что предполагает, что этот антиген может отмечать опухоли, остающиеся заметными для иммунной системы и отзывчивыми на иммунные терапии.
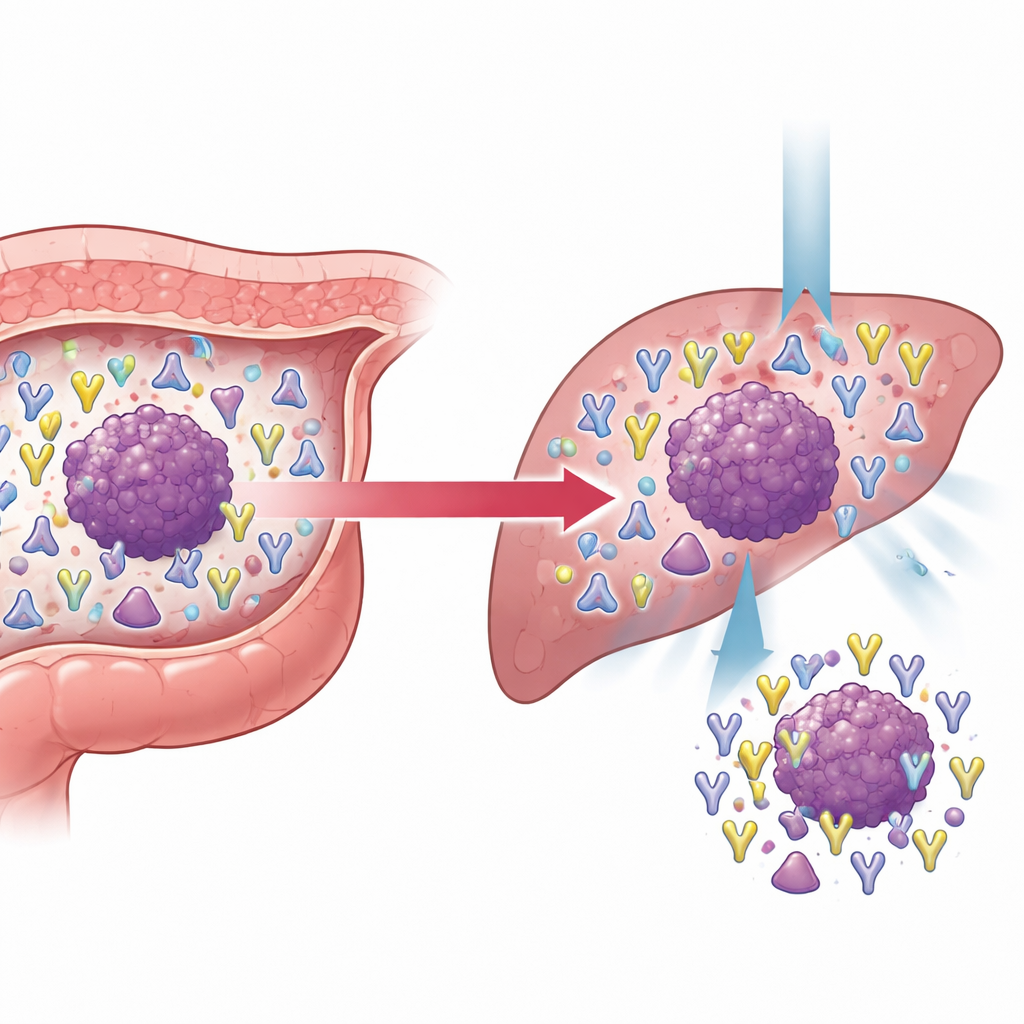
Что это значит для будущей помощи пациентам с раком
В целом работа показывает, что иммунный ландшафт внутри опухолей органов пищеварения не случаен, а формируется типом рака, стадией и распространением. Конкретные паттерны Т-клеточных рецепторов служат читаемыми отпечатками того, как иммунная система взаимодействует с опухолью, подчёркивая как общие, так и специфичные для каждого рака антигены. Для пациентов это открывает путь к будущему, в котором врачи смогут профилировать репертуары Т-клеточных рецепторов из образца опухоли, чтобы уточнять прогноз, разумнее выбирать иммунотерапию и даже разрабатывать индивидуальные лечения, использующие наиболее эффективные Т-клеточные клоны. В колоректальном и гастрическом раке идентифицированные здесь сигнатуры рецепторов и антигены дают дорожную карту для таких усилий по точной иммунотерапии.
Цитирование: Li, L., Li, J., Wang, F. et al. T-cell receptor clonotypic diversity and specialization in digestive system cancers. npj Precis. Onc. 10, 91 (2026). https://doi.org/10.1038/s41698-026-01294-4
Ключевые слова: Т-клеточные рецепторы, колоректальный рак, гастрический рак, опухолевая иммунитет, биомаркеры иммунотерапии