Clear Sky Science · ru
Мультимодальный одноклеточный профиль выявляет перекрестное взаимодействие макрофагов и стромальных клеток у пациентов с холангиокарциномой и неблагоприятным прогнозом
Скрытый район опухоли
Холангиокарцинома, рак желчных протоков в печени, встречается редко, но часто бывает смертельной, и эффективных методов лечения немного. Многие пациенты не отвечают на современные иммуннотерапевтические препараты, которые активируют иммунную систему против опухоли. В этом исследовании поставлен простой, но ключевой вопрос: что происходит внутри «района» опухоли, что мешает защитным клеткам организма выполнять свою работу — и почему у некоторых пациентов исход хуже, чем у других?
Почему иммунные клетки застревают у ворот
Вместо того чтобы быть просто рыхлой массой злокачественных клеток, холангиокарцинома пронизана поддерживающей тканью, называемой стромой, и множеством иммунных клеток. Профилируя отдельные клетки из опухолей, близлежащей ткани печени и крови, исследователи показали, что центр опухоли беден теми самыми Т-клетками, которые наиболее эффективны в уничтожении рака. Так называемые эффекторные Т-клетки памяти в основном остаются в окружающей печени и не проникают в само новообразование. Напротив, регуляторные Т-клетки — иммунные клетки, выполняющие роль «тормозов» — накапливаются внутри опухоли. Многие Т-клетки, которые всё же попадают внутрь, несут на своей поверхности несколько «выключателей», что указывает на их истощение и неспособность эффективно сражаться с раком.
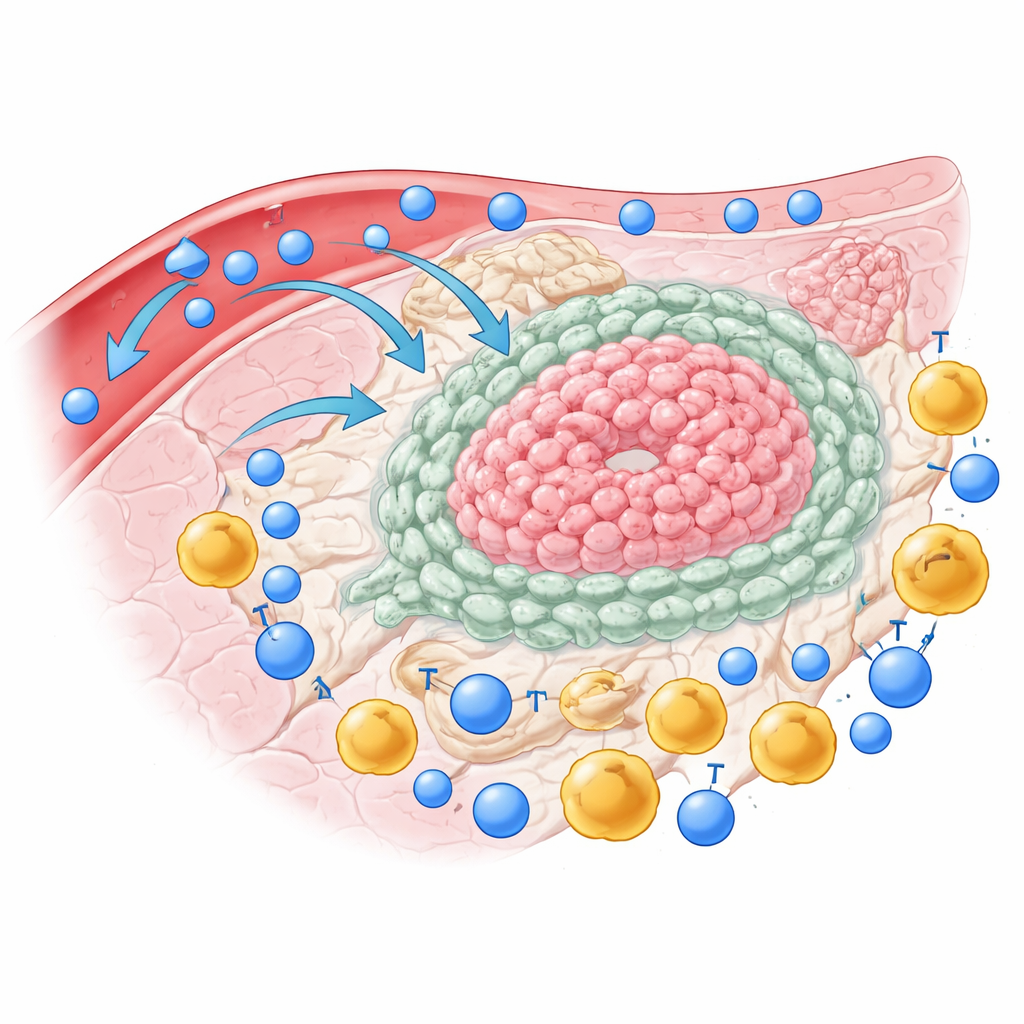
Подавляющий альянс опухоли
Чтобы взглянуть дальше, чем Т-клетки, команда сопоставила тысячи одиночных клеток из опухолей пациентов на уровне активности генов. Они обнаружили не только несколько разновидностей раковых клеток, но и отдельные группы поддерживающих клеток, таких как фибробласты, ассоциированные с опухолью, звездчатые клетки печени, клетки эндотелия кровеносных сосудов и макрофаги — иммунные клетки, которые могут либо атаковать, либо помогать опухоли. У пациентов с особенно плохим прогнозом определённый подтип раковых клеток проявлял более интенсивную коммуникацию со стромальными клетками и макрофагами. Вместо независимых действий эти типы клеток образовывали плотную сеть, которая, по-видимому, была рассчитана на то, чтобы не пускать атакующие Т-клетки и выключать их активность.
Тихие сигналы, которые отключают защиту
Вникая в эти «разговоры», учёные выявили ключевые молекулярные «рукопожатия», передаваемые от одной клетки другой. Раковые клетки продуцировали версикан — клейкий матриксный белок, который взаимодействует с датчиками на макрофагах и рецепторами роста на стромальных клетках, перестраивая ткань таким образом, что это благоприятствует росту опухоли и ослаблению иммунной атаки. Макрофаги выделяли TGF-бета, мощный сигнал, известный тем, что стимулирует образование регуляторных Т-клеток и ослабляет клетки, убивающие рак. Ещё один путь включал связывание GAS6 с рецептором AXL на макрофагах, фибробластах и раковых клетках — комбинацию, связанную в других типах рака с агрессивным поведением и уходом от иммунного контроля. Вместе эти сигналы создают петлю обратной связи: строма и макрофаги перестраивают окружение, усиливают «тормоза» иммунитета и помогают раковым клеткам выживать и размножаться.
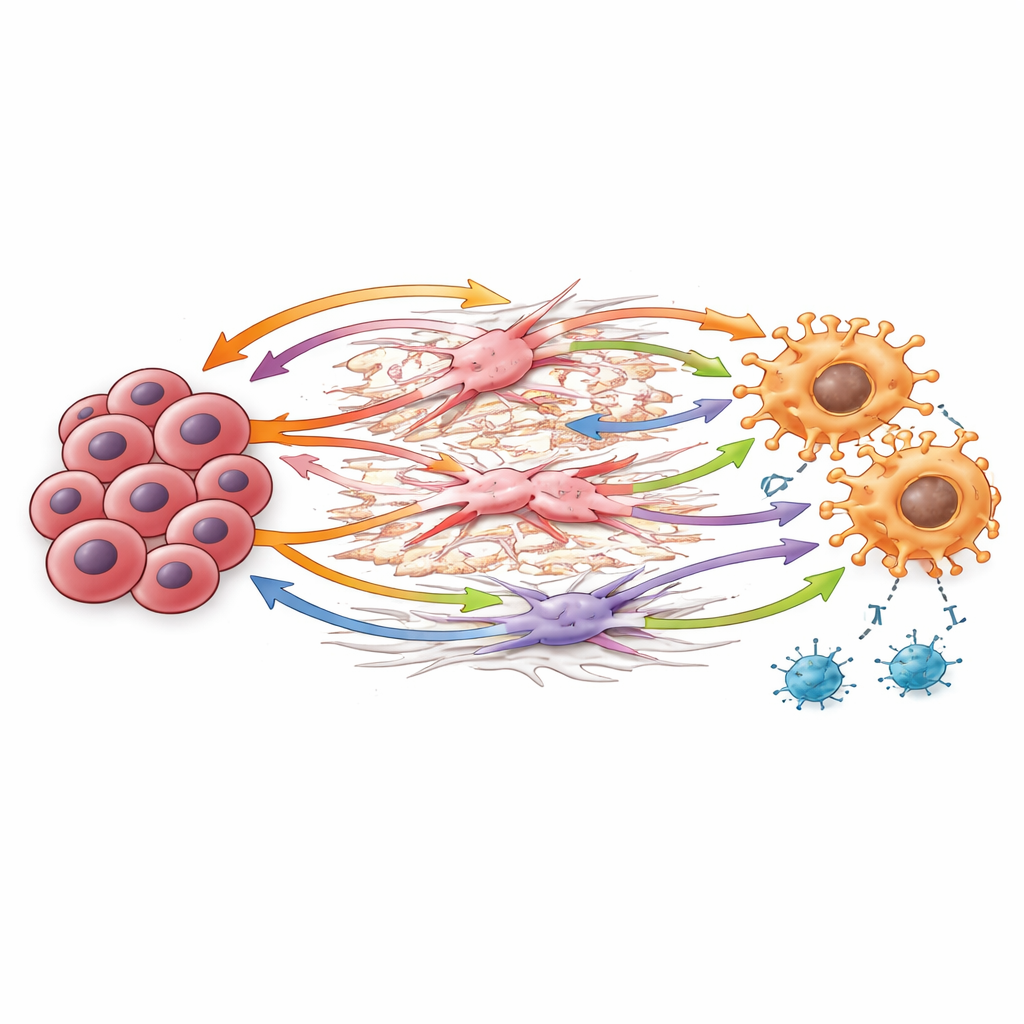
Шаблон, выходящий за пределы небольшой группы
Хотя работа на одноячеечном уровне проводилась на ограниченном числе пациентов, команда сопоставила свои выводы с гораздо большей публичной базой данных образцов внепечёночной холангиокарциномы. Математически оценивая, какие типы клеток присутствуют в каждой опухоли, они обнаружили значительную группу пациентов, чьи опухоли были богаты стромой и макрофагами и экспрессировали высокие уровни тех же ключевых молекул — версикан, GAS6, AXL и рецептора роста EGFR. Это указывает на то, что выявленная подавляющая сеть не является редкой особенностью, а может определять клинически важную подгруппу пациентов с особенно агрессивной биологией заболевания.
Что это означает для будущего лечения
Для пациентов с холангиокарциномой эти результаты помогают объяснить, почему стандартные ингибиторы иммунных контрольных точек часто оказываются недостаточно эффективными: проблема заключается не только в одной «педали тормоза» на Т-клетках, а в целой «окрестности» клеток, сотрудничающих, чтобы держать иммунную систему в узде. Исследование выделяет несколько сигнальных путей — таких как оси GAS6–AXL, версикан–TLR2 и TGF-бета–EGFR — которые можно было бы нацелить параллельно с ингибиторами контрольных точек, чтобы ослабить защитный щит опухоли. Также подчёркивается необходимость тестов, которые оценивают не только раковые клетки, но и окружающую ткань печени, чтобы определить, присутствуют ли агрессивные Т-клетки, но лишены ли они доступа. В долгосрочной перспективе расшифровка этой сложной клеточной перекрёстной связи может привести к более точному отбору пациентов для иммунотерапии и к разработке комбинированных схем лечения, дающих их иммунной системе реальный шанс ответить и победить.
Цитирование: Heij, L., Hayat, S., Reichel, K. et al. Multimodal single-cell profiling reveals crosstalk between macrophages and stromal cells in poor prognostic cholangiocarcinoma patients. npj Precis. Onc. 10, 105 (2026). https://doi.org/10.1038/s41698-026-01292-6
Ключевые слова: холангиокарцинома, микроокружение опухоли, одноклеточный профиль, истощение иммунитета, опухоле-ассоциированные макрофаги