Clear Sky Science · ru
Потеря микроРНК-29b способствует ДНМТ3b-опосредованному снижению STING и ослабляет радиотерапией-индуцируемый антитуморный иммунитет при колоректальном раке с мутацией KRAS
Почему это исследование важно
Для многих пациентов с раком прямой и толстой кишки лучевая терапия является ключевой частью лечения перед операцией. Тем не менее некоторые опухоли слабо уменьшаются, а рак часто возвращается или даёт метастазы. В этом исследовании изучают один распространённый генетический дефект при колоректальном раке — мутацию KRAS — чтобы объяснить, почему такие опухоли часто устойчивы к радиотерапии и новым иммунотерапиям, и предлагают стратегию, позволяющую вновь включить собственную иммунную систему организма против них.
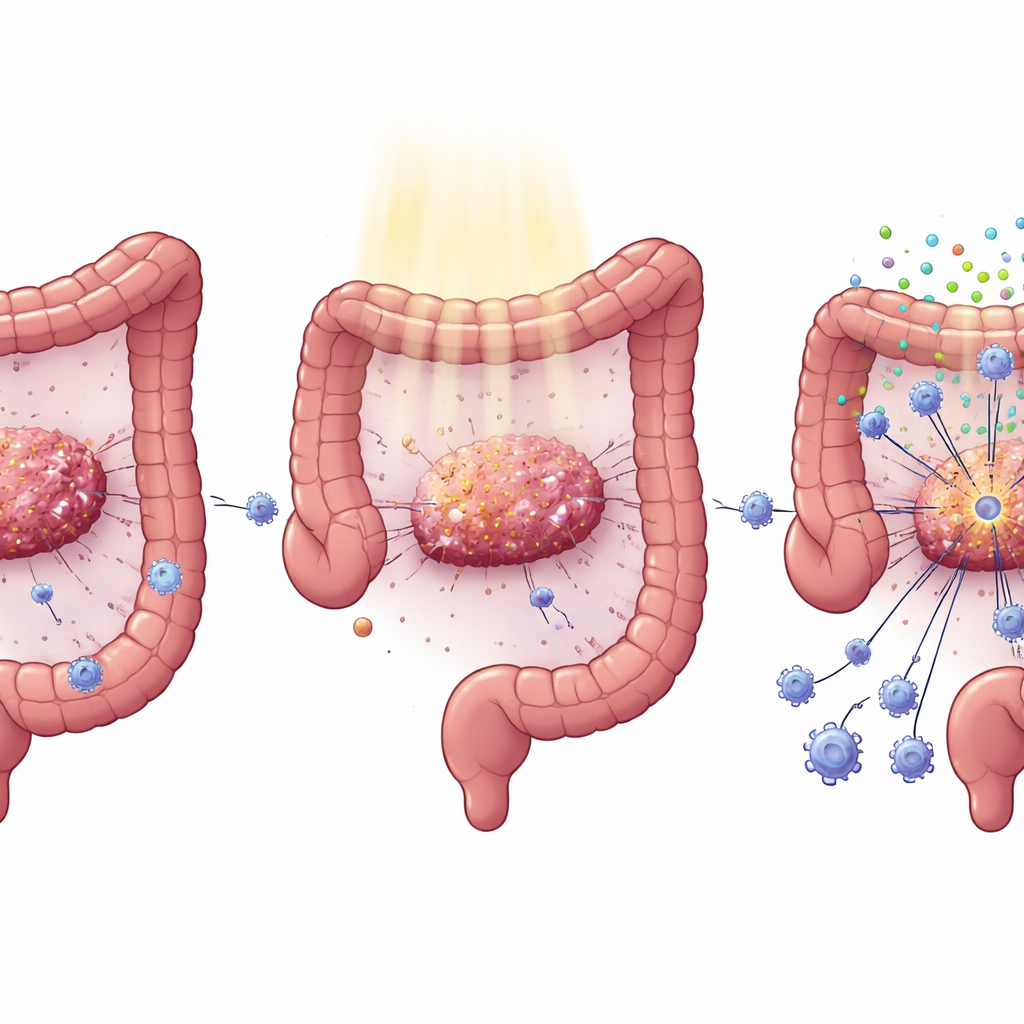
Распространённая мутация, которая скрывает опухоль от иммунной атаки
Колоректальный рак часто несёт мутации в гене KRAS, ключевом стимуляторе роста и распространения опухоли. Клиницисты уже заметили, что опухоли с мутацией KRAS обычно плохо реагируют как на таргетную терапию, так и на радиолечение. Анализ больших онкологических баз данных и образцов пациентов показал: опухоли с мутантным KRAS содержат меньше киллерных CD8 Т‑клеток и характеризуются ослабленной активностью интерфероновых сигналов, усиливающих иммунитет. У пациентов, получавших стандартную хемолучевую терапию перед операцией при раке прямой кишки, у пациентов с нормальным KRAS после лечения внутри опухолей появлялось значительно больше CD8 Т‑клеток, чем у тех, у кого был мутантный KRAS, что объясняет их лучшие исходы.
Отсутствующая «сигнализация тревоги» внутри раковых клеток
Радиотерапия не только повреждает ДНК опухоли; она также может действовать как сигнальный факел, заставляя раковые клетки выпускать фрагменты ДНК, которые активируют внутренний сигнальный путь cGAS–STING. При активности STING клетки вырабатывают интерфероны типа I и другие молекулы, которые привлекают и активируют иммунные клетки, включая Т‑клетки и дендритные клетки. Исследователи показали, что в колоректальных клетках, индуцированных мутантным KRAS, эта система сигнализации подавлена: после облучения такие клетки продуцировали гораздо меньше интерферонов и сопутствующих молекул. У мышей выключение KRAS в опухолях восстанавливало уровни STING, усиливало интерфероновые сигналы и приводило к увеличению числа CD4 и CD8 Т‑клеток, снижению регуляторных Т‑клеток и лучшему контролю опухоли — как в облучённых опухолях, так и в отдалённых, не облучённых «абсцопальных» опухолях.
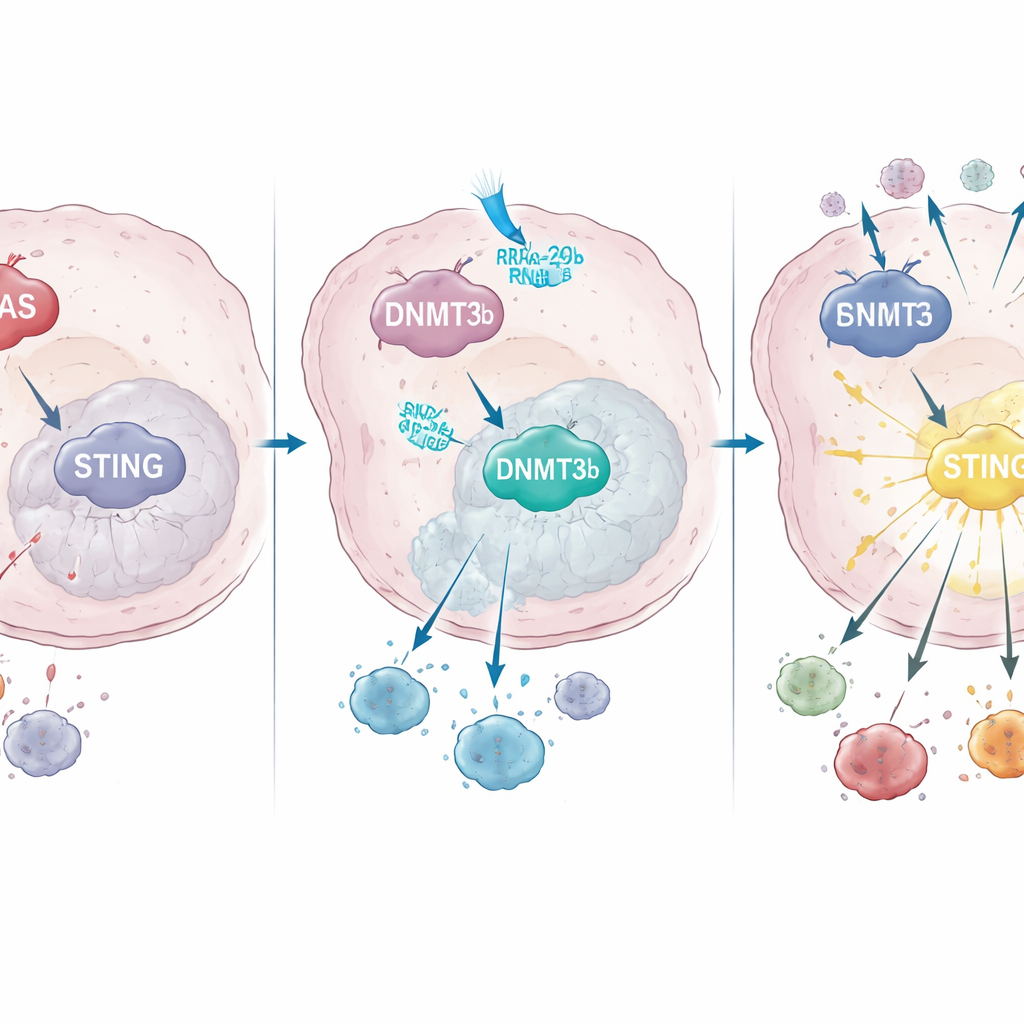
Как KRAS перенастраивает контроль генов, чтобы выключить STING
При более глубоком исследовании команда обнаружила, что мутантный KRAS повышает активность фермента, модифицирующего ДНК, под названием DNMT3b, который добавляет метильные группы в определённые участки ДНК и выключает соседние гены. В клеточных линиях и образцах пациентов высокий уровень DNMT3b сопровождался низким уровнем STING. Ключевой участок промотора STING — «переключатель» гена — был сильно метилирован в опухолях с мутантным KRAS, но не в опухолях с нормальным KRAS. У пациентов, чьи опухоли сохраняли способность повышать экспрессию STING после хемолучевой терапии, наблюдалась большая инфильтрация CD8 Т‑клеток и лучшее выживание, что подчёркивает важность этого пути для успешного лечения.
Маленькая РНК, которая может вновь разбудить «сигнал тревоги»
Далее авторы спросили, почему DNMT3b оказывается в таком избытке при мутантном KRAS. Секвенирование микроРНК выявило небольшую регуляторную РНК — микроРНК‑29b‑3p, которая обычно сдерживает DNMT3b, но сильно подавляется мутантным KRAS. Восстановление этой микроРНК в культурированных клетках с мутантным KRAS снижало DNMT3b, возвращало STING и усиливало выработку интерферонов после облучения; блокирование микроРНК давало обратный эффект. В опухолевых образцах у пациентов с мутантным KRAS наблюдалась тенденция: низкий уровень микроРНК‑29b‑3p, высокий DNMT3b и низкий STING, а у тех, у кого микроРНК‑29b‑3p был выше, выживаемость была лучше, связывая эту молекулярную цепочку с клиническими исходами.
Таргетная генная доставка, усиливающая радиотерапию и иммунотерапию
Чтобы перевести эти выводы в потенциальное лечение, команда создала безвредный вирус (AAV), доставляющий микроРНК‑29b‑3p под управлением промотора, активного преимущественно в клетках колоректального рака. В мышиных моделях с опухолями, несущими мутантный KRAS, введение этого AAV в сочетании с локальной радиотерапией резко уменьшало как облучённые, так и отдалённые необлучённые опухоли. В опухолях наблюдалось снижение DNMT3b, повышение STING, усиление интерфероновых сигналов и густая инфильтрация Т‑клеток и других иммунных клеток. При комбинировании той же терапии микроРНК‑29b‑3p с ингибитором контрольной точки PD‑1 выживаемость улучшалась ещё сильнее, и этот эффект зависел от CD8 Т‑клеток, подтверждая, что именно иммунная система обеспечивала основной терапевтический эффект.
Что это может значить для пациентов
Проще говоря, это исследование показывает, как колоректальные опухоли с мутацией KRAS «перерезают провод» внутренней системы оповещения, которую обычно активирует облучение, позволяя им уклоняться от иммунной атаки. Восстановлением одной малой РНК — микроРНК‑29b‑3p — исследователи смогли снизить DNMT3b, вновь активировать STING и превратить иммунологически «холодные» опухоли в «горячие», лучше реагирующие как на радиотерапию, так и на блокаду контрольных точек. Хотя эта работа пока находится на доклинической стадии, она указывает на перспективу будущих подходов, сочетающих облучение с таргетной генной терапией опухоли, что может преодолеть устойчивость при KRAS‑мутациях и сделать существующие терапии эффективными для большего числа пациентов.
Цитирование: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Ключевые слова: Колоректальный рак с мутацией KRAS, резистентность к радиотерапии, путь STING, микроРНК-29b, опухолевая иммунология