Clear Sky Science · ru
Сравнительный анализ стратегий мониторинга кДНК при распространённом НМРЛ с пропуском экзона 14 гена MET у пациентов, получавших энсартиниб
Почему анализ крови важен при раке лёгкого
Для людей с распространённым раком лёгкого одним из ключевых вопросов является то, работает ли новый препарат и насколько быстро врачи это поймут. В этом исследовании рассматривается подход на основе крови — с использованием крошечных фрагментов опухолевой ДНК, циркулирующей в крови — чтобы оперативно оценить, насколько эффективен таргетный препарат энсартиниб у пациентов с опухолями, имеющими определённую генетическую аномалию. Результаты свидетельствуют о том, что простой ранний анализ крови может указать, у каких пациентов лечение принесёт более длительную пользу, а кому потребуется смена стратегии.
Как отпечатки опухоли попадают в пробирку с кровью
Раковые клетки выбрасывают частицы своей генетической информации в кровоток — так называемую циркулирующую опухолевую ДНК. В этом испытании исследователи сосредоточились на пациентах с немелкоклеточным раком лёгкого, обусловленным изменением в гене MET, конкретно дефектом, известным как пропуск экзона 14. Все пациенты получали энсартиниб после неудачи предыдущих терапий. Образцы крови брали непосредственно перед началом лечения и снова через четыре недели. С помощью передового секвенирования, охватывающего 229 генов, связанных с раком, команда сгруппировала обнаруженные изменения в три категории: изменения в самом MET, набор хорошо известных драйверов рака и широкий «ловец» любых выявляемых мутаций.
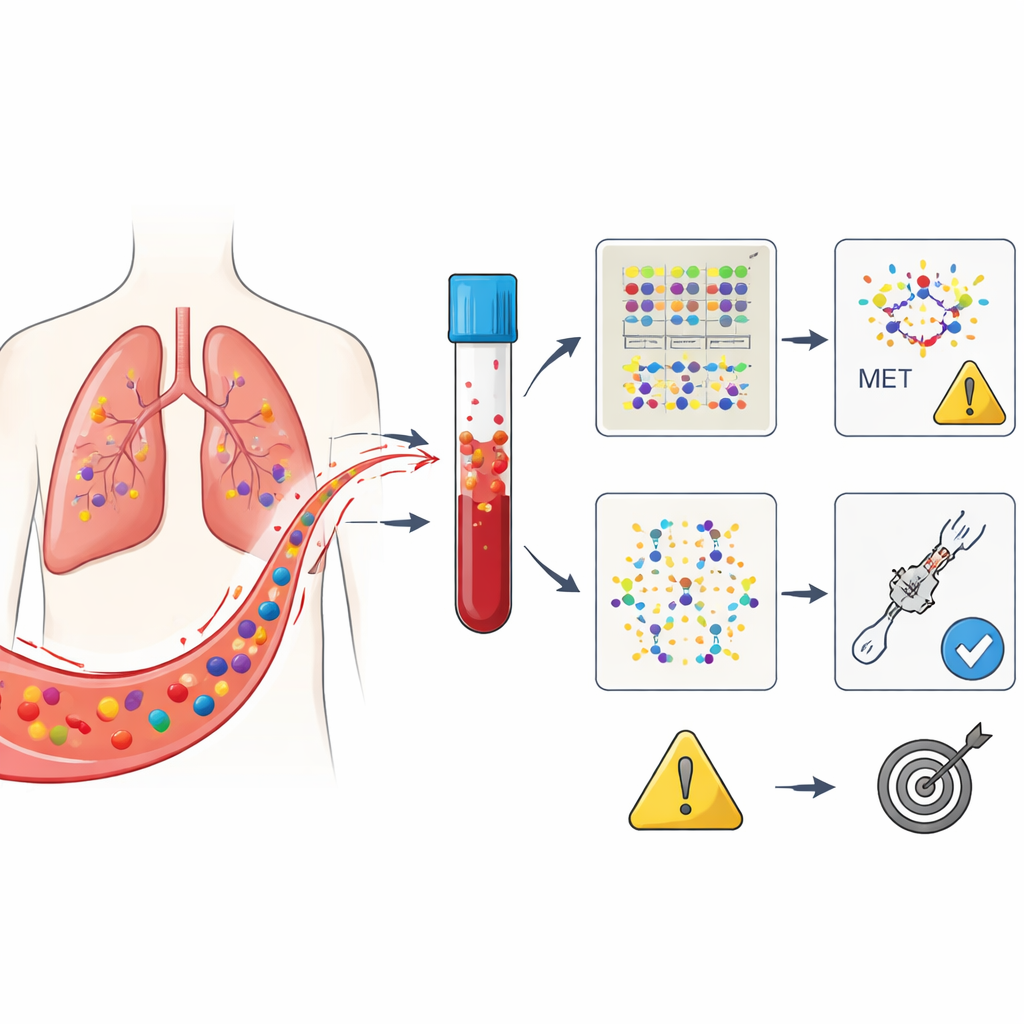
Три способа читать один и тот же сигнал в крови
Ключевой вопрос заключался в том, какой из этих трёх «взглядов» на кровь лучше предсказывает, кто откликнется на энсартиниб и как долго продлится ответ. В начале не у всех пациентов в крови обнаруживалась опухолевая ДНК, хотя их опухоли содержали дефект MET; это отражает неравномерность выброса ДНК различными опухолями. Ранний статус — положительный или отрицательный при базовом исследовании — сам по себе слабо предсказывал исход. Однако к отметке в четыре недели проявилась чёткая закономерность: пациенты, у которых в крови исчезли MET-сигналы, как правило, дольше сохраняли отсутствие прогрессирования по сравнению с теми, у кого эти сигналы сохранялись. Это было верно даже в тех случаях, когда снимки опухолей в это время оставались неоднозначными.
Когда сигналы MET исчезают, прогноз улучшается
При более детальном рассмотрении динамики результатов крови команда выделила три траектории. У некоторых пациентов MET-ДНК в крови никогда не выявляли, у других она была вначале и затем исчезла, а у третьих либо сохранялась, либо появлялись новые изменения в MET. Те, кто очистил MET-сигналы к четвёртой неделе, имели самый продолжительный период до прогрессирования заболевания — в среднем около девяти месяцев — и наивысшую частоту регрессии опухоли. Пациенты с сохраняющейся MET-ДНК чувствовали себя значительно хуже: прогрессирование происходило в среднем чуть более чем за два месяца. Мониторинг более широких наборов мутаций также давал полезную информацию, но был менее точен, поскольку множество низкоуровневых или нерелевантных изменений могло искажать картину.
Баланс между простотой и глубиной понимания
Использование только MET-ассоциированной ДНК как ориентира предлагало наиболее чёткую и простую картину того, помогает ли энсартиниб. Такой фокусный подход обладал высокой специфичностью: когда MET-сигналы исчезали, вероятность благоприятного исхода была велика. Это делает метод привлекательным как практичный инструмент: тесты на один ген дешевле, быстрее и проще в интерпретации, чем крупные генетические панели. В то же время сканирование большего числа генов сохраняет ценность, так как может выявить новые мутации, объясняющие последующую потерю чувствительности опухоли и указывающие на возможные варианты дальнейшей терапии. Исследование предлагает совмещать узконаправленный MET-ориентированный подход для ранних клинических решений с более широким мониторингом для отслеживания механизмов резистентности.
Что это значит для пациентов
Для неспециалиста главный вывод таков: анализ крови, проведённый уже через месяц после начала приёма энсартиниба, может дать представление о длительной эффективности препарата. Если в крови исчезает опухолевая MET-ДНК, шансы на значимую и продолжительную пользу высоки; если же она сохраняется, врачам, возможно, придётся более внимательно наблюдать пациента или рассмотреть альтернативы. Хотя это было относительно небольшое исследование с единственной группой, требующее подтверждения в больших когортах, оно усиливает идею о том, что «жидкостные биопсии» могут служить ранним индикатором эффективности таргетной терапии. В будущем такой мониторинг может помочь персонализировать лечение, избавляя пациентов от продолжения неэффективной терапии и быстрее направляя их к работающим вариантам.
Цитирование: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Ключевые слова: циркулирующая опухолевая ДНК, пропуск экзона 14 MET, энсартиниб, немелкоклеточный рак лёгкого, мониторинг жидкостной биопсией