Clear Sky Science · ru
Субъединица комплекса I митохондрий NDUFS4 при сверхэкспрессии стимулирует прогрессирование глиомы, регулируя митохондриальную функцию и COX5B
Почему важны энергоёмкие опухоли мозга
Глиомы относятся к числу наиболее агрессивных опухолей мозга и часто рецидивируют даже после операции, облучения и химиотерапии. В этом исследовании авторы заглядывают внутрь клеток глиомы, чтобы задать простой, но значимый вопрос: зависят ли эти опухоли от определённой части своих «электростанций» для роста и распространения? Проследив за небольшой митохондриальной белковой субъединицей NDUFS4, исследователи обнаружили метаболическую уязвимость, которая, по-видимому, подпитывает прогрессирование опухоли, при этом здоровые клетки мозга затрагиваются гораздо меньше.
Скрытый переключатель в «электростанциях» опухоли мозга
В каждой клетке митохондрии действуют как мини-генераторы, превращая питательные вещества в пригодную для работы энергию. В клетках глиомы эти генераторы работают на повышенных оборотах. Команда проанализировала крупные общедоступные онкологические наборы данных и данные одиночноклеточного секвенирования и обнаружила, что белок NDUFS4, компонент одного из основных энергопроизводящих комплексов митохондрий, стабильно повышен в ткани глиомы по сравнению с нормальным мозгом. Более высокие уровни NDUFS4 коррелировали с более продвинутой степенью опухоли и с более короткой выживаемостью пациентов. Просмотр на уровне отдельных клеток показал, что этот избыток NDUFS4 сосредоточен именно в опухолевых клетках, а не в окружающих некарциноматозных клетках мозга.
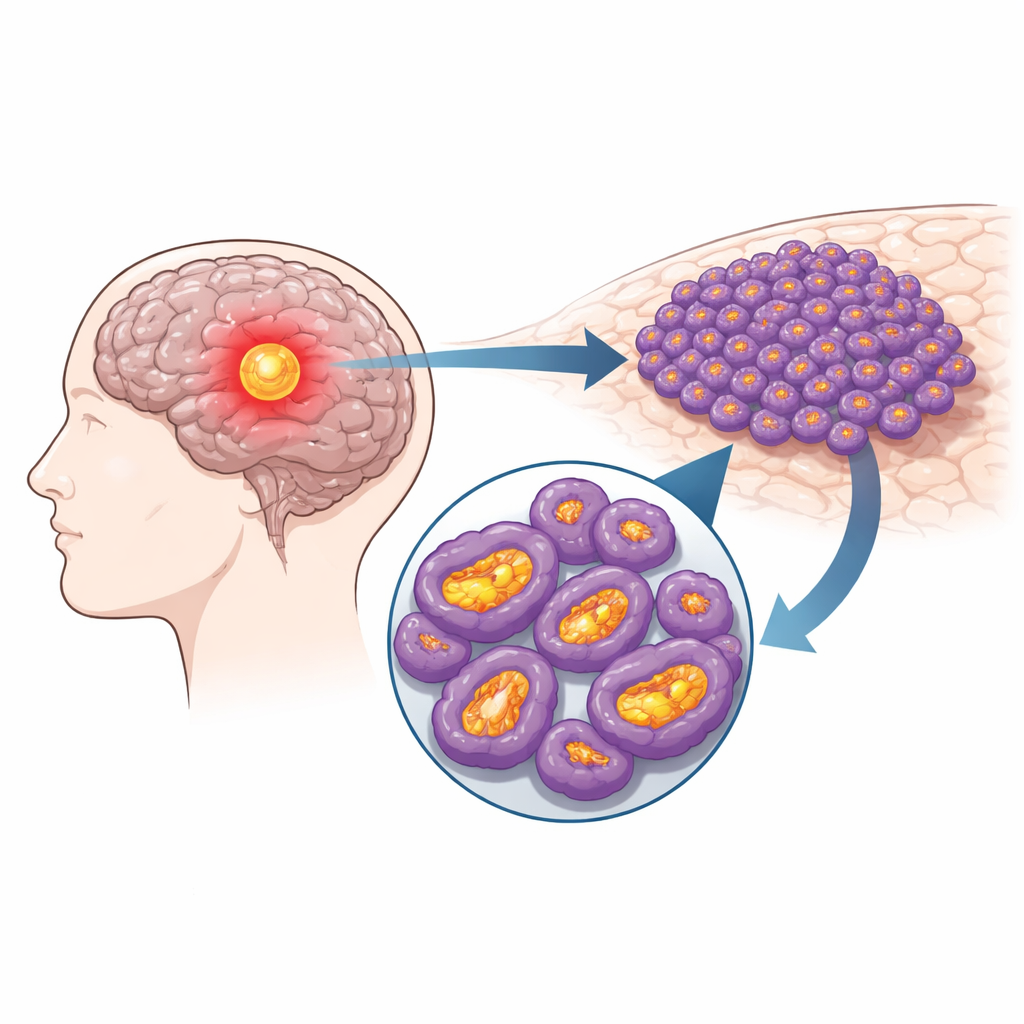
Понижение уровня энергии замедляет рак
Чтобы выяснить, является ли NDUFS4 просто маркером или настоящим драйвером, исследователи преднамеренно подавляли или удаляли его в клетках глиомы, полученных от пациентов и выращенных в лаборатории. При инактивции или нокауте NDUFS4 митохондрии клеток давали сбои: снижалось потребление кислорода, замедлялся ключевой шаг дыхания, уменьшался запас клеточного топлива (АТФ). Одновременно возрастало количество повреждающих побочных продуктов — реактивных форм кислорода, а внутренние мембраны клеток проявляли признаки стресса и окисления. Функционально такие энергетически обеднённые клетки опухоли реже делились, реже формировали колонии, меньше мигрировали и инвазировали, и демонстрировали больше признаков запрограммированной гибели. Примечательно, что тот же генетический удар по некарциногенным астроцитам — клеткам поддержки нормальной ткани мозга — вызвал мало или вовсе не вызвал вреда, что указывает на повышенную зависимость опухолевых клеток от этого митохондриального переключателя.
Повышение мощности делает опухоли более агрессивными
Обратная сторона эксперимента дала столь же наглядный результат. Когда учёные заставляли клетки глиомы продуцировать больше NDUFS4, митохондрии становились более активными: рос выход энергии и активность ключевого дыхательного комплекса. Такие «усиленные» клетки росли быстрее, легче мигрировали и агрессивнее проникали через барьеры, как в первичных клетках пациентов, так и в стандартных лабораторных линиях. В моделях на мышах клетки глиомы, запрограммированные на высокий уровень NDUFS4, формировали более крупные внутричерепные опухоли, тогда как клетки с пониженным NDUFS4 росли в мозге значительно медленнее, демонстрировали более слабую митохондриальную функцию, больше окислительных повреждений, меньше делящихся клеток и больше гибнущих. В совокупности эти эксперименты подтверждают, что NDUFS4 — не просто попутчик, а драйвер прогрессирования глиомы.
Связующий белок связывает контроль энергии с поведением опухоли
Углубившись, команда изучила, как NDUFS4 оказывает столь широкое воздействие. Перекрёстный анализ данных экспрессии генов в тканях опухоли в целом, одиночных клетках и карт белков в раковых клетках привёл их к другому митохондриальному белку — COX5B, как к ключевому партнёру. COX5B участвует в выполнении финального шага основной цепочки энергетического синтеза клетки. Он был тесно коррелирован с уровнями NDUFS4 в глиомах и уже известен как повышенный в других видах рака. При подавлении COX5B в клетках глиомы наблюдалась та же картина, что и при потере NDUFS4: ослабление митохондриальной функции, рост окислительного стресса, замедление роста и миграции, и повышение гибели клеток. Критически важно, что восстановление COX5B в клетках с дефицитом NDUFS4 обращало большую часть митохондриального повреждения и антиопухолевого эффекта назад. Также исследователи обнаружили, что NDUFS4 влияет на то, насколько сильно фактор транскрипции Sp1 связывается с регуляторной областью гена COX5B, помогая настраивать уровень продуцирования COX5B клеткой.
Что это значит для будущих методов лечения рака мозга
Для неспециалиста центральное послание таково: многие глиомы, по-видимому, опираются на сверхактивную энергетическую систему, сосредоточенную вокруг NDUFS4 и его связанного партнёра COX5B. Понижение активности этой системы лишает опухолевые клетки топлива и баланса, необходимых для роста и инвазии, при этом клетки поддержки нормального мозга сравнительно меньше страдают. Поскольку эта уязвимость последовательно проявляется в образцах пациентов, изолированных клетках и моделях на мышах, NDUFS4 — и его контроль над COX5B — выступает многообещающей мишенью для новых препаратов. Терапии, выборочно нарушающие этот митохондриальный «энергетический контур», могли бы дополнить существующие методы лечения, потенциально замедляя рост опухоли и продлевая выживание без серьёзного ущерба для здоровой ткани мозга.
Цитирование: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
Ключевые слова: глиома, митохондрии, NDUFS4, COX5B, метаболизм рака мозга