Clear Sky Science · ru
Интерпретируемая модель глубокого обучения для предсказания молекулярных подтипов рака эндометрия по окрашенным H&E слайдам
Почему это важно для женского здоровья
Рак эндометрия, возникающий в слизистой оболочке матки, — один из наиболее частых видов рака у женщин, и уровень смертности от него растёт во всём мире. Врачи теперь знают, что этот рак включает несколько молекулярных «вариантов», которые по‑разному реагируют на операцию, лучевую терапию, химиотерапию и новые иммунотерапевтические подходы. В настоящее время определение этих молекулярных подтипов обычно требует дорогостоящих и длительных генетических тестов, которые во многих больницах сложно обеспечить. В этом исследовании проверяют, может ли специально разработанная система искусственного интеллекта (ИИ) анализировать рутинные патологические слайды — розово‑фиолетовые изображения тканей, которые берут у всех пациенток — и с достаточной точностью определять молекулярные подтипы, что потенциально сделает персонализированное лечение более доступным.
Взгляд на разнообразие опухолей
Не все рак эндометрия ведут себя одинаково. Некоторые растут медленно и остаются в пределах матки; другие распространяются рано и сложнее поддаются лечению. Современные руководства разделяют эти опухоли на четыре молекулярных подтипа на основании изменений ДНК и механизмов репарации генетического повреждения. Эти категории помогают прогнозировать исход и определять тактику — например, объём операции и целесообразность иммунотерапии. Однако необходимые генетические тесты и специальные иммуногистохимические окраски дороги, требуют экспертной интерпретации и часто недоступны в небольших или ресурсно‑ограниченных больницах. Патологи давно подозревали, что многие молекулярные различия оставляют визуальные подсказки в архитектуре клеток и стромы, однако эти признаки могут быть слишком тонкими и сложными для стабильной оценки невооружённым глазом.
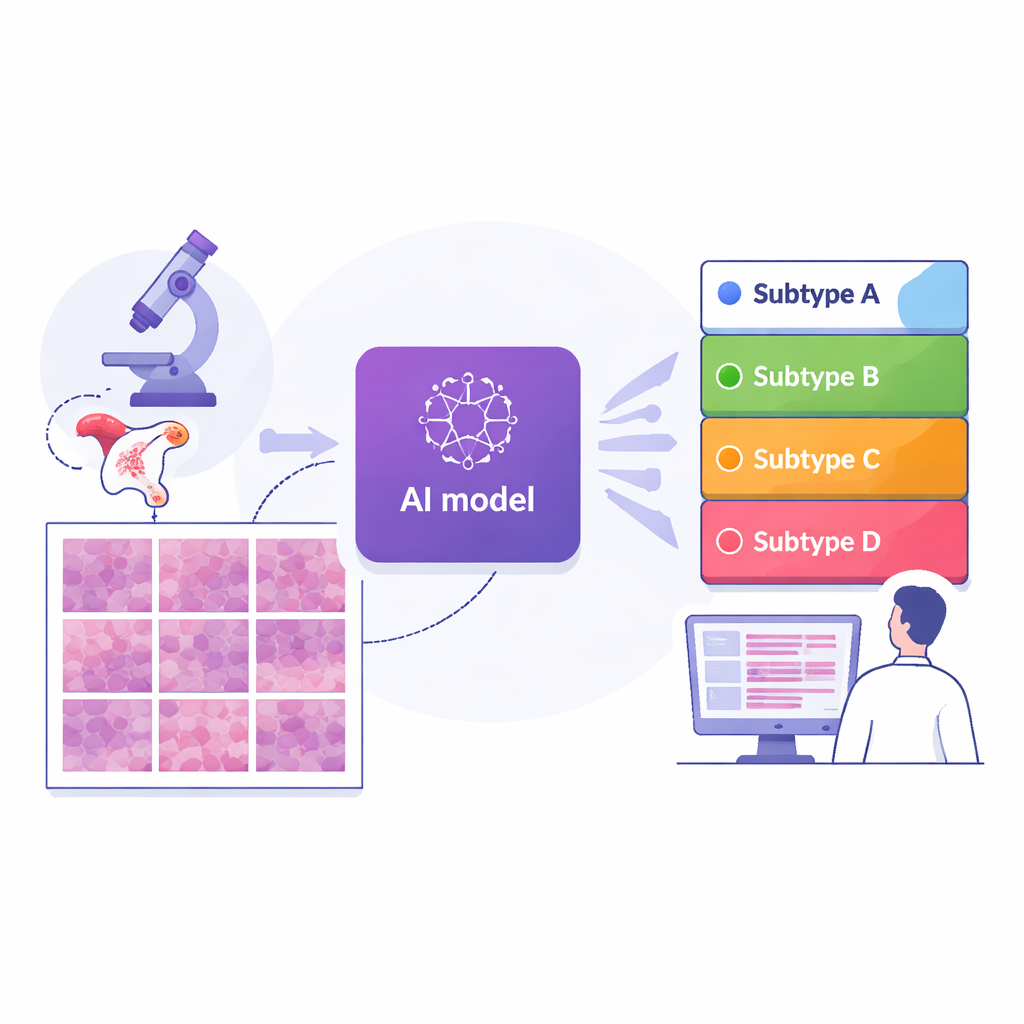
Обучение компьютеров «читать» патологические слайды
Исследователи собрали цифровые изображения 364 слайдов тканей от 324 пациенток, лечившихся в крупном онкологическом центре в Шанхае, а также две независимые контрольные группы: 296 слайдов из международного открытого датасета и 36 слайдов из другой больницы в Сучжоу. Для каждого случая уже был определён один из четырёх молекулярных подтипов с помощью продвинутых генетических тестов. Команда разбила каждое изображение целого слайда на тысячи маленьких тайлов и обучила модель глубокого обучения — тип ИИ, используемый для распознавания изображений — анализировать каждый тайл и оценивать вероятность его принадлежности к каждому подтипу. Усредняя предсказания по всем тайлам слайда, система выдавала единственное предсказание подтипа для каждой пациентки, что в целом отражает клинический подход к оценке опухоли в целом.
Насколько хорошо работала система
В основной шанхайской когорте ИИ продемонстрировал высокий уровень точности: общий показатель разделения четырёх подтипов (измеряемый стандартной статистикой, где 0.5 соответствует угадыванию, а 1.0 — идеальному разделению) составил примерно 0.87. Производительность оставалась высокой — около 0.84 — при тестировании на двух внешних группах, полученных из других больниц и слайнинговых систем, что говорит о разумной устойчивости подхода. По сравнению с несколькими ведущими AI‑стратегиями, использующими более сложные схемы внимания или агрегации, эта end‑to‑end модель на современном ядре анализа изображений в целом показала лучшие результаты. Важно, что авторы спроектировали систему так, чтобы её можно было интерпретировать: они использовали инструменты визуализации, чтобы подсвечивать именно те области каждого тайла, на которые опирался ИИ при принятии решения.
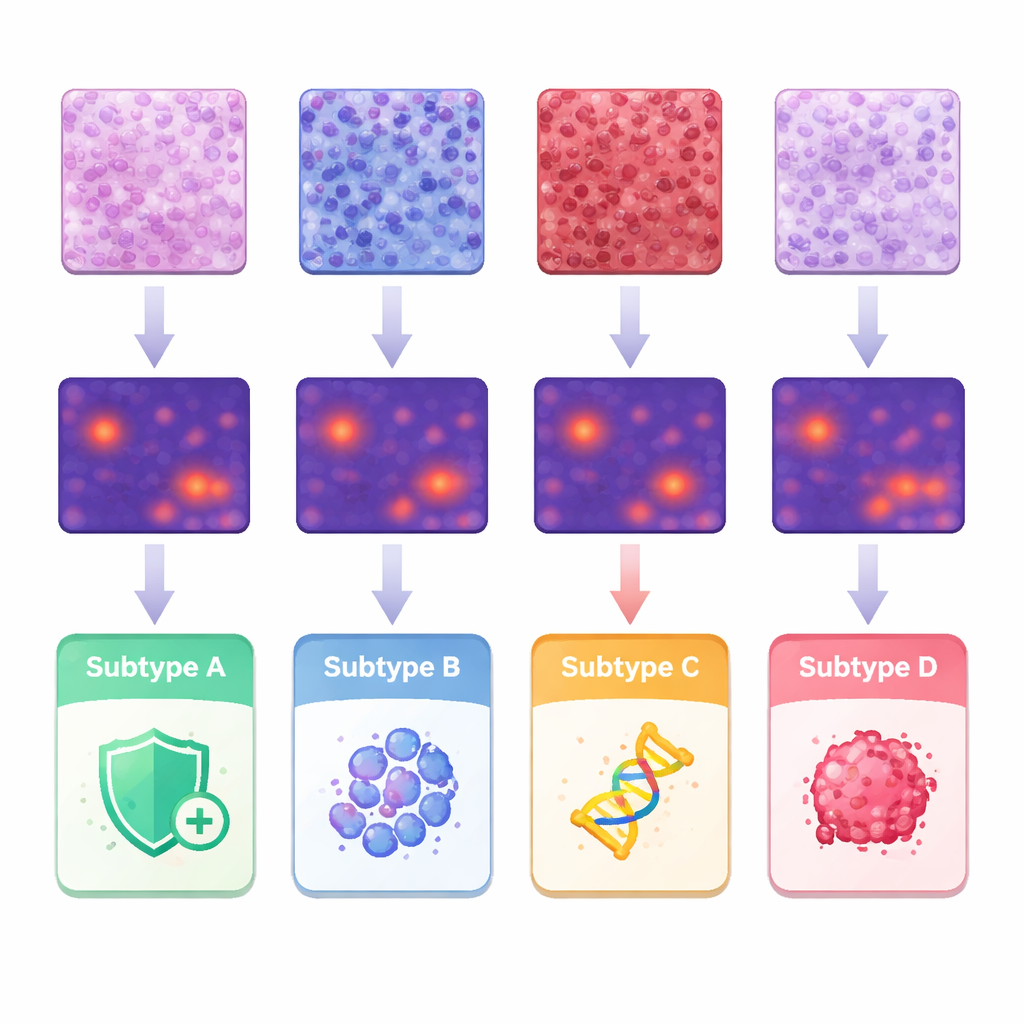
Что «видел» ИИ в микроокружении опухоли
Чтобы понять, какие признаки лежали в основе предсказаний, команда связала тепловые карты ИИ с классическими наблюдениями патологии и с подробными измерениями формы и расположения отдельных клеток. Опухоли одного подтипа демонстрировали плотную инфильтрацию иммунными клетками в строме, другой подтип чаще имел плотно упакованные структурные клетки. Третья группа показывала более сплошные пласты сильно атипичных опухолевых клеток, а подтип, ассоциированный с агрессивным поведением, отличался папиллярными, пальцеобразными структурами и очень неправильными ядрами. Сегментировав и проанализировав около 245 миллионов клеток, исследователи количественно охарактеризовали различия в размере клеток, вариабельности и расстоянии между ними, и показали, как определённые комбинации коррелировали с конкретными подтипами. Эти результаты подтверждают идею о том, что молекулярные различия оставляют распознаваемый отпечаток в архитектуре ткани, который машины могут системно выявлять.
От доказательства концепции к клинической помощи
Эта работа не ставит своей целью заменить генетическое тестирование; наоборот, она предлагает инструмент триажа «H&E‑вперед», использующий стандартное окрашивание, которое уже применяется для каждой биопсии. На практике карта вероятностей подтипа, сгенерированная ИИ, могла бы помочь патологам решить, какие подтверждающие тесты назначать в первую очередь, приоритизировать ограниченный материал для самых информативных анализов и ускорять терапевтические решения, особенно в учреждениях, где полное молекулярное профилирование затруднено. Исследование также подчёркивает текущие ограничения, такие как худшая работа для самого редкого подтипа и необходимость более крупных и разнообразных наборов данных перед внедрением. Тем не менее работа убедительно демонстрирует, что рутинные микроскопические изображения содержат достаточно скрытой информации, чтобы ИИ мог приближённо восстановить сложные молекулярные метки, открывая путь к более справедливой, основанной на данных помощи женщинам с раком эндометрия.
Цитирование: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Ключевые слова: рак эндометрия, цифровая патология, глубокое обучение, молекулярные подтипы, точная онкология