Clear Sky Science · ru
Интегрированный атлас рака легкого на уровне одиночных клеток выявляет различающиеся фенотипы фибробластов при аденокарциноме и плоскоклеточном раке
Почему окружение опухоли имеет значение
Рак легкого — это не только злокачественные клетки. Это скорее переполненный город, где клетки опухоли соседствуют с кровеносными сосудами, иммунными клетками и поддерживающими клетками. В этом исследовании задают на первый взгляд простой, но важный вопрос: строят ли два основных типа нерепрессивного рака легкого — аденокарцинома и плоскоклеточный рак — разные «районы» внутри легкого, и могут ли эти различия объяснить, почему у пациентов разная выживаемость? С помощью мощных методов чтения РНК в одиночной клетке исследователи сопоставили сотни тысяч отдельных клеток, чтобы показать, как одна ключевая группа поддерживающих клеток — фибробласты — ведет себя по‑разному в этих двух типах рака.
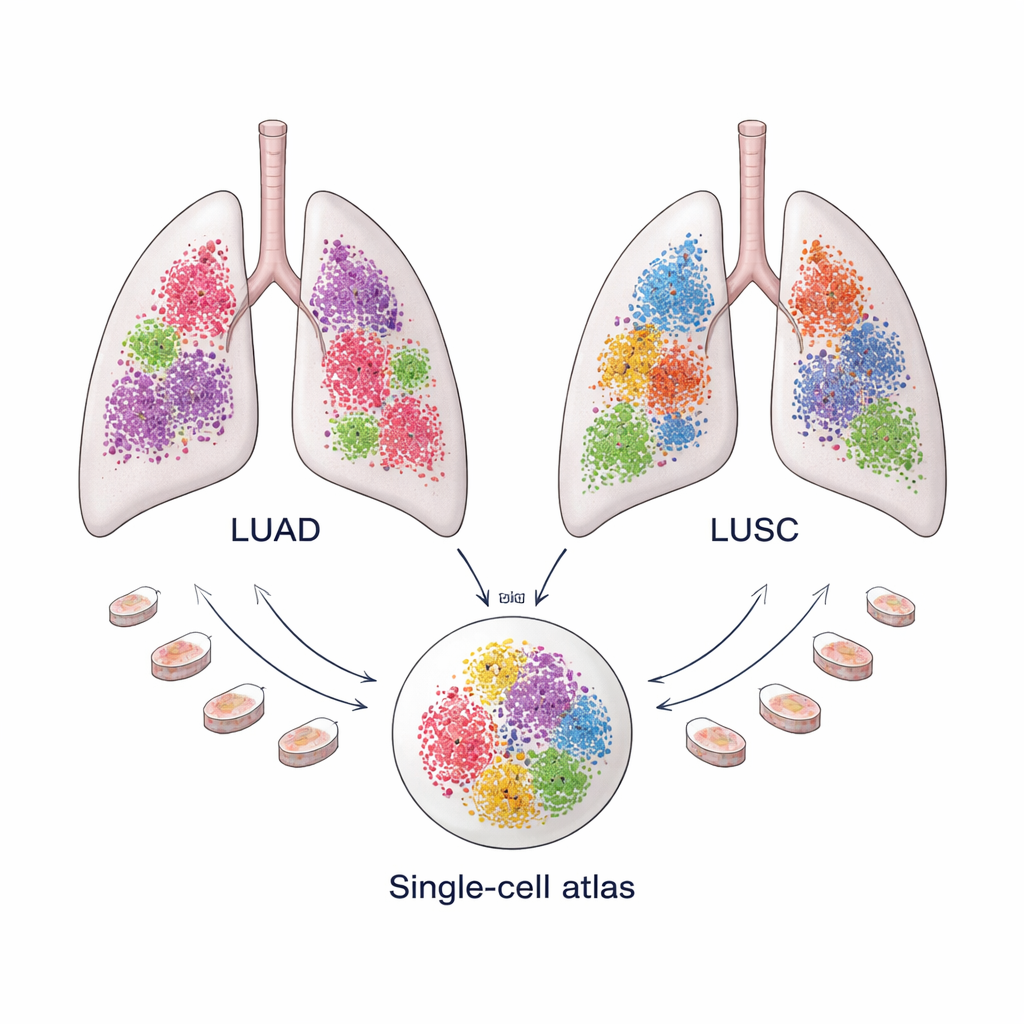
Два распространенных рака легкого — две разные экосистемы
Нерепрессивные (non–small cell) раки легкого составляют около 85 процентов всех раков легкого и представлены двумя основными типами: аденокарциномой легкого (LUAD), которая часто возникает в периферических отделах легкого, и плоскоклеточным раком легкого (LUSC), который склонен развиваться ближе к центральным отделам. Хотя их часто рассматривают под одним общим ярлыком, они по‑разному реагируют на терапию и имеют различную долгосрочную перспективу. Накопленные данные указывают, что эти различия обусловлены не только самимими раковыми клетками, но и «микроокружением опухоли» — набором иммунных клеток, сосудов и структурных клеток, которые окружают и взаимодействуют с опухолью.
Создание атласа рака легкого на уровне одиночных клеток
Чтобы подробно изучить эти микроокружения, команда собрала большой «атлас» данных сингл‑селл РНК‑секвенирования: 366 652 клетки из 175 образцов LUAD и 125 238 клеток из 74 образцов LUSC, взятых из десяти публичных наборов данных. Паттерн активности генов каждой клетки служил отпечатком, который позволял отнести клетки к основным группам, таким как иммунные клетки, клетки сосудов, раковые клетки и структурные или «стромальные» клетки. Сложные вычислительные методы устраняли технические шумы и выравнивали образцы, чтобы клетки разных пациентов можно было сравнивать напрямую. Такой масштаб важен, потому что некоторые типы клеток — особенно фибробласты — редки и трудно получить их в достаточном числе в рамках одного исследования.
Фибробласты: формирователи ландшафта опухоли
Фибробласты — поддерживающие клетки, которые формируют и ремоделируют соединительную ткань. В опухолях они превращаются в раково‑ассоциированные фибробласты (CAF), которые в зависимости от своего состояния могут либо сдерживать, либо способствовать росту опухоли. Сосредоточившись на более чем 8 700 фибробластах, авторы выделили пять основных подтипов CAF: миофибробластные CAF (mCAF), воспалительные CAF (iCAF), сосудисто‑ассоциированные CAF (vCAF), циклирующие CAF (cCAF) и антиген‑представляющие CAF (apCAF). Соотношение этих подтипов резко отличалось между LUAD и LUSC. Опухоли LUAD, как правило, содержали больше iCAF, которые секретируют высокие уровни провоспалительных молекул, тогда как опухоли LUSC были богаче mCAF, производящими жесткую, волокнистую матрицу и формирующими физический каркас опухоли.
Раковые клетки «обучают» фибробласты их ролям
Чтобы проверить, действительно ли раковые клетки инструктируют фибробласты принимать те или иные идентичности, исследователи выращивали нормальные легочные фибробласты в культурах вместе либо с клеточными линиями LUAD, либо с линиями LUSC. При воздействии LUAD‑клеток фибробласты включали гены, типичные для iCAF, включая известные провоспалительные сигналы, такие как IL‑6 и определенные хемокины. В парах с LUSC‑клетками те же фибробласты активировали гены mCAF, связанные с сократительной «мышечной» программой и синтезом коллагена. Анализы межклеточной коммуникации показали, что LUAD‑клетки используют цитокины, такие как IL‑1, LIF и OSM, чтобы индуцировать воспалительное состояние iCAF, тогда как LUSC‑клетки больше опираются на механические сигналы и неканонный WNT‑сигналинг, направляющие фибробласты в матриксо‑образующий mCAF‑статус.
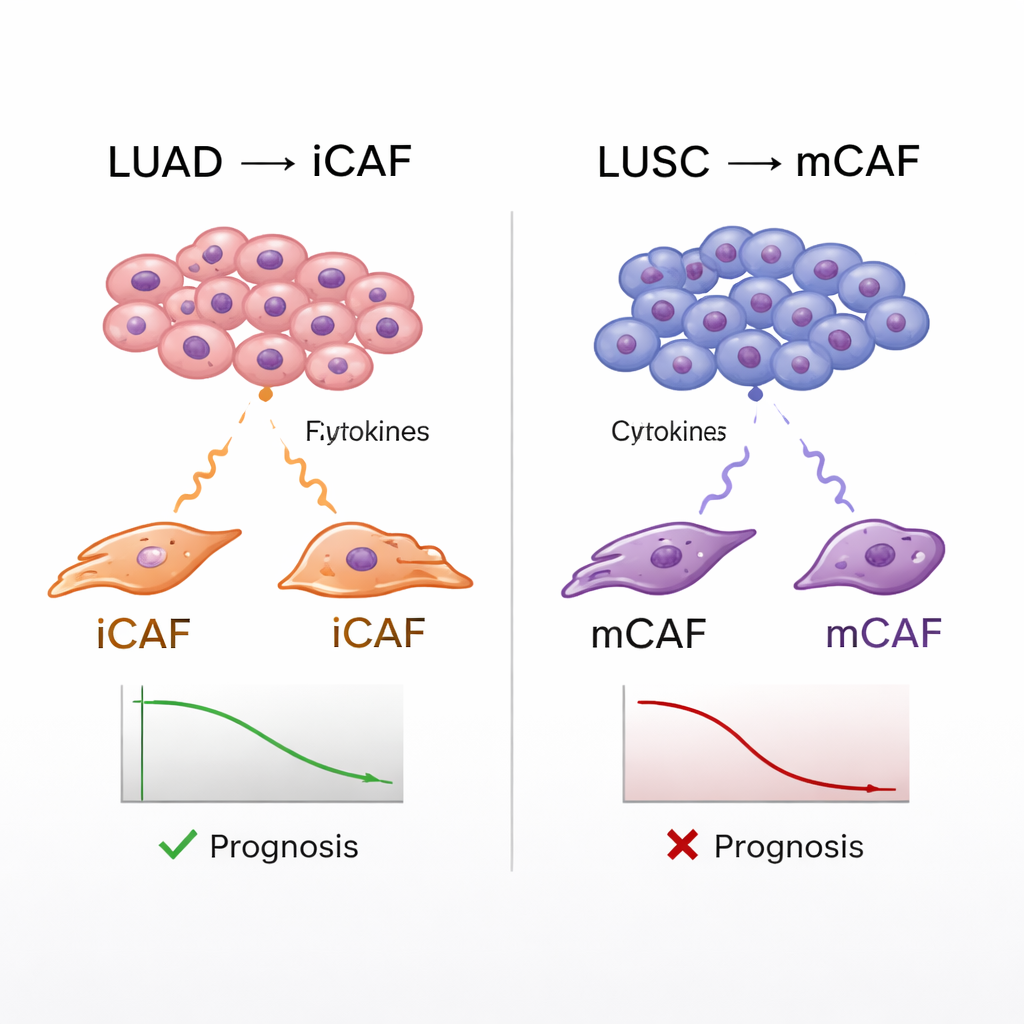
Связь типов фибробластов с исходами пациентов
Атлас также позволил авторам связать подтипы CAF с клиническими данными пациентов. Используя большие онкологические базы данных, они оценивали, насколько сильно опухоль каждого пациента экспрессирует генетические сигнатуры различных типов фибробластов, и сравнивали эти показатели с выживаемостью. В обеих группах, LUAD и LUSC, опухоли, обогащенные mCAF, ассоциировались с худшими исходами, что согласуется с идеей о том, что плотная волокнистая капсула вокруг опухолей может способствовать прогрессированию рака и блокировать иммунную атаку. iCAF же показали двойственность: в LUSC высокая сигнатура iCAF также прогнозировала худшую выживаемость, тогда как в LUAD она была связана с лучшими исходами. Дальнейшие анализы указали, что в LUSC iCAF способствуют притягиванию нейтрофилов — иммунных клеток, которые в этом контексте, по‑всему, подавляют полезные Т‑клетки — создавая особенно враждебную среду для эффективного иммунного ответа.
Что это значит для будущего лечения рака легкого
Для неспециалиста ключевая мысль в том, что не все поддерживающие клетки в опухолях легкого одинаковы, и один и тот же подтип фибробластов может иметь противоположное значение в зависимости от контекста рака. LUAD и LUSC различаются не только по ДНК раковых клеток; они формируют разные микроскопические экосистемы, которые влияют на рост опухолей и прогноз пациентов. Картируя эти экосистемы клетка за клеткой, исследование выделяет конкретные популяции фибробластов, которые могут служить маркерами прогноза или целями для будущих терапий — что в идеале позволит подбирать лечение не только по типу рака, но и по составу клеток, окружающих и поддерживающих опухоль.
Цитирование: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Ключевые слова: рак легкого, микроокружение опухоли, фибробласты, сингл‑селл РНК‑секвенирование, прогноз рака