Clear Sky Science · ru
Оценка иммуно‑онкологических биомаркеров и экспрессии β-катенина при ответе гепатоцеллюлярных карцином на иммунотерапию
Почему это исследование рака печени важно
Препараты иммунотерапии изменили подход к лечению ряда опухолей, но при раке печени — в частности при гепатоцеллюлярной карциноме (ГЦК) — они помогают лишь части пациентов, и у врачей по‑прежнему нет надежных тестов для прогнозирования, кто получит пользу. В этом исследовании проанализированы образцы опухолей более чем у 1 300 пациентов с ГЦК, чтобы выяснить, могут ли распространённые лабораторные маркеры, уже используемые для выбора иммунотерапии при других опухолях, дать подобное руководство и для рака печени.
В поисках полезных предупреждающих сигналов
Исследователи сосредоточились на группе сигналов на поверхности или внутри раковых клеток, которые могут влиять на ответ иммунной системы. Один из ключевых сигналов — PD‑L1, белок на опухолевых клетках, действующий как «тормоз» для атакующих иммунных клеток; при раке лёгкого и желудка высокий уровень PD‑L1 часто предсказывает лучший ответ на некоторые препараты иммунотерапии. Они также изучали опухолевую мутационную нагрузку (сколько изменений ДНК содержит опухоль), дефицит системы исправления несоответствий ДНК и активность сигнального пути роста, связанного с белком β‑катенином, кодируемым геном CTNNB1. С применением комплексного профилирования ДНК и РНК в сохранённых образцах опухолей они проверяли, коррелировали ли эти характеристики с тем, как долго пациенты оставались на терапии ингибиторами контрольных точек или какова была их общая выживаемость.
Распространённые тесты — редкие подсказки
Первой неожиданностью стало то, как мало печёночных опухолей имели те же иммуноонкологические маркеры, что и при других раках. Только около 6 процентов пациентов имели опухоли с высоким уровнем PD‑L1, ещё примерно 12 процентов — с низким уровнем; более четырёх из пяти опухолей были PD‑L1–отрицательными. Опухоли с очень высокой мутационной нагрузкой или с дефектами системы исправления несоответствий ДНК — признаки, часто предсказывающие сильный ответ на иммунотерапию при других опухолях — также были редки, каждое встречалось примерно в 5 процентах случаев или реже. При сравнении этих маркеров с продолжительностью лечения иммунотерапией и общей выживаемостью у пациентов уровни PD‑L1, мутационная нагрузка и статус системы исправления несоответствий не дали значимого разделения хороших и плохих ответов.
Активная иммунная среда, но эффекта не хватает
Хотя сам PD‑L1 не оказался полезным в виде простого «да/нет» теста, его уровень коррелировал с более воспалённым опухолевым микросредой. Опухоли с повышенным PD‑L1, как правило, были окружены большим числом иммунных клеток — такими как цитотоксические T‑клетки, регуляторные T‑клетки, B‑лимфоциты и некоторые макрофаги — и демонстрировали более выраженную активность генов, связанных с воспалением. Иными словами, PD‑L1‑высокие опухоли выглядели больше как классические «горячие» опухоли, распознаваемые иммунной системой. Тем не менее в этой когорте больных с раком печени такое иммунное оживление не перешло в явно лучшие результаты при иммунотерапии, что указывает на то, что другие барьеры, присущие уникальной среде печени, могут по‑прежнему ослаблять действие препаратов.
Загадка β‑катенина
Исследование также изучало путь Wnt/β‑катенин, который, как считают, помогает опухолям укрываться от иммунной атаки. Мутации в CTNNB1, гене, лежащем в основе этого пути, были чаще у PD‑L1–отрицательных опухолей, чем у PD‑L1‑высоких. При анализе пациентов, лечившихся иммунотерапией, высокая активность CTNNB1 не предсказывала однозначно лучшего или худшего исхода. Неожиданно среди пациентов, никогда не получавших иммунотерапию, те, у кого опухоли имели более высокую экспрессию CTNNB1, показали несколько лучшую общую выживаемость, хотя это наблюдение требует подтверждения. Другие генетические изменения — например, в TP53 и нескольких сигнальных генах — также различались между группами PD‑L1, но ни одно из них не сложилось в простой клинически применимый тест для прогнозирования успеха иммунотерапии.
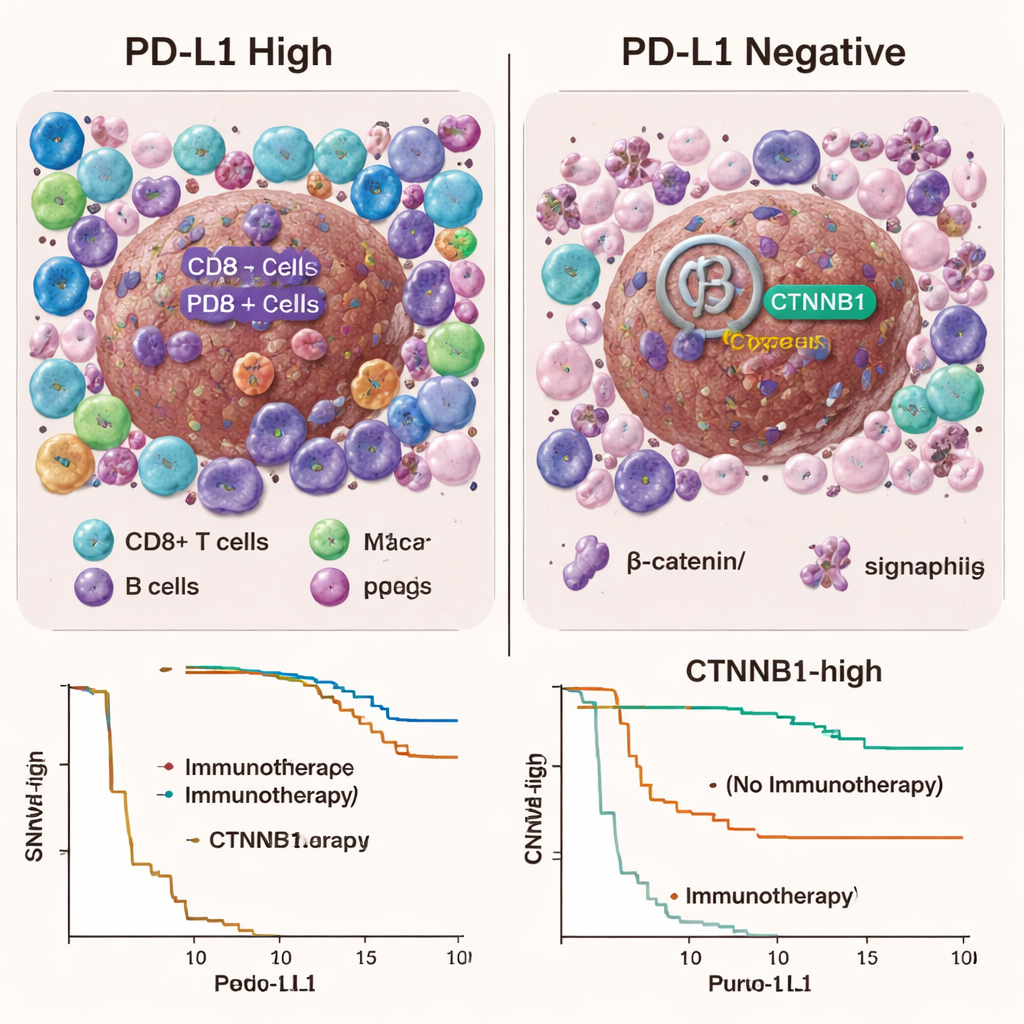
Что это означает для пациентов и врачей
Для людей с раком печени и их клиницистов выводы одновременно и трезвящие, и проясняющие. Тесты, которые сейчас являются стандартными инструментами для подбора иммунотерапии при раке лёгкого или желудка — окраска на PD‑L1, оценка мутационной нагрузки и статус системы исправления несоответствий — не дают надёжного прогноза пользы иммунотерапии при гепатоцеллюлярной карциноме. Печёночные опухоли часто находятся в сложной, иммунологически особой среде, и это исследование показывает, что привычные маркеры отражают лишь часть картины. Результаты указывают на то, что подходы к лечению ГЦК нельзя просто перенимать из других опухолей; необходимы новые, специфичные для печени иммунные сигнатуры и стратегии комбинированной терапии, чтобы лучше предсказывать и повышать долю пациентов, которые действительно выигрывают от иммунотерапии.
Цитирование: Sharma, G., Baca, Y., Goel, S. et al. Evaluation of immuno-oncologic biomarkers and β-catenin expression in response of hepatocellular carcinomas to immunotherapy. npj Precis. Onc. 10, 86 (2026). https://doi.org/10.1038/s41698-026-01275-7
Ключевые слова: гепатоцеллюлярная карцинома, биомаркеры для иммунотерапии, PD-L1, бета-катенин, микроокружение опухоли