Clear Sky Science · ru
TheraMind: ансамбль из нескольких LLM для ускорения репозиционирования лекарств при раке легкого посредством анализа клинических описаний случаев
Почему это важно для пациентов и врачей
Для людей с продвинутым раком легкого время на вес золота, и варианты лечения часто исчерпываются очень быстро. Разработка новых препаратов с нуля может занимать более десятилетия, тогда как разрозненные подсказки о полезных терапиях уже могут быть скрыты в опубликованных историях пациентов — так называемых описаниях случаев. В этой статье представлена TheraMind, система искусственного интеллекта, которая просматривает тысячи таких отчетов, чтобы выявить существующие лекарства, которые потенциально можно безопасно перепрофилировать для помощи больным с трудноизлечимым раком легкого.
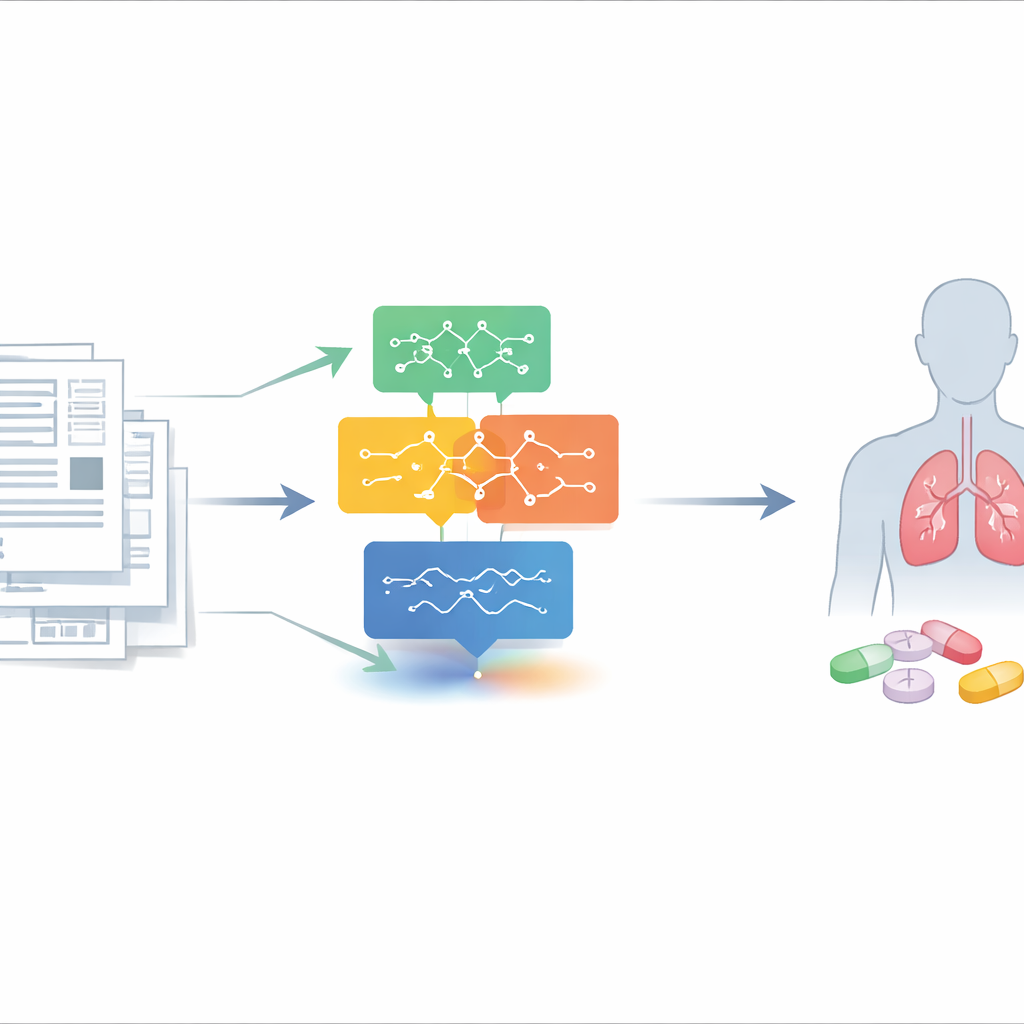
Задача поиска новых применений у старых препаратов
Немелкоклеточный рак легкого — самый смертоносный вид рака в мире, и показатели выживаемости остаются очень низкими после того, как болезнь распространилась. Открытие и тестирование новых препаратов с нуля идет медленно, дорого и рискованно. В отличие от этого, «репозиционированные» препараты уже одобрены для других состояний, поэтому их безопасность лучше изучена. Онкологи заинтересованы в таких лекарствах, особенно для пациентов, исчерпавших стандартные варианты лечения, но им нужны данные из реальной клинической практики, подтверждающие, что препарат действительно помог кому-то с раком легкого — а не только обнадеживающие лабораторные результаты. Эти клинические подсказки часто встречаются в отдельных описаниях случаев, похороненных глубоко в медицинской литературе, которые трудно и долго искать вручную.
Цифровой читатель для тысяч историй пациентов
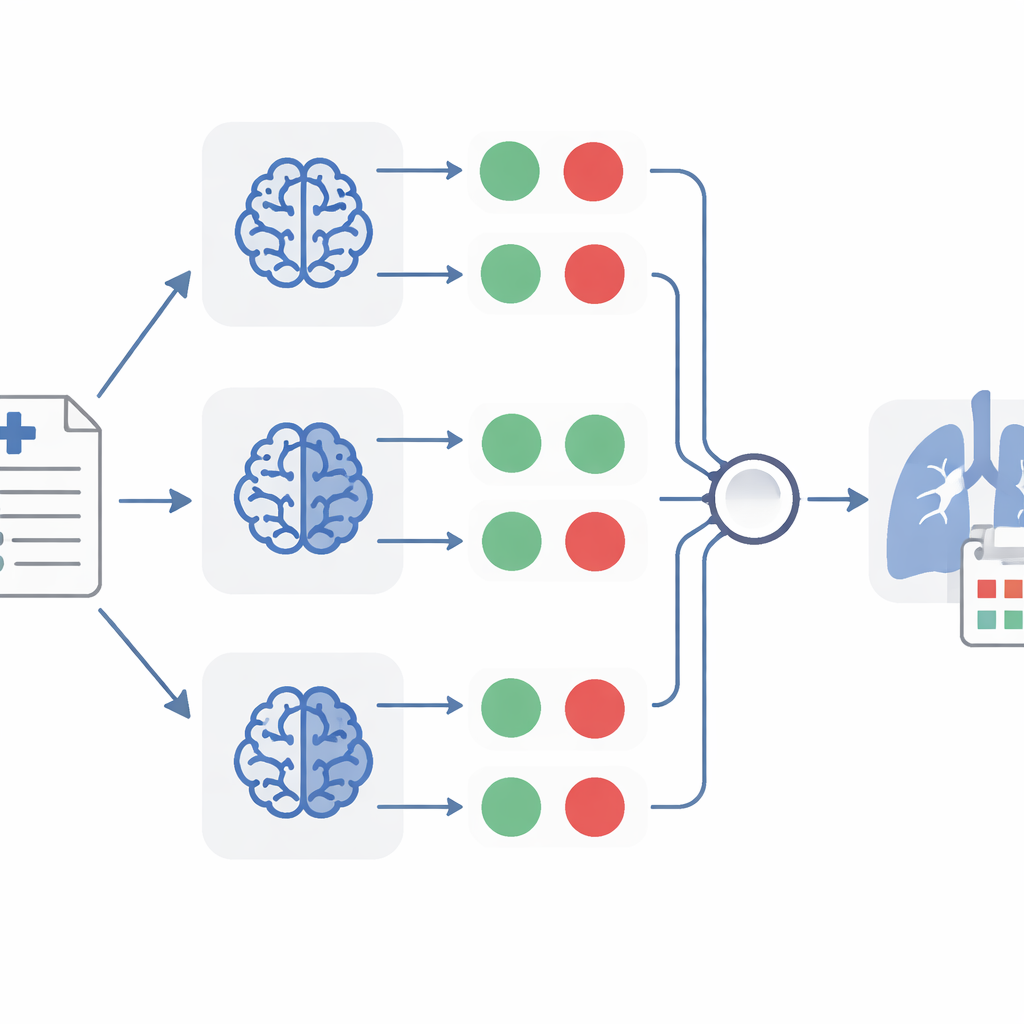
Исследователи создали TheraMind, чтобы она служила неутомимым и внимательным читателем описаний случаев. Начиная с 18 кандидатов на препараты, предложенных ранними геномными и лабораторными исследованиями, система автоматически извлекла 10 023 описания случаев из PubMed — крупнейшей базы медицинских статей. Затем текст каждого отчета был передан трем отдельным языковым моделям — разным AI«читателям», обученным понимать медицинские тексты. Для каждого отчета эти модели ответили на одни и те же четыре простых вопроса: указан ли в описании немелкоклеточный рак легкого? Был ли исследуемый препарат назначен специально для его лечения? Было ли лечение прекращено досрочно? И наблюдалась ли у пациента положительная клиническая реакция?
Как AI-команда приходит к совместному решению
После того как TheraMind переводит каждый отчет в набор ответов «да» или «нет», вступают в силу несколько уровней принятия решений. Один метод использует вручную разработанное дерево решений, которое требует выполнения всех четырех условий, прежде чем считать случай релевантным для репозиционирования. Другой позволяет одной модели более гибко оценивать доказательства, учитывая как ответы «да/нет», так и короткие объяснения, которые она сгенерировала. Самый мощный метод комбинирует три отдельные классификатора, каждый основан на разной модели, и принимает отчет только тогда, когда как минимум два из трех согласны, что он релевантен. Этот подход «большинства голосов» помогает компенсировать индивидуальные ошибки, подобно тому как несколько независимых врачей могут совместно просмотреть одну и ту же карту пациентов.
Что TheraMind обнаружила в отчетах о раке легкого
Примененная к большой коллекции описаний случаев TheraMind выделила 26 отчетов, которые сильно поддерживают использование десяти различных препаратов при немелкоклеточном раке легкого. Метод ансамбля достиг чувствительности примерно 92 процента, что означает, что он обнаружил почти все действительно релевантные отчеты, при этом сохраняя очень высокую специфичность — 99,7 процента — так что очень немногие нерелевантные отчеты прошли через фильтр. Для каждого выбранного отчета система также извлекла ключевые данные о пациенте — такие как возраст, пол, анамнез, состояние и предполагаемый препарат — в единый формат, а также сгенерировала короткое, понятное резюме случая. Человеческие рецензенты с биологическим и компьютерным образованием проверили эти результаты и подтвердили, что одна из моделей в особенности давала высокоточные и полные извлечения.
За пределами рака легкого и в клинику
Чтобы проверить гибкость системы, команда также направила TheraMind на рак молочной железы и несколько кандидатных препаратов, ранее выявленных их собственными исследованиями. В этом сценарии система не нашла совпадающих описаний случаев, что точно отражало текущее состояние научной литературы, а не выдумывало доказательства. Авторы утверждают, что подобный структурированный и прозрачный конвейер — объединяющий логику на основе правил с несколькими AI«читателями» — может помочь сократить разрыв между лабораторными открытиями и препаратами, готовыми к клиническим испытаниям. Они подчеркивают как перспективы применения подобных методов к другим видам рака, так и необходимость внимательного обращения с конфиденциальностью пациентов, если будущие версии будут подключаться непосредственно к электронным медицинским записям.
Что это означает для будущих методов лечения
Проще говоря, TheraMind превращает разрозненные, неструктурированные истории пациентов в организованные доказательства, на которые врачи и исследователи могут опереться. Быстро выявляя отчеты, в которых существующие препараты, по-видимому, помогают пациентам с раком легкого, система может указывать, какие репозиционированные лекарства заслуживают более тщательного изучения в клинических испытаниях. Хотя она не заменяет медицинскую экспертизу, этот много-модельный AI«читатель» предоставляет способ просеять горы медицинских текстов и представить короткий, надежный список перспективных вариантов для пациентов, которым срочно нужны новые возможности лечения.
Цитирование: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Ключевые слова: репозиционирование препаратов, рак легкого, описания клинических случаев, большие языковые модели, добыча клинических доказательств