Clear Sky Science · ru
Неоадъювантный синтилумаб, паклитаксел, связанный с альбумином, и карбоплатин при локально распространённой, резектабельной плоскоклеточной карциноме пищевода: клиническое исследование и механистическое исследование
Перелом в борьбе с опасным раком глотки
Рак пищевода — один из самых смертоносных видов рака в мире, часто выявляемый лишь тогда, когда он уже глубоко проникает в грудную полость. Многие пациенты всё ещё могут перенести операцию, но даже при современных схемах химио- и лучевой терапии риск рецидива остаётся высоким. В этом исследовании проверяют новый подход: усилить собственную защиту организма перед операцией и изучить, как опухоли и окружающие их клетки меняются под микроскопом в ответ на лечение. Результаты указывают на возможность более эффективной терапии и путь к действительно персонализированному лечению.
Новая трёхпрепаратная схема перед операцией
В исследование были включены 24 пациента в Китае с распространённой и агрессивной формой рака пищевода — плоскоклеточной карциномой. У всех опухоли были локально прогрессирующими, но всё ещё резектабельными. Перед операцией каждый пациент получил три цикла комбинированной терапии: синтилумаб — антитело, активирующее иммунитет и помогающее Т‑клеткам распознавать рак; а также два стандартных химиопрепарата — паклитаксел, связанный с альбумином, и карбоплатин. После неоадъювантного этапа пациенты перенесли операцию по удалению опухоли пищевода, и большинство затем продолжили прием синтилумаба.
Глубокое уменьшение опухолей и обнадёживающая выживаемость
Когда хирурги и патологами исследовали удалённые опухоли, они обнаружили, что предоперационная схема вызвала значительное уменьшение у многих пациентов. Примерно у 42% был отмечен крупный патологический ответ, то есть живая опухолевая ткань оставалась лишь в небольшой части образца. У каждого третьего пациента в основной области опухоли вообще не обнаружили жизнеспособных раковых клеток. По данным сканирования и клинического последующего наблюдения, результаты также были многообещающими: через три года после лечения примерно три из четырёх пациентов жили без признаков рецидива, и почти четыре из пяти были живы. Важно, что побочные эффекты этой усиленной схемы оставались контролируемыми: не было летальных исходов, связанных с лечением, и операция оставалась безопасной и выполнимой.
Как окружение опухоли влияет на ответ
Не все пациенты выиграли в равной степени, поэтому команда задалась вопросом, почему. Они сосредоточились на микроокружении опухоли — сложном сообществе раковых клеток, иммунных клеток и сигнальных молекул. Путём целевых измерений белков в тщательно выделенных образцах опухоли они сравнили тех, кто ответил хорошо, с теми, кто ответил плохо. До лечения было выявлено 14 белков, различавшихся между этими двумя группами. На поверхность выделялся один белок — CD44: опухоли с более высоким уровнем CD44, как правило, лучше реагировали на терапию на основе синтилумаба. После лечения у респондентов снизилось множество белков, связанных с иммунной активностью и репарацией ДНК, что подразумевает, что комбинированная терапия успешно нарушила поддерживающие системы опухоли и перестроила локальную иммунную среду.
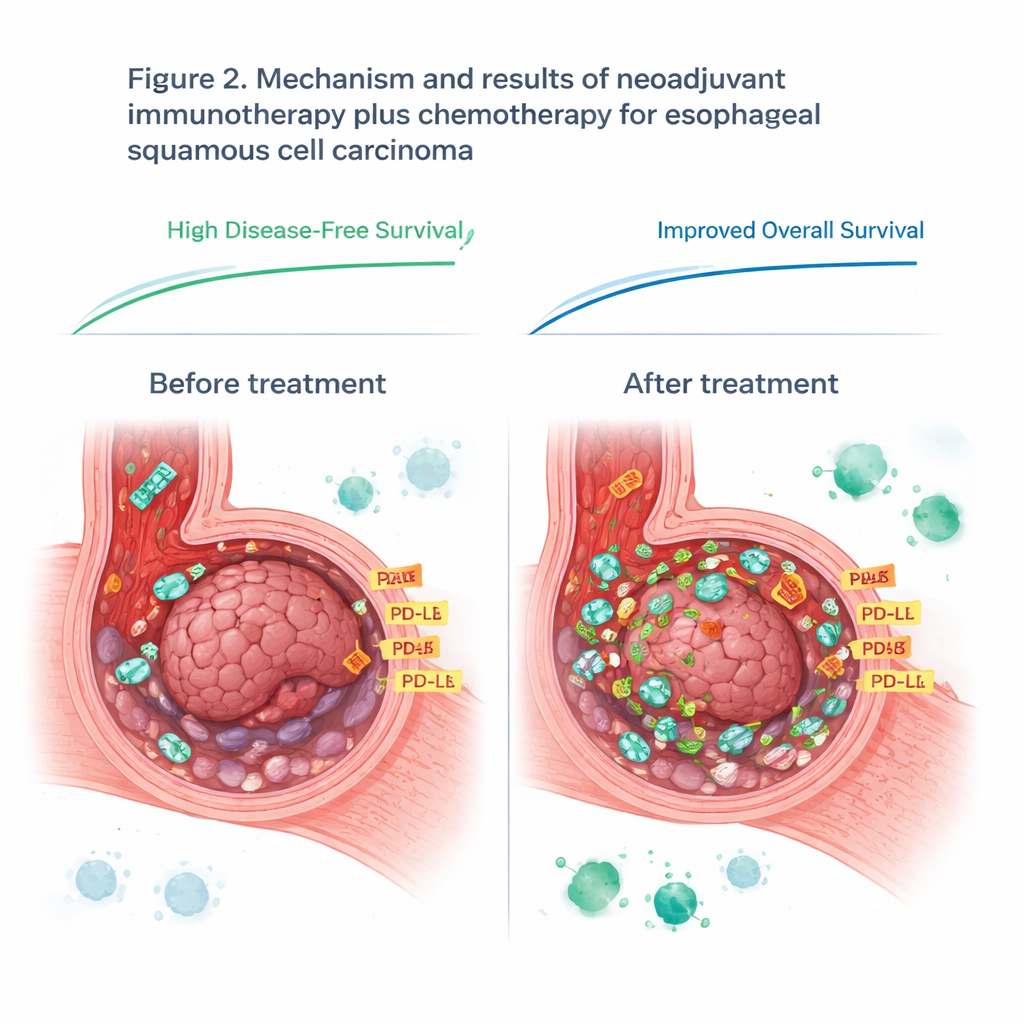
Переосмысление популярного иммунного маркера
Исследование также оценивало PD-L1 — белок, часто используемый как ориентир при выборе пациентов для ингибиторов контрольных точек. До лечения уровни PD-L1 на образцах опухолей не предсказывали, кто будет иметь хороший исход, что ставит под сомнение текущую практику для этого типа рака. Однако в ходе лечения уровни PD-L1 повысились у всех пациентов, вероятно из‑за того, что активированный иммунитет наполнил опухоль воспалительными сигналами. После терапии более высокий PD-L1 в оставшейся ткани опухоли оказался теснее связан с эффективностью иммунотерапии. Это указывает на важность времени: одиночная оценка PD-L1 до лечения может упустить ключевые изменения, разворачивающиеся после включения иммунной системы.
Что это значит для пациентов и будущего
Для людей, стоящих перед операцией при локально распространённом раке пищевода, это исследование несёт две обнадёживающие новости. Во‑первых, комбинация синтилумаба с химиотерапией перед операцией, по-видимому, обеспечивает более глубокое уменьшение опухолей и может повысить шансы на долгосрочную выживаемость, не добавляя опасных побочных эффектов. Во‑вторых, работа показывает, что опухоль и её микроокружение не статичны: они перестраиваются под воздействием терапии и это можно отслеживать по белкам, таким как PD-L1 и CD44. В будущем такие молекулярные «отпечатки» помогут врачам выбирать и корректировать терапию в реальном времени, превращая всё больше «холодных» опухолей, игнорирующих иммунитет, в «горячие», привлекающие мощный и долговременный иммунный ответ.
Цитирование: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Ключевые слова: рак пищевода, иммунотерапия, неоадъювантная терапия, ингибиторы PD-1, микроокружение опухоли