Clear Sky Science · ru
Индивидуализированное лечение с помощью алгоритмов улучшает выживаемость в мышиной модели тройного негативного рака груди
Почему более разумная химиотерапия важна
Химиотерапия спасает жизни, но по-прежнему в основном назначается по принципу «один для всех»: пациенты с похожим раком часто получают одинаковую дозу лекарства по одинаковому графику. Это может приводить к тяжелым побочным эффектам у одних и недостаточной пользе у других. В описанном исследовании поставлен простой, но важный вопрос: что если мы сможем с помощью компьютерных алгоритмов настраивать химиотерапию для каждого пациента в реальном времени, подобно тому как термостат регулирует отопление в доме? На продвинутой мышиной модели агрессивного рака молочной железы исследователи показывают, что такое персонализированное дозирование может продлить выживание и ограничить развитие лекарственной устойчивости.
Проблема стандартных схем противораковой терапии
Сегодня многие пациенты получают максимально переносимую дозу химиопрепарата через фиксированные интервалы. Такая стратегия максимальной переносимой дозы не учитывает, насколько быстро растет конкретная опухоль, как организм пациента перерабатывает препарат и как опухоль меняет ответ на лечение со временем. В результате опухоли могут сначала уменьшаться, а затем возвращаться в виде более устойчивых к лекарствам вариантов, в то время как пациенты страдают от сильных побочных эффектов. Ранние попытки улучшить подход, например «метрономическая» химиотерапия с меньшими, но более частыми дозами, дали неоднозначные результаты в клинических испытаниях и не определили однозначно, как оптимально выбирать дозы и время их введения. Явно необходим более рациональный, индивидуализированный способ планирования химиотерапии.
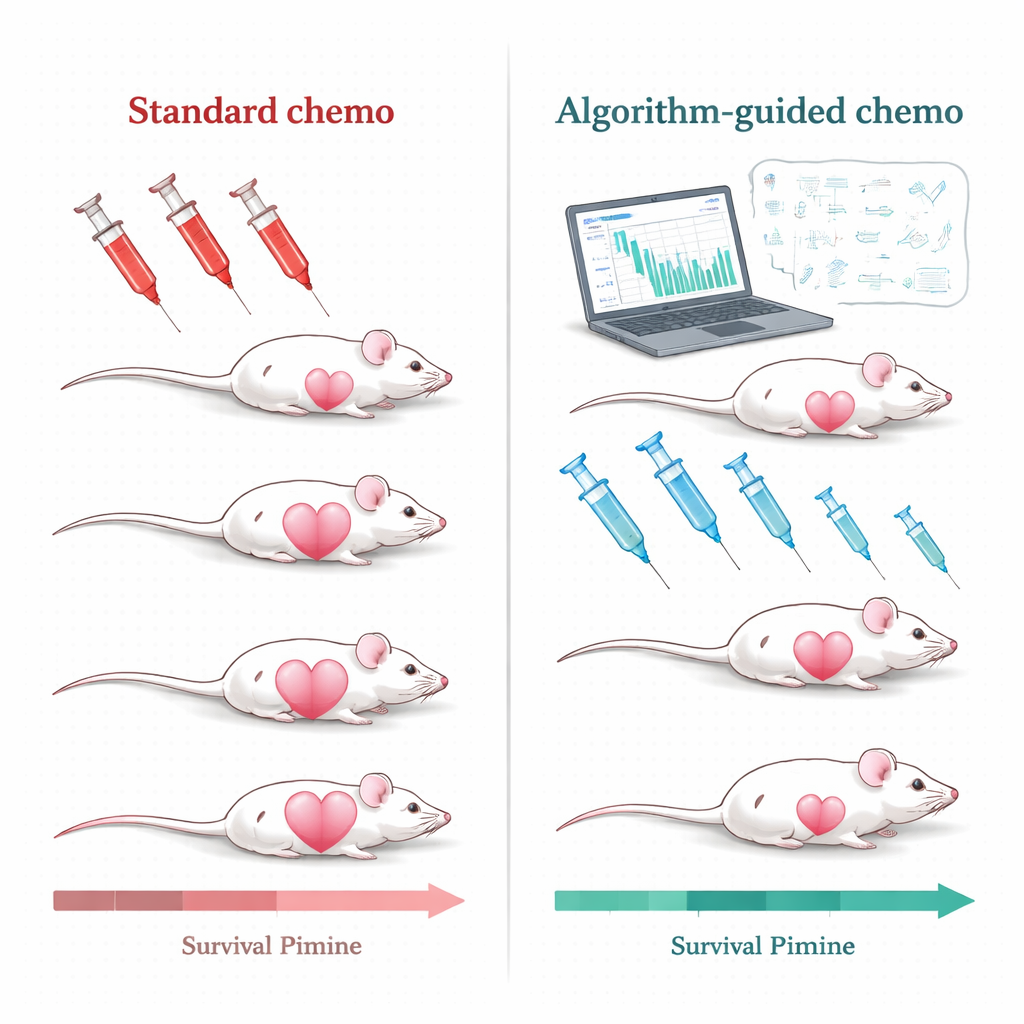
Использование алгоритмов для персонализации лечения
Исследовательская группа решила эту задачу на мышах с опухолями тройного негативного рака молочной железы — формой рака, которая у людей особенно трудно поддается лечению и по-прежнему в основном лечится химиотерапией. Мышам вводили широко используемую форму препарата, пегилированный липосомальный доxorubicin. Вместо повторных высоких доз, назначаемых лишь при росте опухоли до определенного размера, ученые построили математические модели, описывающие рост опухоли, ее регрессию под лечением и фармакокинетику препарата. В модели подавались простые, клинически реалистичные измерения: повторные замеры размера опухоли и уровни препарата в крови. На основе этих входных данных компьютерный алгоритм формировал персонализированные планы лечения для каждой мыши.
Два подхода к помощи со стороны компьютера
В исследовании проверяли два варианта проектирования терапии с помощью алгоритмов. В одном подходе, названном PDPK, компьютер использовал ранние данные для разработки 30‑дневного расписания относительно небольших повторяющихся доз, направленных на поддержание стабильного, но низкого уровня препарата в крови — достаточно высокого, чтобы контролировать опухоль, но достаточно низкого, чтобы ограничить токсичность. Во втором подходе, называемом предиктивным управлением модели (model predictive control), алгоритм обновлял план ежедневно на основе последних измерений опухоли, подбирая размеры доз так, чтобы последовательно снижать объем опухоли. Оба метода опирались на одну основную идею: использовать реалистичную «цифровую копию» мыши с опухолью для моделирования многих возможных схем дозирования и выбирать те, которые с наибольшей вероятностью будут эффективны с учетом ограничений безопасности.
Дольше выживание и меньше лекарственной устойчивости
При сравнении режимов, управляемых алгоритмами, со стандартным протоколом с высокими дозами, вводимыми при росте опухоли, различия оказались впечатляющими. При обычной терапии опухоли часто резко уменьшались сначала, но затем возвращались, а повторные большие дозы способствовали появлению лекарственно-устойчивых форм. Напротив, большинство схем, разработанных алгоритмом, обеспечивали более строгий контроль над опухолями, удлиняли период до рецидива и во многих случаях предотвращали явные признаки устойчивости в течение исследования. В десятках животных как группы PDPK, так и группы с предиктивным управлением демонстрировали значительно более длительное выживание по сравнению со стандартным протоколом, при этом несколько алгоритмических стратегий показали сильные статистически значимые выигрыши по выживаемости.
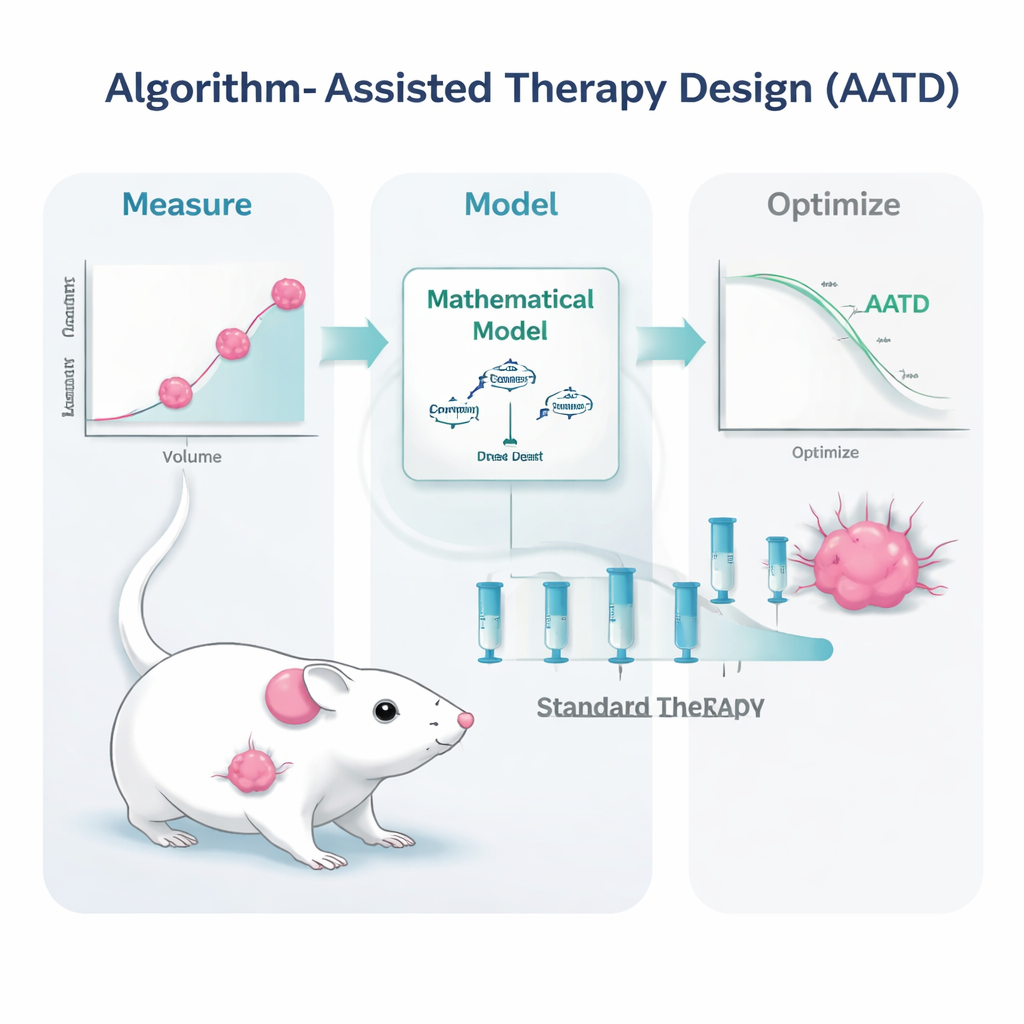
Что это может значить для будущих пациентов
Хотя работа проведена на мышах, ее ключевые составляющие — измерение размера опухоли, мониторинг уровней препарата в крови и запуск компьютерных моделей — уже возможны у людей с использованием современных методов визуализации и лабораторных инструментов. Исследование предлагает, что вместо вопроса «Какова стандартная доза?» врачи в будущем могут спросить: «Учитывая поведение этой конкретной опухоли и то, как пациент обрабатывает препарат, какая доза и когда сейчас будут наиболее эффективны?» Практические препятствия остаются — например, необходимость более частых измерений и логистика гибкого дозирования — но сообщение ясно: химиотерапия не обязана быть грубой и одинаковой для всех. С помощью алгоритмов она может стать более точным, адаптивным инструментом, дающим пациентам лучший шанс на длительный контроль агрессивных опухолей.
Цитирование: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Ключевые слова: персонализированная химиотерапия, тройной негативный рак молочной железы, терапия с поддержкой алгоритмов, математическое моделирование опухоли, дозирование адриамицина