Clear Sky Science · ru
Пространственная транскриптомика выявляет молекулярную гетерогенность и субтип‑специфические терапевтические мишени при мелкоклеточном раке легкого
Почему это исследование рака легкого важно
Мелкоклеточный рак легкого — одна из самых смертоносных форм рака, в основном поражающая людей с историей курения и часто рецидивирующая вскоре после химиотерапии. Врачи знают, что мелкоклеточные опухоли ведут себя по‑разному, но им не хватало инструментов, чтобы увидеть, как разные типы раковых и иммунных клеток расположены внутри каждой опухоли. В этом исследовании использовали новую технологию, которая считывает активность генов в тысячах крошечных участков по срезу опухоли, создавая «молекулярную карту» каждого образца. В сочетании с собственным компьютерным анализом исследователи выявили скрытые паттерны, которые могут указывать на более точные, субтип‑специфические подходы к лечению.
Картирование опухолей in situ
Команда проанализировала опухолевые образцы от 21 пациента с ограниченной стадией мелкоклеточного рака легкого, которые перенесли операцию до получения каких‑либо лекарств. Вместо того чтобы измельчать ткань и терять всю пространственную информацию, они применили пространственную транскриптомику — метод, измеряющий, какие гены включены в многочисленных заданных точках на срезе ткани. Каждая точка сохраняет своё исходное положение, что позволяет связывать активность генов с тем, где физически находятся раковые, нормальные и иммунные клетки. Они добавили два ключевых инструмента: новый показатель «Edgeindex» для количественной оценки глубины инфильтрации опухолевых клеток в соседние ткани и искусственную нейронную сеть — форму машинного обучения — для автоматического пометки точек как опухолевых или не‑опухолевых.
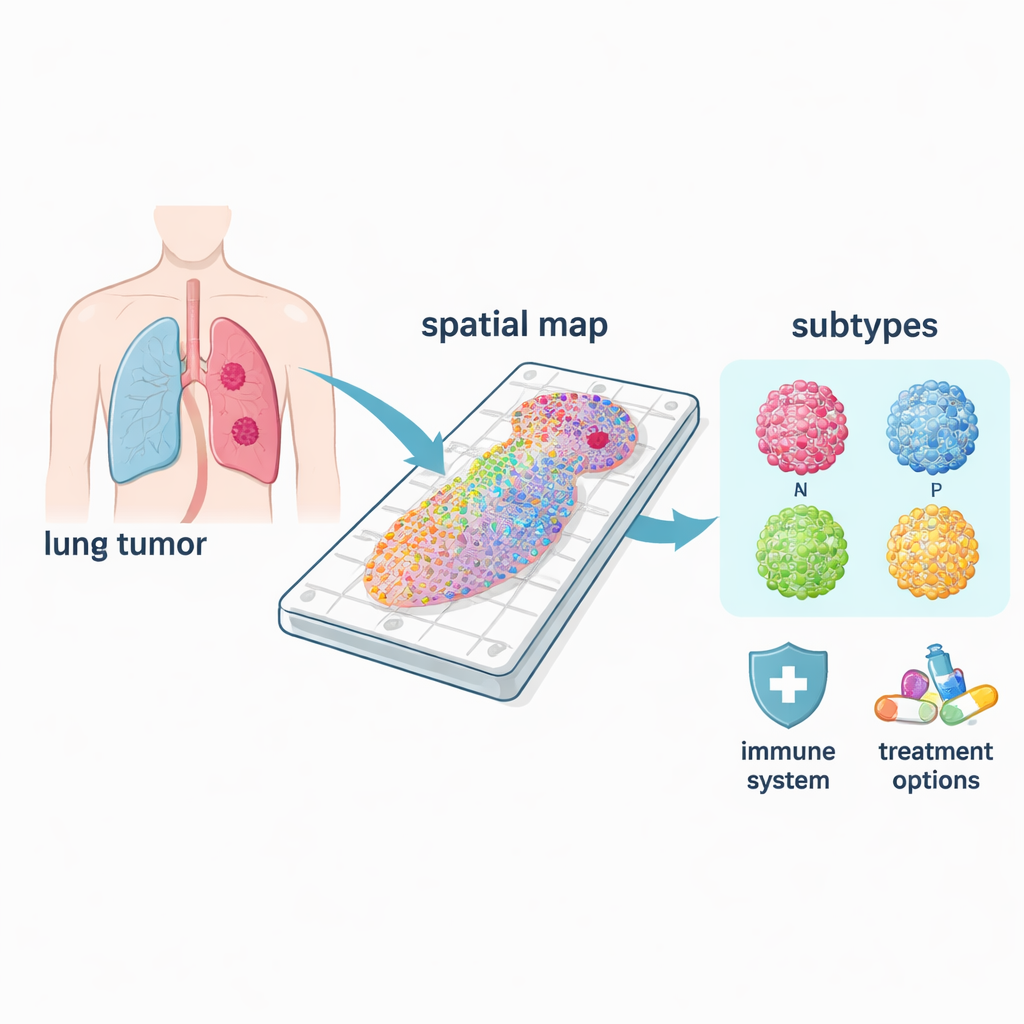
Разные типы рака в одном заболевании
Мелкоклеточный рак легкого — не единое заболевание, а по крайней мере четыре основных молекулярных субтипа, часто называемых ASCL1, NEUROD1, POU2F3 и YAP1, по ключевым регуляторным генам, которые их определяют. С помощью своих пространственных карт исследователи могли видеть, где в опухолях доминирует каждый субтип и чем различается их биология. Распространённые формы ASCL1 и NEUROD1 были тесно связаны с программами деления клеток, что соответствует их репутации высоко пролиферирующих. Напротив, области с POU2F3 ассоциировались с иммунорегулирующими путями, а зоны с YAP1 проявляли сигналы, связанные с метаболизмом и ремоделированием тканей — черты, которые могут быть связаны с метастазированием и устойчивостью к лечению. Поскольку эти паттерны разрешены в пространстве, метод может выявить истинный «ведущий» субтип в смешанной опухоли — то, что часто упускается при анализе гомогенизированного материала.
Инвазивный край и сдвиг иммунитета
Одна из ключевых инноваций исследования, Edgeindex, фиксирует, насколько сильно опухолевые клетки перемешаны с окружающей нетуморной тканью. Низкие значения отражают компактные, чётко ограниченные опухоли, тогда как высокие указывают на рассеянные островки и рваные, инвазивные границы. Опухоли с высоким Edgeindex обогащены генными программами, связанными с внеклеточным матриксом, метастазами и клеточной гибелью. Они также демонстрировали заметно изменённый иммунный ландшафт: меньше помощи со стороны Т‑хелперов и других адаптивных иммунных клеток, но больше врождённых клеток, таких как некоторые натуральные киллеры и моноциты. Авторы интерпретируют это как «перестройку иммунологической ниши», когда опухоль отталкивает точные, направленные иммунные ответы и оставляет менее эффективную, в основном врождённую защиту, неспособную полностью контролировать развитие опухоли.
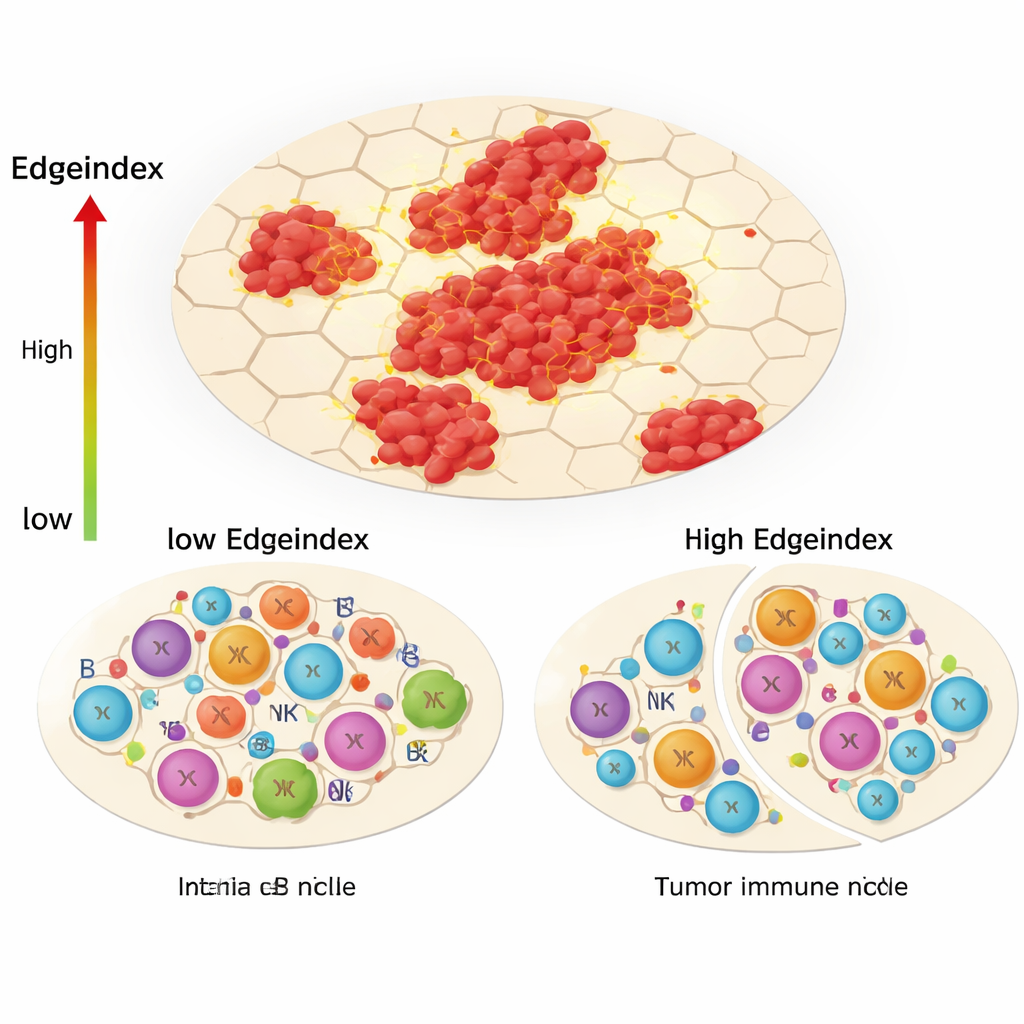
Скрытое разнообразие внутри и вокруг опухолей
Помимо субтипов и паттернов инвазии, пространственные данные показали, что как популяции раковых клеток, так и их окружающие микроокружения внутренне разнообразны. Кластеризуя точки внутри каждой опухоли, команда подсчитала, сколько различных «соседств» по экспрессии генов существовало в раковых областях и в прилегающей нетуморной ткани. Более высокое разнообразие внутри опухоли было связано с иммунными путями, в то время как определённые паттерны в окружающей ткани связывались с активностью клеточного цикла и генетической регуляцией. Исследователи также оценили, насколько интенсивно разные регионы «коммуницируют» с помощью известных сигнальных молекул. Опухоли с более интенсивным общением между регионами, как правило, демонстрировали более выраженные иммунные сигналы, что усиливает идею о тесной пространственной взаимосвязи иммунной активности и роста опухоли.
Прослеживая развитие опухоли во времени
Чтобы приблизительно реконструировать изменения опухолевых клеток по мере прогрессирования заболевания, команда провела анализ «псевдовремени», который упорядочивает клетки вдоль траектории развития на основе их генетической активности. По образцам они неоднократно выделяли один ген, UCHL1, как центральный в этих траекториях. Высокие уровни UCHL1 совпадали с интенсивной активностью клеточного цикла в опухолевых точках, тогда как низкие уровни — с иммунными и путями, связанными с клеточной гибелью. Поскольку UCHL1 — нейроноподобный белок, ранее связанный с агрессивными формами рака легкого, эти находки укрепляют предположение, что он может представлять пригодную для лекарственной мишень, особенно для нейроэндокриноподобных клеток, движущих мелкоклеточный рак легкого.
Что это значит для пациентов
Проще говоря, это исследование превращает плоские микроскопические слайды мелкоклеточного рака легкого в богатые, многоуровневые карты, показывающие, где расположены разные субтипы, насколько агрессивно они инфильтрируют ткани, как они взаимодействуют с окружением и как реагирует или терпит неудачу иммунная система. Новый показатель Edgeindex и метод картирования помогают выявить, какие опухоли особенно инфильтрируют соседние ткани и какие иммунные клетки присутствуют или отсутствуют на границе. Связывая эти пространственные паттерны с уязвимостями, характерными для субтипов — например, препаратами, нацеленными на DLL3, BCL‑2, AURKA, IGF‑1R/PARP или иммунные контрольные точки — работа приближает область к подбору индивидуальной стратегии лечения для каждого пациента. Хотя эти инструменты ещё требуют проверки в крупных исследованиях, они предлагают план действий для более точных и потенциально более эффективных терапий при типе рака, которому остро необходимы лучшие варианты лечения.
Цитирование: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Ключевые слова: мелкоклеточный рак легкого, пространственная транскриптомика, гетерогенность опухоли, иммунная микроокружение опухоли, персонифицированная онкология