Clear Sky Science · ru
К методам оценки микроокружения опухоли для прогнозирования ответа на ингибиторы иммунных контрольных точек
Почему важно предсказывать ответ на противораковую терапию
Ингибиторы иммунных контрольных точек — новый класс противоопухолевых препаратов, который может высвободить собственные защитные силы организма против опухоли и иногда приводить к впечатляющим длительным ремиссиям. Тем не менее лишь часть пациентов получает пользу, тогда как другие испытывают побочные эффекты без значимого улучшения. В этой работе поднят практический вопрос с последствиями для жизни и смерти: можно ли, изучив молекулярный «отпечаток» опухоли и окружающей её ткани, заранее оценить вероятность того, что пациент ответит на такие препараты до начала лечения?
Пульс микроокружения опухоли
Каждая опухоль находится в оживлённом микроокружении из раковых клеток, кровеносных сосудов, иммунных клеток и поддерживающей ткани, совместно называемой микроокружением опухоли. Авторы сосредотачиваются на методах, которые переводят эту сложную среду в числовые «оценки» с помощью измерений активности генов по данным массового РНК‑секвенирования — технологии, показывающей, какие гены включены или выключены в образце опухоли. Они обзорно рассматривают и повторно анализируют 17 таких систем оценок, многие из которых фиксируют разные аспекты иммунного ландшафта — например, число цитотоксических Т‑клеток, состояние активности или истощения иммунных клеток, или сколько «рубцовой» стромальной ткани окружает опухоль. Эти оценки нацелены на прогнозирование, кто ответит на ингибиторы контрольных точек при нескольких типах рака, включая меланому, рак лёгкого, мочевого пузыря, головы и шеи, а также почки.
Как исследование проверяло эти оценки
Для справедливого сравнения методов, разработанных разными группами, авторы собрали данные из нескольких клинических исследований, в которых пациенты получали ингибиторы иммунных контрольных точек и у них выполняли РНК‑секвенирование опухолей. Они сформировали большие объединённые наборы данных — например, объединив четыре исследования по меланоме и несколько смешанных когорт по разным опухолям — а также анализировали отдельные типы рака по отдельности. Поскольку в разных исследованиях использовались слегка разные лабораторные протоколы, сначала скорректировали «эффекты партии», чтобы технические различия не маскировались под биологию. Затем для каждой оценки задали два основных вопроса: насколько хорошо она отличала ответивших от неответивших и насколько точно предсказывала продолжительность жизни пациентов после лечения?
Что сработало, что помогло и где были провалы
Анализ показал одновременно трезвую и познавательную картину. Некоторые оценки работали достаточно хорошо в конкретных условиях: например, меры цитолитической, то есть убивающей клетки, активности Т‑лимфоцитов (обозначенные CYT1 и CYT2) и сосредоточенная на дисфункции оценка TIDE оказались особенно информативны для меланомы. Простое отношение двух генов, отражающее поведение макрофагов и известное как CS Polarity, лидировало в большой смешанной группе опухолей, тогда как сигнатура «горячей опухоли» TIP Hot систематически оказывалась полезной в нескольких типах, особенно при раке мочевого пузыря, лёгкого и головы и шеи. Другая оценка, IS_immune, отражающая общую иммунную активность, хорошо прогнозировала выживание как при раке мочевого пузыря, так и в более широкой неиммунотерапевтической выборке TCGA. Однако при сравнении всех оценок бок о бок их способность предсказывать ответ или выживание в целом оказалась умеренной, и ни один метод не был надёжно сильным во всех типах рака.
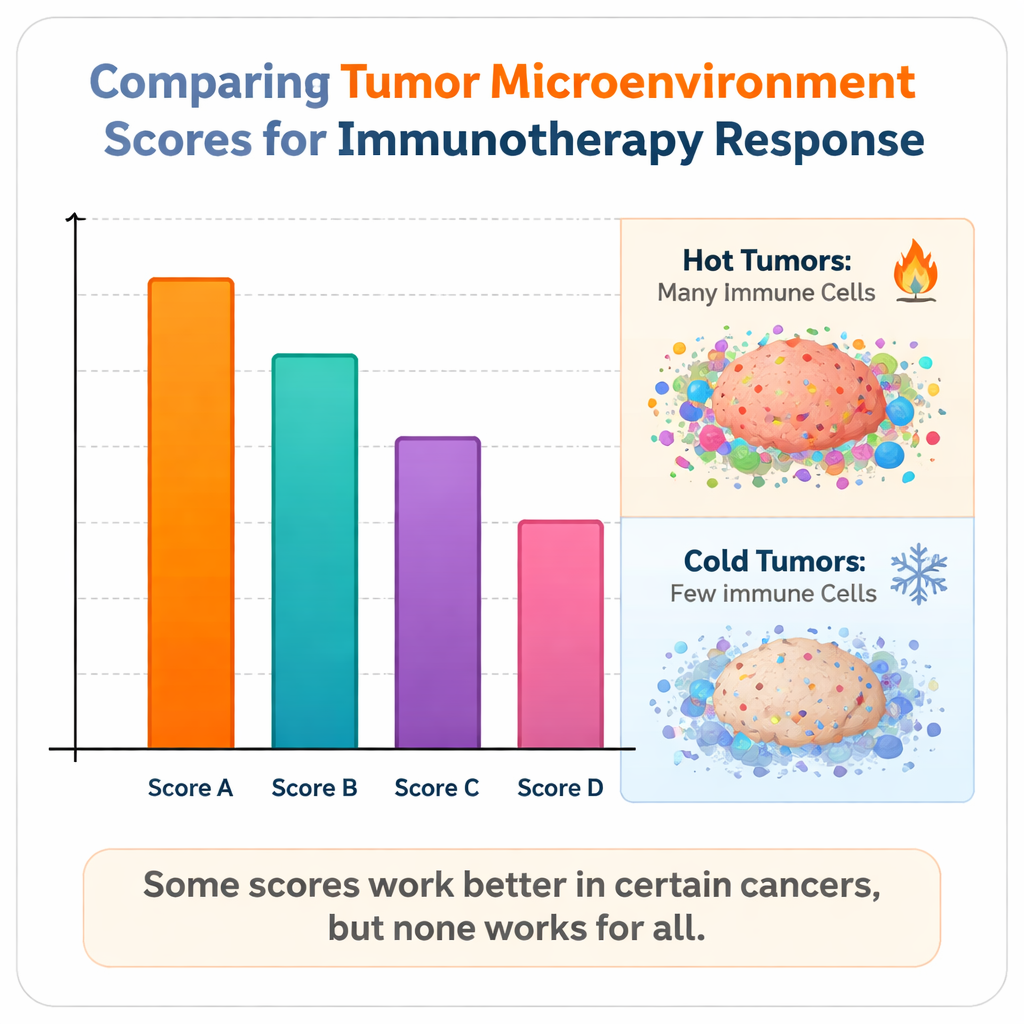
«Горячие» и «холодные» опухоли и пределы существующих оценок
Авторы обнаружили, что оценки лучше работают в так называемых «горячих» опухолях — уже инфильтрованных множеством активных иммунных клеток, например меланоме, некоторых опухолях лёгкого, раке головы и шеи и уротелиальном (мочевом) раке. Напротив, в «холодных» опухолях, как многие раки почки, где иммунные клетки редки или подавлены, все существующие оценки испытывали трудности. Даже когда некоторые меры показывали статистические различия между ответившими и неответившими, их практическая прогностическая сила оставалась слабой. Исследование также подчёркивает, почему узкие сигнатуры могут давать сбой: оценки, построенные вокруг одного типа клетки или пути, могут пропустить важные контекстные факторы, например истощение Т‑клеток или механизмы, которыми опухоль блокирует их работу. С другой стороны, крайне большие сложные модели рискуют переобучиться и давать плохие результаты на новых группах пациентов.
Что это значит для пациентов и дальнейших исследований
Для пациентов и клиницистов главное — осторожный оптимизм. Оценки микроокружения опухоли уже улавливают значимые биологические сигналы, и некоторые — такие как TIP Hot, CS Polarity, TIDE и IS_immune — демонстрируют потенциал для отдельных типов рака. Но они ещё недостаточно точны или универсальны, чтобы служить самостоятельными тестами для принятия решения о назначении ингибиторов иммунных контрольных точек. Авторы утверждают, что дальнейший прогресс потребует больших и более разнообразных наборов данных, более умных способов снижения размерности геномных данных, лучшей интеграции клинических факторов и других биомаркеров (например, анализов крови и данных о микробиоме), а также моделей, учитывающих эволюцию опухолей во времени. При таких усовершенствованиях оценка микроокружения опухоли может стать мощным инструментом для подбора подходящей иммунотерапии и избавления других пациентов от неэффективного лечения.
Цитирование: Zhou, Q., Kirshtein, A. & Shahriyari, L. Towards the tumor microenvironment scoring methods for immune checkpoint inhibitor response. npj Precis. Onc. 10, 88 (2026). https://doi.org/10.1038/s41698-025-01221-z
Ключевые слова: микроокружение опухоли, ответ на иммунотерапию, ингибиторы контрольных точек иммунитета, оценки по экспрессии генов, «горячие» и «холодные» опухоли