Clear Sky Science · ru
Целевая иммунотерапия и наномедицина при раке яичников: путь вперёд
Почему это важно для женского здоровья
Рак яичников — один из самых смертельных онкологических заболеваний у женщин, во многом потому, что его часто обнаруживают на поздних стадиях и лечат агрессивными, неспецифичными препаратами. В этом обзоре рассматривается, как новое поколение иммунных подходов и крошечные магнитные частицы — магнитные наночастицы — могут преобразить лечение рака яичников: сделать его точнее, более персонализированным и в конечном счёте эффективнее при меньшем числе побочных эффектов.
Сложности обнаружения и лечения рака яичников
Рак яичников часто развивается «тихо». Ранние симптомы расплывчаты — вздутие, лёгкие боли в животе — и стандартные методы визуализации, такие как УЗИ, КТ и МРТ, могут пропустить маленькие или ранние опухоли, скрытые глубоко в брюшной полости. К моменту постановки диагноза у многих пациентов заболевание уже распространилось по брюшине, что усложняет хирургическое вмешательство и увеличивает риск рецидива. Химиотерапия и таргетные препараты помогают, но повреждают и здоровые ткани, а опухоли нередко вырабатывают механизмы ускользания от их действия. Эти ограничения подтолкнули исследователей к поиску более умных способов обнаружения и уничтожения клеток рака яичников.
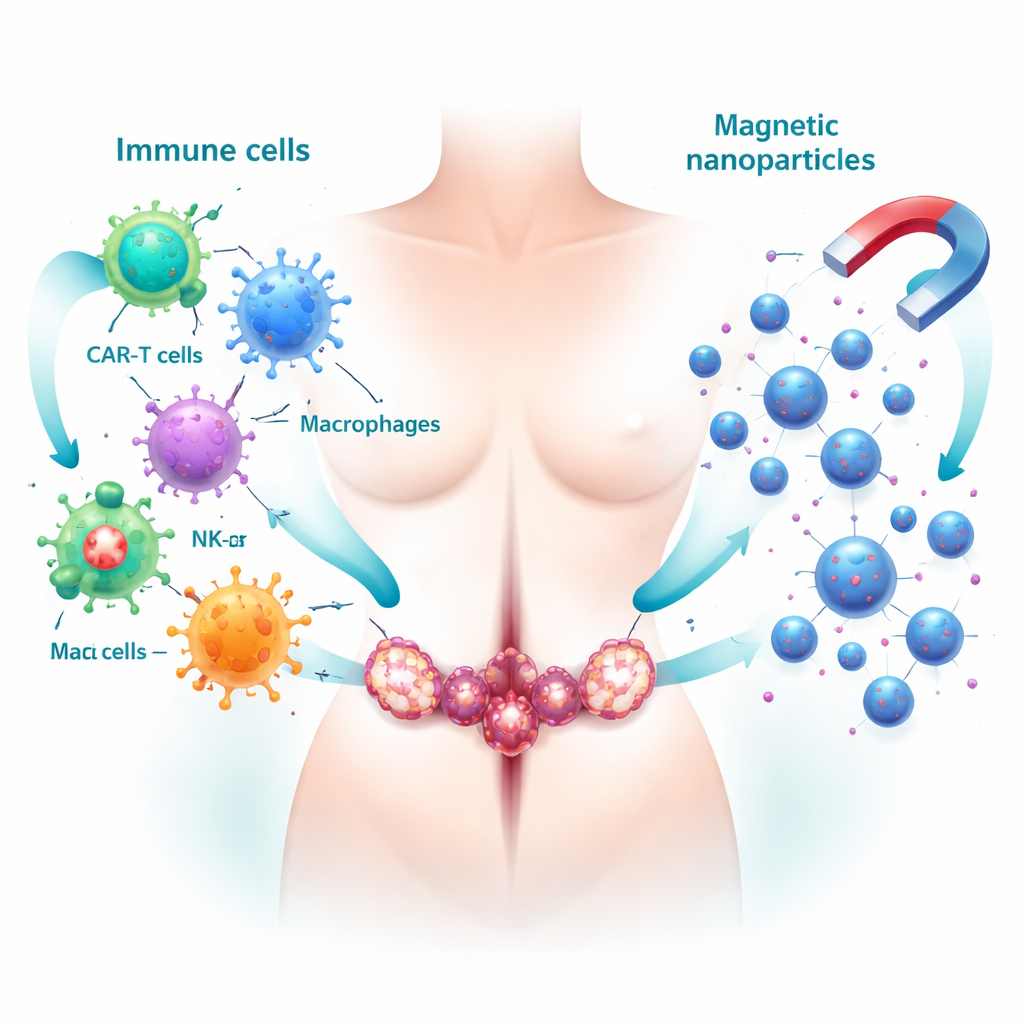
Обучение иммунной системы охоте на опухоли
Одна из ключевых стратегий — использовать собственные защитные силы организма. Специально модифицированные Т‑лимфоциты, известные как CAR‑T‑клетки, создают в лаборатории для распознавания маркеров, присутствующих преимущественно на клетках рака яичников. Вернувшись в организм пациента, они могут целенаправленно находить и уничтожать эти клетки. Естественные киллеры (NK‑клетки) дают ещё одну линию защиты: их можно расширять или генетически настраивать для лучшего распознавания опухолей, и они становятся ещё эффективнее в сочетании с таргетными антителами или ингибиторами контрольных точек, снимающими «тормоза» с иммунного ответа. В то же время обзор подчёркивает тёмную сторону опухолевого микроокружения: опухолеассоциированные макрофаги — тип иммунных клеток, которые часто перепрограммируются так, что защищают, а не борются с опухолью. Обратное перепрограммирование или «перевоспитание» этих клеток в борцов с опухолью становится многообещающим путём повышения эффективности иммунотерапии.
Магнитные наночастицы как интеллектуальные инструменты против рака
Второй столп обзора — наномедицина, особенно магнитные наночастицы на основе железосодержащих материалов. Благодаря чувствительности к магнитному полю и хорошей визуализации на МРТ они могут выступать в роли крошечных управляемых инструментов внутри организма. Покрытые на поверхности молекулами, распознающими маркеры рака яичников, такие частицы могут нацеливаться на опухоли и доставлять химиопрепараты непосредственно в них, значительно повышая концентрацию лекарства в опухоли и уменьшая нагрузку на здоровые органы. Под переменным магнитным полем те же частицы безопасно нагревают опухоль до примерно 42–45 °C — достаточно для ослабления или уничтожения раковых клеток и повышения их чувствительности к стандартным препаратам, но недостаточно для серьёзного повреждения окружающих нормальных тканей.
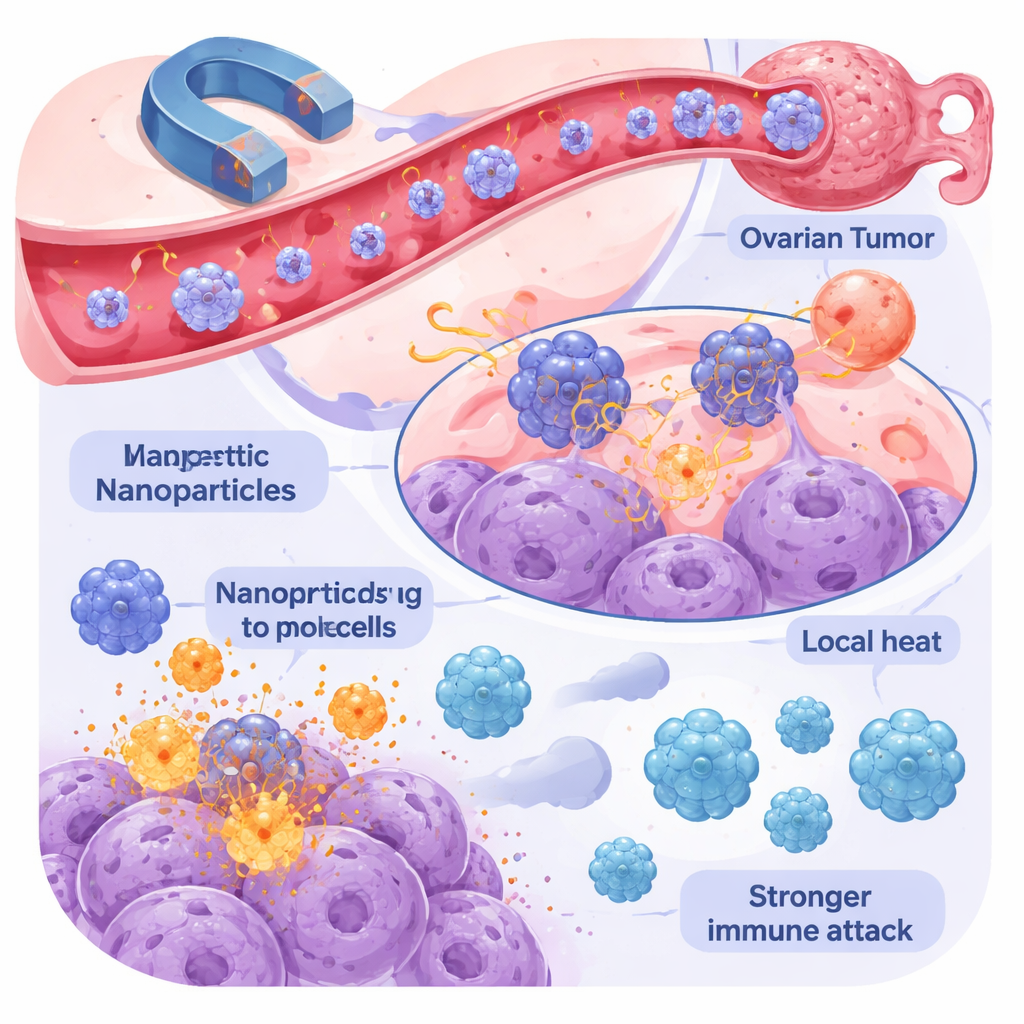
Сочетание тепла, лекарств и иммунитета
Настоящее воодушевление вызывает объединение иммунотерапии и магнитной наномедицины. Когда магнитные наночастицы доставляют препараты, генерируют тепло или помогают разрушать опухоль, гибель раковых клеток сопровождается выбросом «сигналов опасности» и фрагментов опухоли в местной среде, фактически превращая опухоль в собственную вакцину. Это привлекает и активирует Т‑клетки и NK‑клетки, облегчая действие ингибиторов контрольных точек и терапий на основе CAR‑клеток. Исследователи также используют наночастицы для транспортировки иммуномодулирующих молекул и антител прямо в опухоль, повышая их локальную концентрацию и снижая системные побочные эффекты. Ранние исследования на животных показывают более резкое сокращение опухолей, меньше рецидивов и более активную инфильтрацию иммунных клеток при комбинированном использовании этих подходов.
Препятствия, безопасность и перспективы
Несмотря на достигнутый прогресс, остаётся много проблем. Опухоли яичников часто имеют очаговый и рассеянный характер в брюшной полости, что затрудняет равномерное распределение наночастиц, а неразлагаемые частицы могут накапливаться в органах, таких как печень, если их конструкция не продумана. Плотные рубцовые ткани вокруг опухолей могут препятствовать глубокому проникновению. Обзор рассматривает инженерные приёмы — биоразлагаемые покрытия, маскировку «своими» клеточными мембранами и ферменты, размягчающие барьеры опухоли — которые повышают безопасность, точность нацеливания и выведение частиц. Также подчёркивается важность индивидуализации терапии с учётом генетики и иммунного профиля пациента и использование передовой визуализации для контроля местоположения наночастиц и оценки их эффективности.
Что это может значить для пациентов
Практически, описанная в обзоре работа указывает на будущее, в котором рак яичников будет обнаруживаться раньше и лечиться более бережно, но эффективнее. Магнитные наночастицы смогут направлять лекарства и тепло точно туда, где это необходимо, а иммунные терапии обеспечат продолжительную системную атаку на оставшиеся раковые клетки. Если предстоящие клинические испытания подтвердят обещающие результаты лабораторных и животных исследований, пациентки с раком яичников могут получить доступ к методам лечения, которые будут более целенаправленными, персонализированными и гораздо менее изнуряющими по сравнению с нынешними стандартами.
Цитирование: Li, Y., Dou, J., Fu, Y. et al. Targeted immunotherapies and nanomedicines for ovarian cancer: the way forward. npj Precis. Onc. 10, 80 (2026). https://doi.org/10.1038/s41698-025-01204-0
Ключевые слова: рак яичников, иммунотерапия, наномедицина, магнитные наночастицы, целенаправленная доставка лекарств