Clear Sky Science · ru
Методы рандомизированной, слепой, контролируемой оценки предполагаемых вмешательств при заболеваниях в многолабораторных доклинических сетях
Почему это важно для повседневного здоровья
Многие многообещающие медицинские методы выглядят эффективными в исследованиях на животных, но затем терпят неудачу в крупных дорогостоящих клинических испытаниях. В этой работе подробно показано, как учёные могут перестроить ранние испытания на животных так, чтобы их результаты были более надёжными и с большей вероятностью предсказывали поведение у реальных пациентов — в качестве примера использован инсульт. 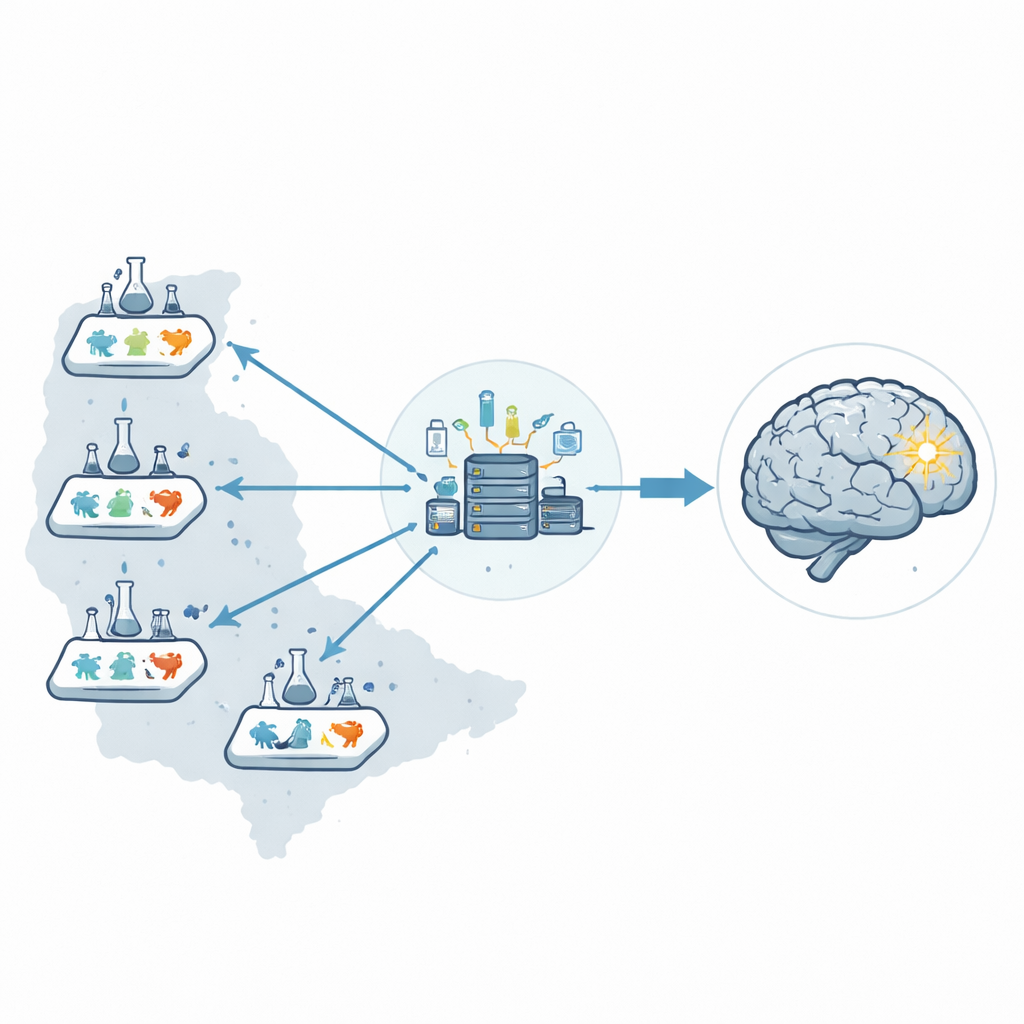
Создание сети вместо одной лаборатории
Вместо того чтобы полагаться на одну лабораторию, исследователи создали шестилaborаторную доклиническую сеть по всей территории США, названную Stroke Preclinical Assessment Network. Центральный координационный центр управлял всей операцией: отправкой кодированных флаконов с препаратами, случайным назначением лечения, приёмом всех данных и проведением статистики. Разделив эти роли и отстранив их от людей, выполнявших операции или оценку исходов, они снизили вероятность того, что человеческие ожидания могут тонко повлиять на результаты.
Воплощение справедливости и сокрытия информации на практике
Чтобы имитировать правила хорошего клинического испытания, каждое животное регистрировалось, маркировалось и отслеживалось с момента поступления в лабораторию. Лечения хранились в идентичных флаконах, чтобы хирурги не могли отличить реальные препараты от плацебо во время индуцирования инсульта и введения терапии. Структурированный план рандомизации обеспечивал равномерное распределение по группам лечений с учётом самцов и самок, различных моделей инсульта и всех шести площадок. Даже если животное погибало или процедура не удавалась, оно оставалось в учёте, чтобы потери нельзя было тихо игнорировать, что помогало избежать скрытых смещений.
Испытание препаратов в реалистичных моделях инсульта
Сеть использовала пять различных моделей грызунов, которые вместе отражали важные аспекты человеческого инсульта, включая возраст, высокое кровяное давление и ожирение, вызванное диетой. Инсульт индуцировали одинаковым образом на всех площадках — кратковременно блокируя крупную мозговую артерию с последующим восстановлением кровотока — аналогично современным процедурам удаления тромба у людей. Животным давали одно из шести кандидатов на защитное средство или соответствующий контроль. Команда затем наблюдала за ними с помощью простых тестов подвижности, таких как поворот в углу или ходьба по решетке, а также делала сканы мозга для измерения объёма поражения в течение 30 дней.
Слепая оценка, общий доступ к данным и продуманная статистика
Чтобы сохранить беспристрастность суждений, поведенческие тесты записывали на видео и загружали в центральный архив. Эти видео, лишённые любой идентифицирующей информации, отправлялись обученным оценщикам в других лабораториях, которые проводили оценки, не зная, какое лечение получило животное и где оно было исследовано. Магнитно-резонансные изображения обрабатывались автоматизированным аналитическим конвейером, который сегментировал мозг и область поражения с минимальным участием человека. Все результаты поступали в многоармную, многоступенчатую статистическую схему, позволявшую тестировать несколько препаратов параллельно: слабые или явно неэффективные кандидаты могли отбраковываться на ранних этапах, в то время как перспективные продолжали проверку на последующих стадиях. 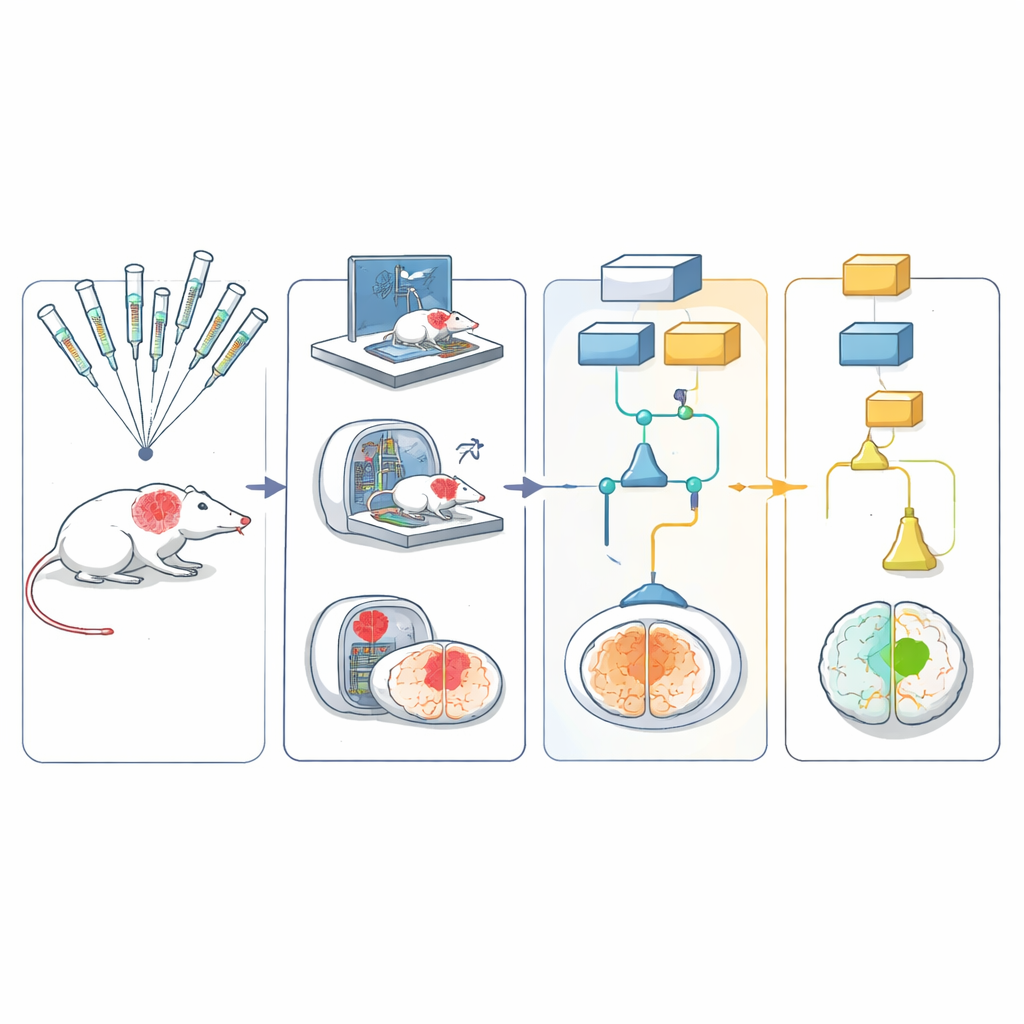
Что показали результаты о терапиях при инсульте
На протяжении четырёх этапов и 2615 животных система показала свою работоспособность даже в условиях перебоев, вызванных пандемией COVID-19. Методы последовательно обеспечивали баланс между группами лечения, минимизировали ошибки в дозировании и демонстрировали улучшение качества данных по мере того, как площадки набирали опыт. В итоге пять из шести препаратов были исключены, тогда как один — мочевая кислота, ловушка для свободных радикалов — достиг заранее запланированного критерия пользы. Одновременно работа выявила ограничения некоторых популярных моделей, например очень высокую смертность среди старых мышей, что указывает на то, что они могут быть непрактичны или нереалистичны для будущих исследований.
Общая картина: шаблон для более надёжной доклинической науки
Для непрофессионального читателя ключевое послание таково: то, как мы испытываем препараты на животных, так же важно, как и то, что мы испытываем. Перенесши меры предосторожности современных клинических испытаний — рандомизацию, слепость, полный учёт каждого субъекта и тщательную статистику — в исследования на животных, эта сеть показала, что ранние исследования могут быть одновременно более строгими и более эффективными. Подробная инструкция, которую они предоставляют, может быть адаптирована для других болезней, предлагая путь к лабораторным результатам, которые выдерживают репликацию и дают врачам, пациентам и донорам больше уверенности в том, что терапия действительно имеет шанс сработать в клинике.
Цитирование: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Ключевые слова: инсульт, доклинические исследования, модели животных, строгость исследований, многоцентровые исследования