Clear Sky Science · ru
Трансгенез, опосредованный PiggyBac, и нокауты CRISPR–Cas9 у большой восковой моли Galleria mellonella
Крошечная гусеница с большим медицинским потенциалом
Представьте проверку новых антибиотиков или изучение опасных инфекций без использования мышей или других млекопитающих. Личинки большой восковой моли, Galleria mellonella, становятся доступной и этически приемлемой альтернативой для таких экспериментов. В этом исследовании показано, как учёные сделали важный шаг вперёд, предоставив этим гусеницам те же генетические инструменты, которые сделали дрозофилу и данио рерио такими ценными для биомедицинских исследований.
Почему этот насекомое важно для здоровья человека
Личинки Galleria mellonella удивительно хорошо имитируют реакцию организма человека на патогены. Их можно содержать при 37 °C — температуре человеческого тела — и инфицировать широким спектром медицински значимых бактерий и грибов. При заболевании тела личинок темнеют в процессе, называемом меланизацией, что даёт исследователям наглядный показатель состояния здоровья. Так как они являются беспозвоночными, использование этих личинок обходится без многих юридических и этических ограничений, применимых к позвоночным, и они недороги в массовом разведении. Кроме того, у личинок обнаружена способность разлагать обычные пластики, что открывает возможности и для экологических исследований.
Отсутствовавший генетический набор инструментов
Несмотря на эти преимущества, у личинок восковой моли отсутствовали те же сложные генетические приёмы, которые есть у классических лабораторных животных. За последнее десятилетие несколько групп секвенировали геном моли и каталогизировали активные гены и белки, но исследователям по‑прежнему было трудно включать или выключать гены или добавлять полезные маркеры. Этот пробел ограничивал возможности модели — например, создание животных, которые светятся при инфицировании, или удаление конкретных генов для проверки их роли в иммунитете. Настоящая работа решает эту проблему, адаптировав для Galleria mellonella две мощные системы генной инженерии, известные как PiggyBac и CRISPR–Cas9.
Создание репортерных личинок, светящихся в темноте
Исследователи сначала изучили тайминг раннего эмбрионального развития моли и обнаружили примерно шестичасовое окно после откладки яиц, когда все делящиеся ядра ещё разделяют общий цитоплазматический объём. Введение ДНК в этот период позволяет новому генетическому материалу попадать во все последующие ткани, включая будущие сперму и яйцеклетки. Используя это окно, авторы ввели конструкты ДНК на основе транспозона PiggyBac — «вырезай‑и‑вставь» элемент, который может интегрировать крупные фрагменты ДНК в геном. После тестирования разных вспомогательных плазмид они выявили вариант с гиперактивным ферментом PiggyBac, который успешно дал трансгенные линии. Эти личинки экспрессировали зелёные и красные флуоресцентные белки в разных тканях, а анализ ДНК показал, что вставленная кассета оказалось в безвредном регионе между эндогенными генами.
Наблюдение за клетками и нокауты генов
Далее авторы создали более специализированные репортерные линии. Одна конструкция пометила структурный белок тубулин зелёной флуоресценцией, чтобы подсветить внутреклеточный «скелет», а другая слила красный маркер с гистоном — белком, упаковывающим ДНК в ядре. Эти линии светились характерными узорами в кишечнике, жировом теле, шелковых железах и других тканях, позволяя визуализировать структуры клеток в живых или фиксированных личинках. Чтобы не просто добавлять гены, но и отключать их, команда применила CRISPR–Cas9. Они вводили заранее собранные белково‑РНК комплексы CRISPR, нацеленные на зелёный флуоресцентный маркер, в эмбрионы, уже несущие репортерную кассету. Многие потомки показали частичную или полную потерю зелёного сигнала при сохранении красного свечения глаз, а секвенирование ДНК подтвердило небольшие вставки и делеции в заданном месте разреза CRISPR.
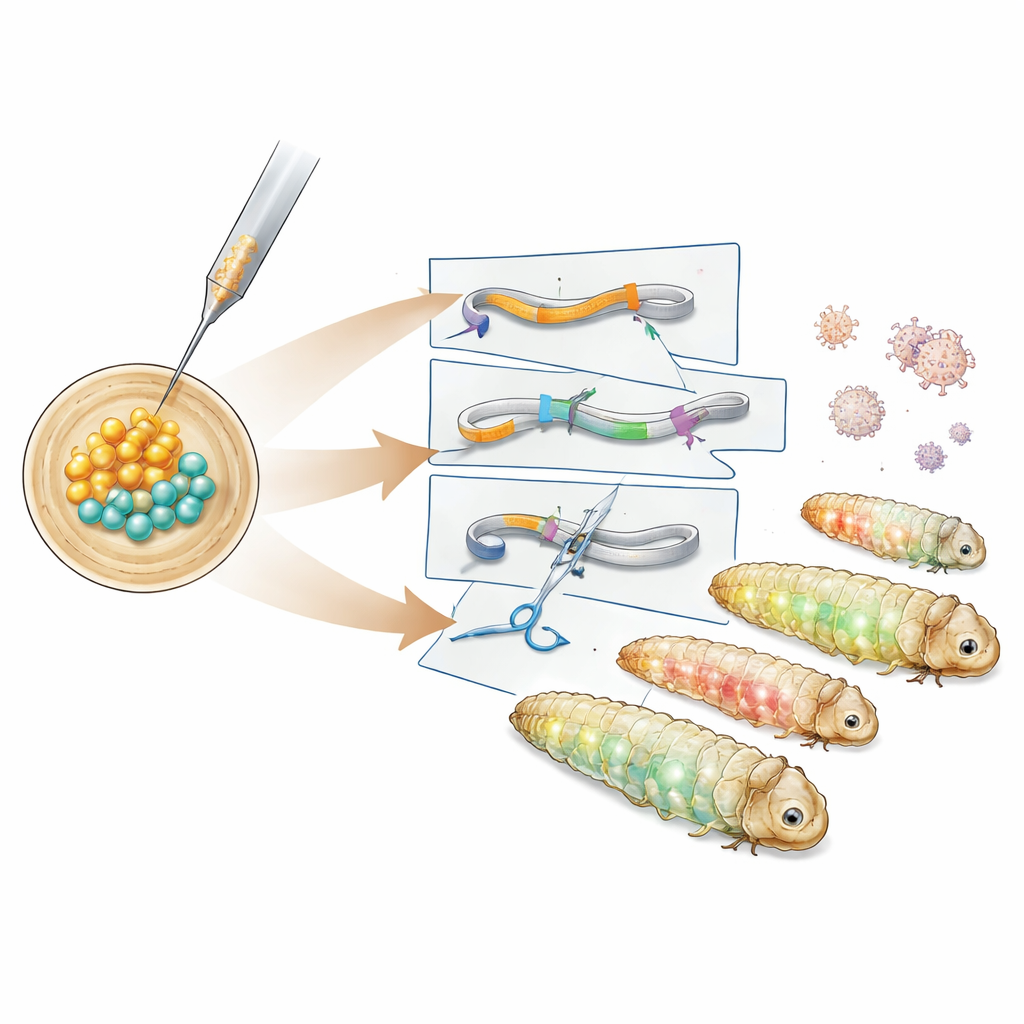
От технического достижения к практическому воздействию
Хотя эффективность как PiggyBac, так и CRISPR в этих мольях пока скромнее, чем у некоторых других насекомых, авторы описывают очевидные пути для улучшения — настройку промоторов, вариантов ферментов и стратегий инъекций. Даже в нынешнем виде набор инструментов достаточно силён, чтобы создавать стабильные линии, визуализирующие ключевые клеточные компоненты или несущие целевые генетические нокауты. Для неспециалистов главное: Galleria mellonella теперь можно генетически модифицировать почти с той же гибкостью, что и более известные лабораторные животные. Это означает, что исследователи могут создавать гусениц, которые сигнализируют об инфекции, моделируют аспекты человеческих болезней или тестируют новые препараты быстрее, дешевле и гуманнее, что потенциально уменьшит зависимость от млекопитающих моделей в исследовании инфекционной биологии и смежных областях.
Цитирование: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Ключевые слова: Galleria mellonella, модель инфекции у беспозвоночных, генетическая инженерия, трансгенез PiggyBac, CRISPR‑нокауты