Clear Sky Science · ru
Таргетирование опухолевого экспрессируемого EGFR гуманизированным моноклональным антителом
Поиск скрытых флагов рака
Лечение рака часто сталкивается с задачей найти баланс между атакой по опухолевым клеткам и сохранением здоровых тканей. В этой работе описано новое лабораторно созданное антитело A10, которое умеет отличать раковые клетки, несущие особую форму рецептора фактора роста, от нормальных клеток. Фокусируясь на конформации, которая появляется преимущественно тогда, когда этот рецептор изменён или чрезмерно сконцентрирован на опухолевых клетках, A10 открывает путь к терапии, одновременно мощной и более избирательной, чем многие существующие варианты.
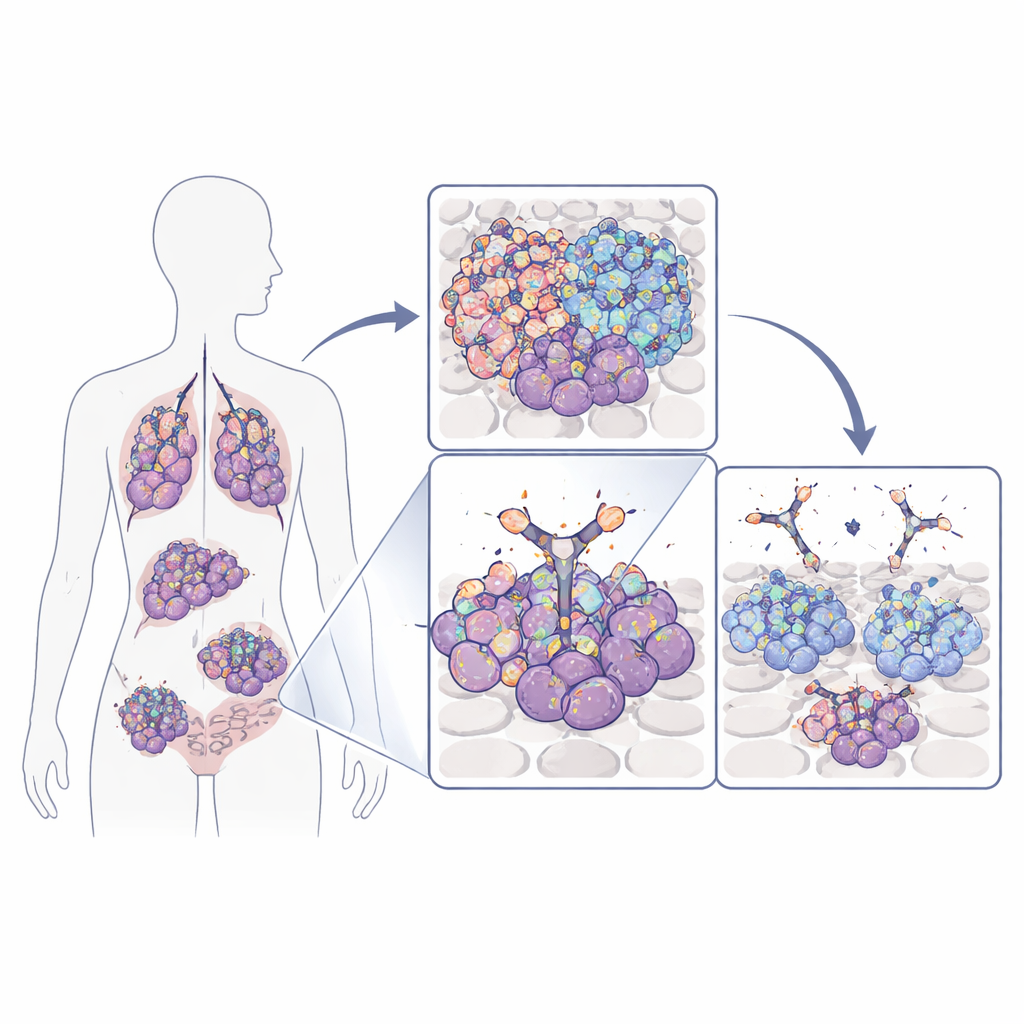
Почему этот переключатель роста важен
Многие опухоли, включая агрессивные формы мозга, лёгких, молочной и толстой кишки, зависят от поверхностного белка — рецептора эпидермального фактора роста (EGFR) — для роста и выживания. Опухолевые клетки могут усиливать этот рецептор путём амплификации гена, его мутаций или производства укороченной постоянно активной формы, известной как EGFRvIII. Стандартные препараты, блокирующие EGFR, часто поражают и раковые, и нормальные ткани, поскольку распознают участки рецептора, присутствующие везде. Авторы работы вместо этого сосредоточились на небольшом петлеобразном участке EGFR, который становится явно доступным преимущественно на раковых клетках — либо потому, что EGFR присутствует в аномально больших количествах, либо потому, что рецептор укорочен в EGFRvIII. Эта петля действует как опухоле‑специфический «флаг», на который, в принципе, можно нацеливаться намного безопаснее.
Превращение мышиного антитела в человеческое лекарство
Ранее исследователи обнаружили мышиное антитело 40H3, которое распознавало эту выставленную петлю на экспрессируемом в опухоли EGFR. Однако мышиные антитела могут вызывать иммунные реакции при повторном введении пациентам. Чтобы избежать этого, команда использовала методы белкового инжиниринга, пересадив ключевые сегменты связывания 40H3 на человеческие каркасы антител, получив четырнадцать «гуманизированных» кандидатов и один химический референсный молекулу. При тестировании этих вариантов на клетках, сверхэкспрессирующих EGFR, три версии связывались особенно хорошо, а одна — A10 — выделялась как сильнейший связывающий вариант, при этом игнорируя нормальные клетки с умеренным уровнем EGFR. На широкой панели опухолевых клеточных линий с разными мутациями и копийностью EGFR, A10 последовательно показывала более высокое связывание, чем исходное мышиное антитело, и сохраняла сильное предпочтение к злокачественным клеткам.
Как антитело захватывает свою мишень
Чтобы понять, почему A10 столь селективна, команда получила высокоразрешающую трёхмерную структуру активной части антитела в комплексе с петлёй EGFR. Петля складывается в тугую шпильку, стабилизированную дисульфидным мостиком, а A10 обхватывает эту форму в бороздке, образованной между её двумя «руками», с многочисленными заряженными контактами, фиксирующими её на месте. Сравнение этой структуры с известными конформациями полного молекулы EGFR выявило ключевое наблюдение: как в неактивной «связанной» форме, так и в активной димерной форме нормального EGFR петля в основном скрыта или частично экранирована соседними доменами. Это означает, что A10 не может легко достичь своего сайта связывания на типичных рецепторах с умеренной экспрессией. Напротив, в опухоле‑специфическом варианте EGFRvIII передняя часть рецептора отсутствует, оставляя петлю сильно открытой и доступной. Данные указывают, что A10 в основном распознаёт EGFR в определённых переходных конформациях и в переполненных или укороченных формах, которые преимущественно встречаются на опухолевых клетках.
Вооружение антитела для уничтожения опухолевых клеток
Распознавание опухолевого флага полезно само по себе, но исследователи пошли дальше и превратили A10 в конъюгат антитело‑лекарство (ADC). Они химически прикрепили мощное цитотоксичное соединение монометил-ауристатин E (MMAE) к A10 с помощью линкера, который разрушается внутри клеток. Этот конъюгат A10‑MMAE связывался с раковыми клетками так же хорошо, как и неконъюгированное антитело. В лабораторных тестах на множестве клеточных линий ADC оказывался наиболее эффективным против опухолей с очень высоким уровнем EGFR или EGFRvIII, где у A10 было много участков связывания. В таких клетках крошечные количества конъюгата были достаточны для индукции гибели клеток. Клеточные линии опухолей с меньшим числом целей для A10 или с врождённой устойчивостью к MMAE были менее подвержены эффекту, а нормальные фибробласты с дикой формой EGFR оставались невредимыми, несмотря на чувствительность к свободному MMAE. Результаты показывают, что сочетание селективного связывания и высвобождения препарата внутри клетки позволяет резко сфокусировать токсичность на раковых клетках.
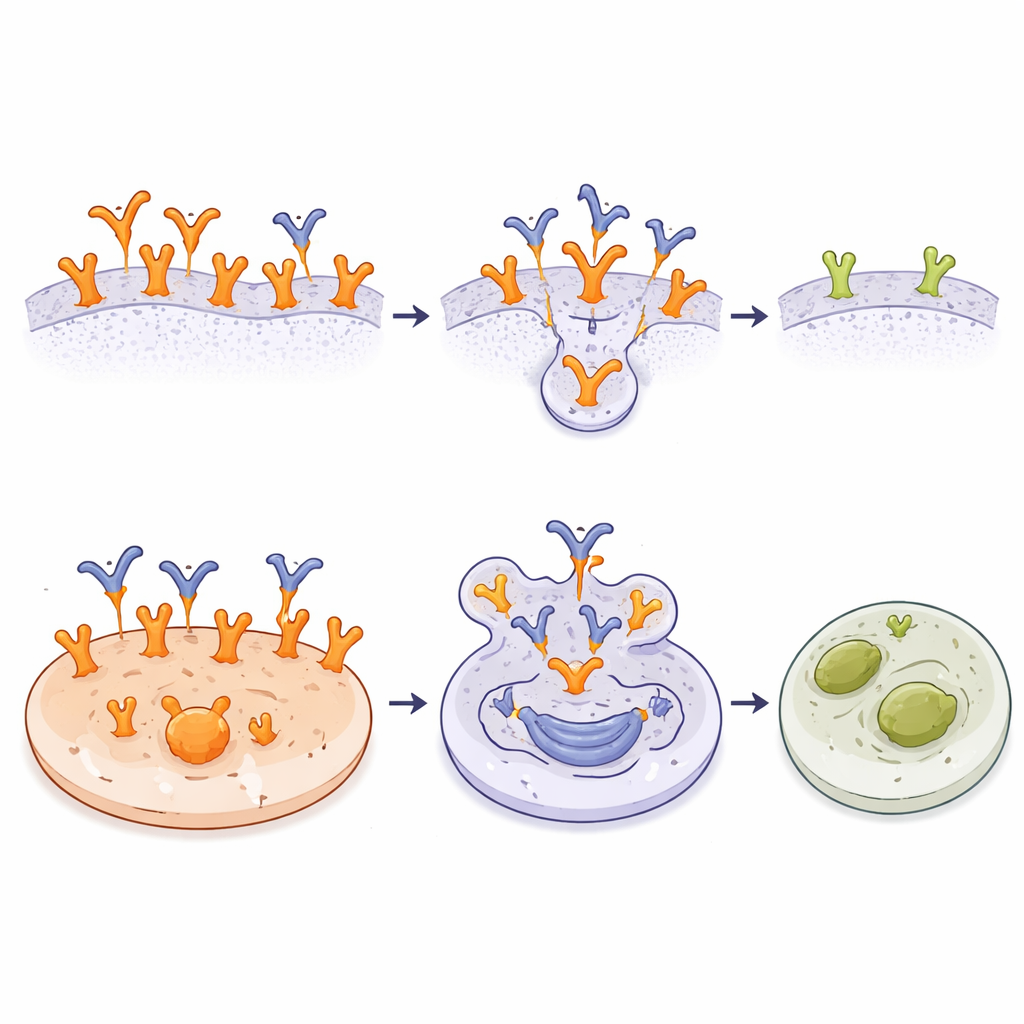
Что это может означать для будущей помощи при раке
Проще говоря, эта работа демонстрирует возможность создания антитела, которое «видит» EGFR только тогда, когда он выглядит и функционирует как рецептор, стимулирующий рак, при этом в основном игнорируя его обычную форму в здоровых тканях. Покажав, как именно A10 захватывает скрытую петлю на EGFR, и продемонстрировав, что конъюгат на основе A10 эффективно убивает рецептор‑богатые опухолевые клетки, щадя нормальные клетки, исследование закладывает прочную основу для разработки более безопасных, высокоспецифичных терапий. Если эти результаты подтвердятся у пациентов, будущие препараты на базе A10 могли бы доставлять мощные лекарства непосредственно к EGFR‑зависимым опухолям, оставляя остальную часть организма в значительной степени нетронутой.
Цитирование: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Ключевые слова: EGFR, конъюгат антитело‑лекарство, таргетная терапия рака, глиобластома, EGFRvIII