Clear Sky Science · ru
Структурные и механистические сведения о нацеливании на интегрины α2β1 и α5β1 с помощью биоинженерных внеклеточных везикул, происходящих из клеток рака легкого
Скрытые посланцы рака
Рак легкого часто обнаруживают на поздних стадиях, когда возможности лечения ограничены. Один перспективный подход — доставлять препараты исключительно в раковые клетки, щадя здоровые ткани. В этом исследовании рассматривается крошечная природная система доставки — внеклеточные везикулы (EV), которыми клетки рака уже обмениваются для передачи сообщений. Путём реинжиниринга этих везикул с коротким таргетным тегом исследователи показали, как они могут закрепляться на специфических «стыковочных портах» опухолевых клеток, создавая основу для более точных и менее токсичных противораковых терапий.
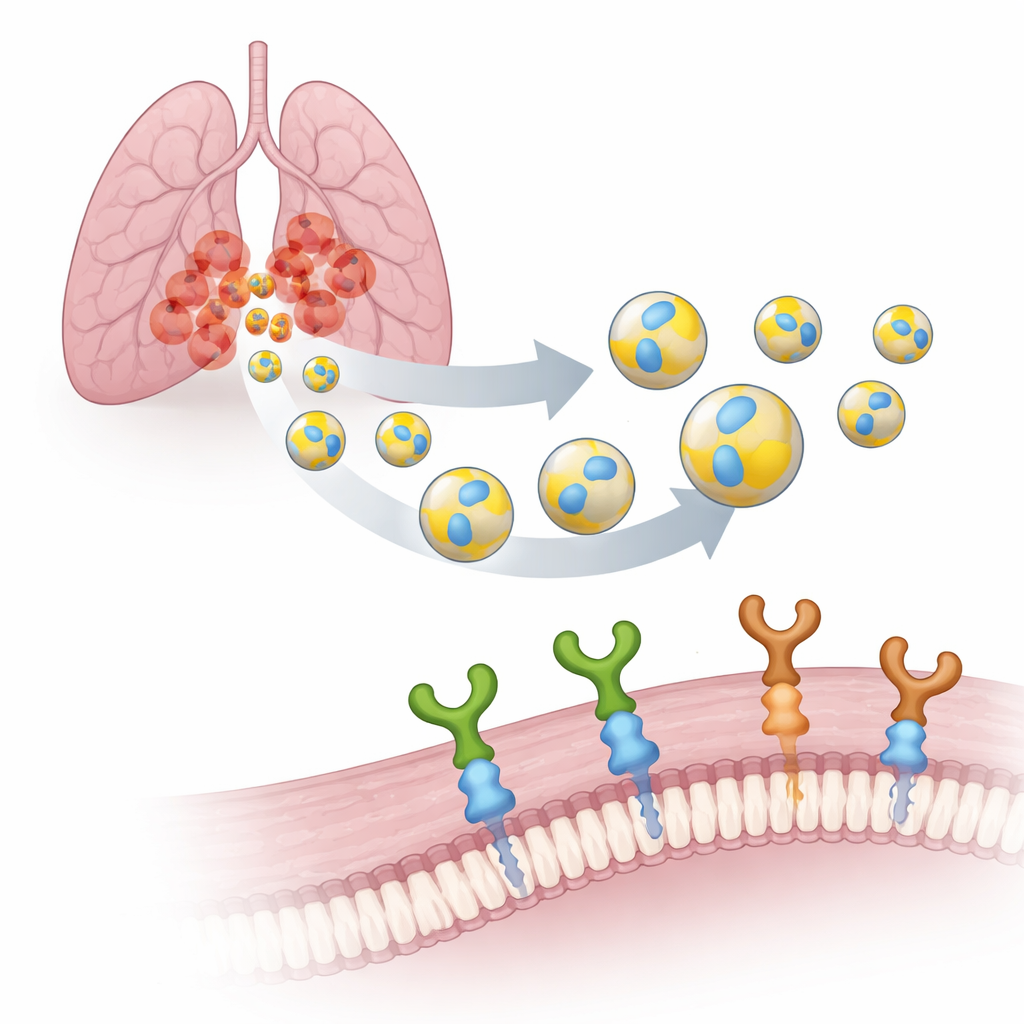
Преобразование природных упаковок в умных курьеров
Каждая клетка в нашем организме выпускает EV: наномасштабные пузырьки, окружённые мембраной, немного похожие на микроскопические мыльные пузыри. Поскольку их производят собственные клетки, EV биоразлагаемы, легко проникают через биологические барьеры и с меньшей вероятностью вызывают побочные эффекты по сравнению с синтетическими носителями. Команда сосредоточилась на везикулах, производимых человеческими клетками рака легкого (A549), и оформила их поверхность небольшим семиаминокислотным тегом PTHTRWA. Предыдущие эксперименты показали, что этот тег направляет EV к клеткам рака легкого у мышей, связываясь с опухолевыми клетками гораздо сильнее, чем с нормальными клетками легкого, при при этом слабой токсичности.
Поиск правильных «стыковочных портов» на опухолевых клетках
Чтобы превратить эти помеченные везикулы в по-настоящему нацеленные инструменты, исследователям нужно было определить, какие «порты» на раковых клетках они распознают. Они изучили два родственных поверхностных рецептора — интегрины α2β1 и α5β1. Это молекулярные «крюки», которые помогают клеткам прикрепляться к окружению и передавать сигналы внутрь. В опухолях легкого α5β1 тесно связан с агрессивным поведением, метастазированием и плохим прогнозом, тогда как α2β1 связывают с устойчивостью к химиотерапии. С помощью чувствительной техники поверхностного плазмонного резонанса команда сравнила, насколько сильно EV, украшенные PTHTRWA, связываются с обоими интегринами. Они обнаружили, что везикулы без тега едва взаимодействовали, тогда как помеченные EV формировали прочные, стабильные комплексы с обоими рецепторами в условиях, близких к физиологическим.
Приближение к молекулярному «объятию»
Чтобы понять, что происходит атом за атомом при встрече тега с интегринами, исследователи обратились к компьютерным симуляциям. Они построили трёхмерные модели тега, связаного с ключевыми участками интегринов, и наблюдали за поведением этих систем в виртуальной воде в течение сотен наносекунд. Вычисления показали, что PTHTRWA плотно ложится в неглубокую борозду на рецепторе α2β1, образуя сеть водородных связей и гидрофобных контактов, которые стабилизируют комплекс. Важно, что связывание сдвигало рецептор в более «открытую» форму — высокоаффинную, готовую к передаче сигнала — по сравнению с «закрытым» покоящимся состоянием. При испытании слегка изменённых версий тега оказалось, что небольшие химические модификации на одном конце могут тонко менять положение пептида в борозде и его предпочтение к одному интегрину перед другим.
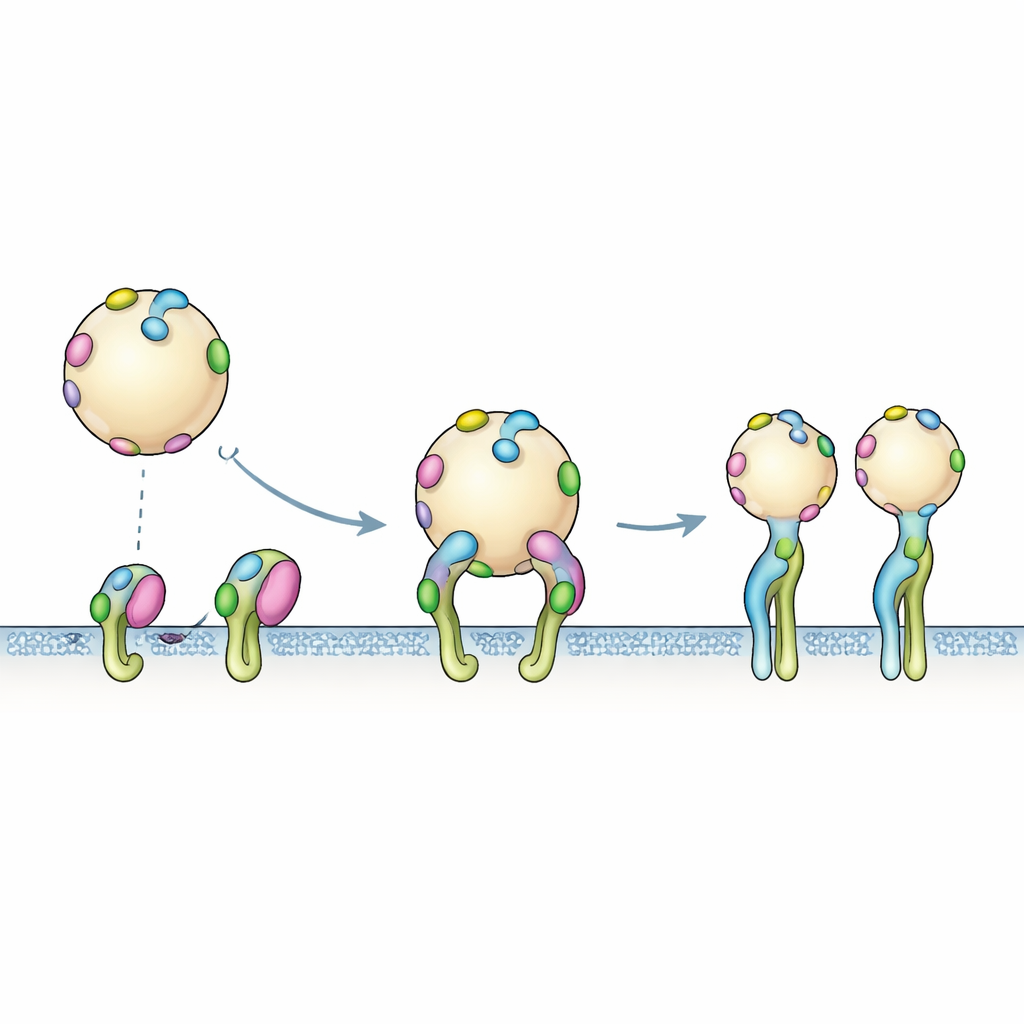
От одиночных тегов к мультивалентному захвату
Компьютерные модели описывают один тег, касающийся одного рецептора за раз, но реальная поверхность EV усеяна многочисленными копиями PTHTRWA. Эксперименты по связыванию отражали эту мультивалентную реальность: когда помеченная везикула приближается к участку с интегринами, вовлекаются сразу несколько тегов. Данные сенсора лучше всего соответствовали двухэтапному процессу. Сначала везикула кратковременно «пристыковывается» через быстрые обратимые контакты. Затем происходит более медленная перестройка, при которой интегрины переходят в открытую форму и общий захват усиливается. Это кооперативное, многорукое сцепление объясняет, почему кажущееся сродство связывания целых везикул выше, чем предсказанное по одному тегу.
Что это может значить для будущих методов лечения
Проще говоря, исследование показывает, что EV, вооружённые тегом PTHTRWA, могут избирательно распознавать интегрины, гиперактивные при раке легкого, и делают это, подталкивая эти рецепторы в открытую, туго связанную форму. Точная картография этих взаимодействий даёт правила проектирования для следующего поколения носителей на основе везикул, которые могли бы доставлять лекарства, контрастные вещества или другие грузы непосредственно в злокачественные клетки, в значительной степени игнорируя здоровые ткани. Хотя потребуются дополнительные испытания на животных и людях, стратегия нацеливания на интегрины приближает видение персонализированной медицины на основе EV к реальности.
Цитирование: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Ключевые слова: рак легкого, внеклеточные везикулы, интегрины, таргетная доставка лекарств, молекулярные моделирования