Clear Sky Science · ru
Точное количественное определение гетерогенности и прогрессирования при МСА и болезни Паркинсона с помощью машинного обучения
Почему это важно для людей с нарушениями движений
Люди с болезнью Паркинсона или множественной системной атрофией (МСА) часто годами живут в состоянии неопределённости, поскольку эти два состояния клинически могут быть очень похожи, но имеют принципиально разный прогноз. В этом исследовании рассматривается, как современные компьютерные методы, применённые к снимкам мозга, могут помочь врачам раньше отличать эти заболевания друг от друга, понимать их индивидуальную вариабельность и отслеживать их изменения со временем.
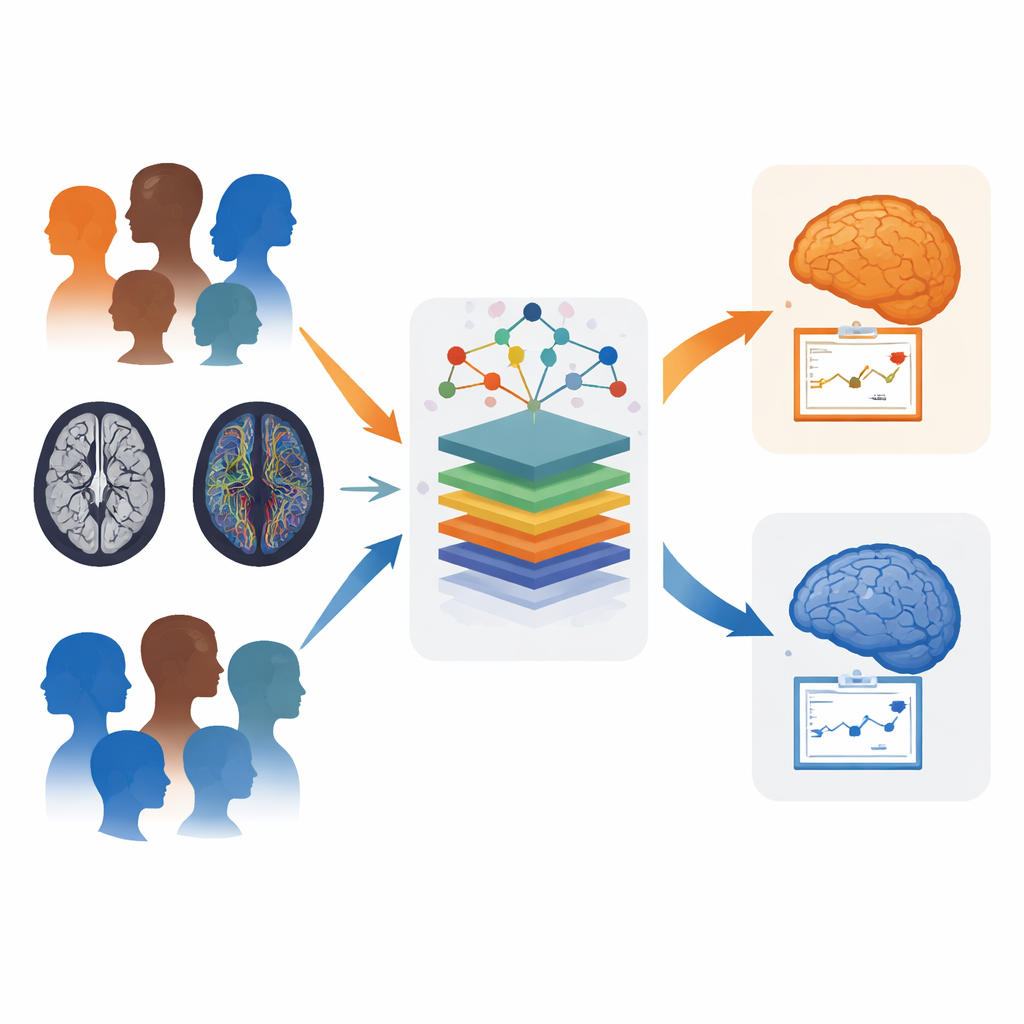
Взгляд внутрь мозга для более чётких подсказок
В основе и болезни Паркинсона, и МСА лежит патологическое накопление белка альфа‑синуклеина, но поражаются разные участки мозга. При болезни Паркинсона в основном страдает глубокая область, продуцирующая дофамин, тогда как при МСА затрагиваются более широкие сети, включая мозжечок, ствол мозга и двигательные цепи. На обычных МРТ эти различия могут быть слабо выражены, особенно на ранних стадиях, и многих пациентов с МСА сначала ошибочно диагностируют как больных Паркинсоном. Исследователи использовали два вида МРТ — структурные сканы, показывающие форму и объём мозга, и диффузионную МРТ, раскрывающую состояние белого вещества — чтобы искать более точные, индивидуально значимые паттерны.
Обучение компьютеров выявлять скрытые паттерны
Команда изучала 17 здоровых добровольцев, 27 человек с МСА (разделённых на церебеллярный и паркинсонический подтипы) и 15 больных Паркинсоном, с наблюдением до четырёх ежегодных визитов. Они разделили мозг на десятки регионов и измерили локальные объёмы и два диффузионных параметра, отражающих, как вода движется вдоль нервных волокон. Эти измерения были поданы в несколько моделей машинного обучения, которые обучались на простой задаче: определить, принадлежит ли скан человеку с МСА или с болезнью Паркинсона. Чтобы избежать переобучения на редкой болезни, авторы применили тщательную кросс‑валидацию, многократное повторение обучения и сравнили пять семейств алгоритмов, прежде чем выбрать лучших исполнителей.
От сложных снимков к единому персональному показателю
Вместо того чтобы остановиться на бинарном компьютерном диагнозе, авторы хотели получить число, которое отражало бы, насколько «МСА‑подобен» мозг конкретного человека по сравнению с Паркинсоном. Они использовали объяснимый метод ИИ под названием SHAP, который разбивает решение модели на вклад каждого региона мозга. Эти вклады послужили весами, подчёркивающими области, которые модель сочла наиболее информативными. Комбинируя веса с фактическими МРТ‑измерениями по всем регионам, они создали три показателя «гетерогенности» (HET) — по одному для объёма мозга и по одному для каждого из двух диффузионных параметров. Каждый HET‑балл сводит сложный паттерн изменений по всему мозгу к единому суммарному значению для каждого человека и визита.
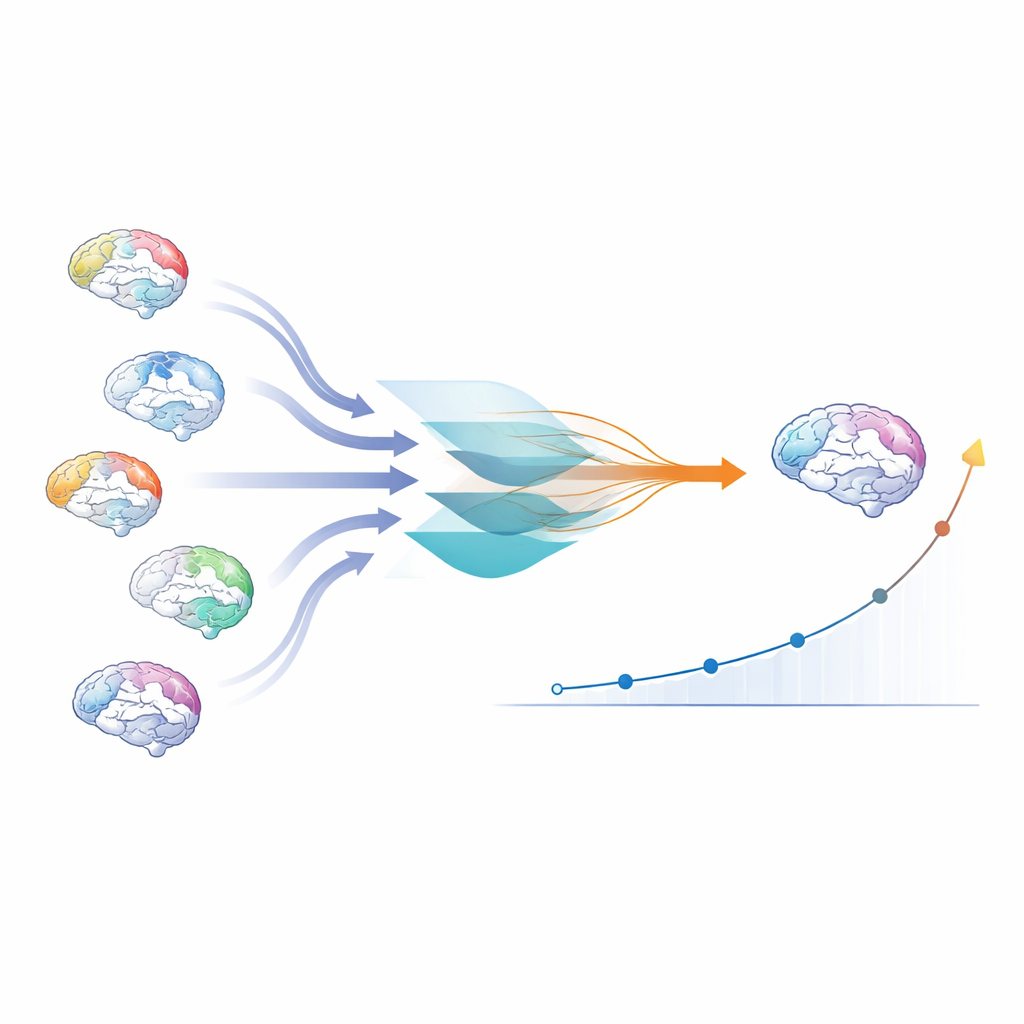
Определение типа заболевания и его изменений во времени
Новые HET‑показатели оказались полезнее, чем просто имитация существующих МРТ‑маркеров. Они классифицировали МСА и болезнь Паркинсона так же хорошо, а часто и лучше, чем широко используемый индекс атрофии, основанный на нескольких ключевых областях. Важно, что HET особенно хорошо разделял паркинсоническую форму МСА и болезнь Паркинсона — различие, которое традиционно сложно уловить на стандартных снимках. При анализе динамики изменения HET за год они лучше коррелировали с клиническим ухудшением, измеряемым стандартной шкалой для МСА, чем простые показатели усадки мозжечка. Карты HET по регионам также воспроизводили известные паттерны поражения при МСА, такие как дегенерация цепей мозжечка и ствола мозга, одновременно выявляя более широкое вовлечение лобного и лимбического белого вещества и соединений между полушариями мозга.
Что это может значить для пациентов и ухода
Для неспециалиста ключевая мысль такова: более умный анализ рутинных данных МРТ может преобразовать разрозненные признаки повреждения по всему мозгу в единый, понятный показатель, отражающий, насколько «МСА‑подобен» паттерн у конкретного человека и насколько быстро он меняется. Этот подход не лечит болезнь и требует подтверждения на больших когортах, но он предлагает перспективный инструмент для более ранней и точной диагностики, лучшего отслеживания прогрессирования и более чувствительного тестирования новых методов лечения в клинических испытаниях. Учитывая, что у разных пациентов мозг меняется по‑разному, рамка HET приближает область к действительно персонализированной помощи при нарушениях движений.
Цитирование: Gebre, R.K., Raghavan, S., De Tora, M.E.J. et al. Precise disease heterogeneity and progression quantification in MSA and Parkinson’s disease using machine learning. Sci Rep 16, 10579 (2026). https://doi.org/10.1038/s41598-026-45949-5
Ключевые слова: множественная системная атрофия, болезнь Паркинсона, МРТ мозга, машинное обучение, биомаркеры