Clear Sky Science · ru
Фторхинолиновое соединение оказывает анти-эритролейкимические эффекты за счёт двойного воздействия на GLUT1 и сигнальный путь PI3K/AKT
Новый взгляд на опасный рак крови
Эритролейкемия — редкая, но крайне агрессивная форма рака крови, для которой помимо трансплантации стволовых клеток доступно немного вариантов лечения. Для многих, в основном пожилых пациентов, это означает тяжёлую терапию, большие расходы и неблагоприятный прогноз. В этом исследовании изучается лабораторно синтезированное соединение FKL-137, которое повреждает клетки эритролейкемии неожиданным образом: лишая их любимого топлива — сахара — и запуская механизм самоуничтожения. Работа указывает на возможный новый класс таргетных препаратов, использующих зависимость раковых клеток от изменённого энергетического обмена при относительном сохранении здоровых тканей.
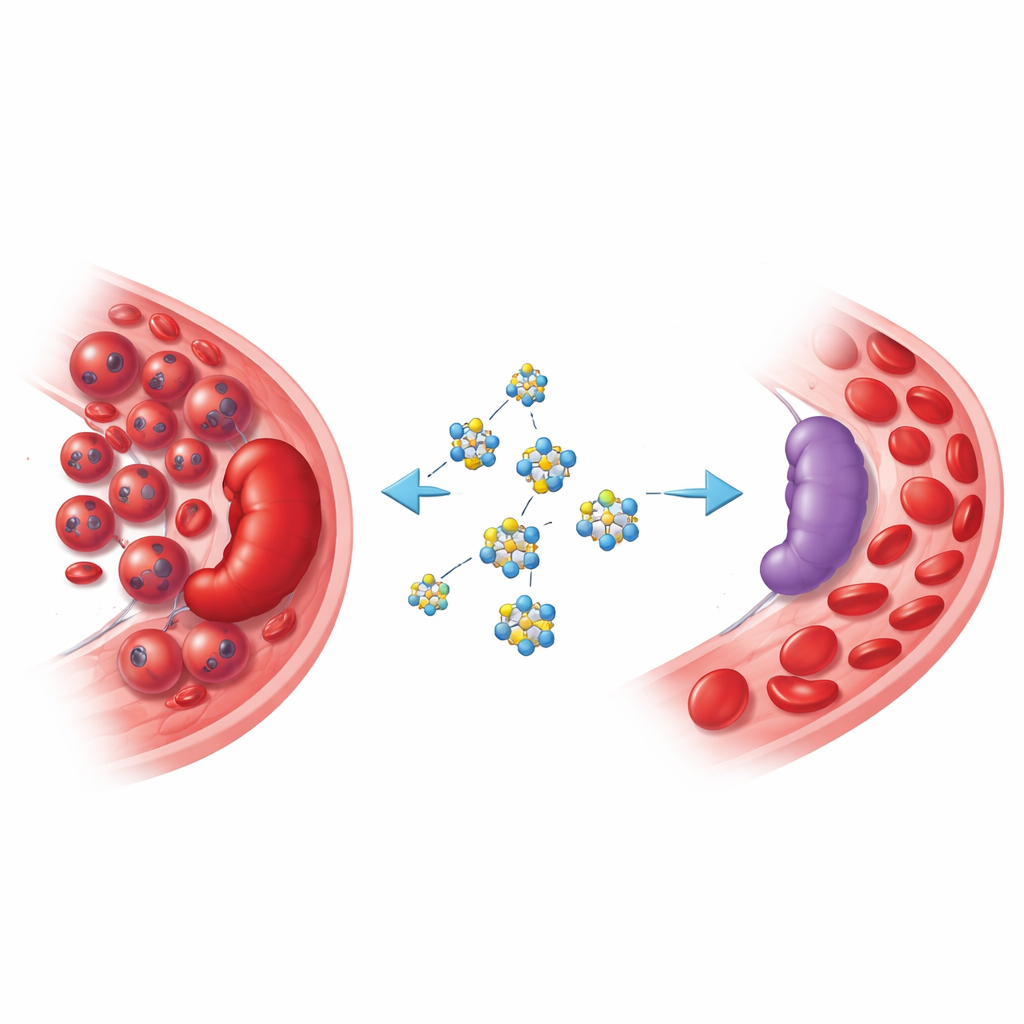
Когда кровяные клетки выходят из-под контроля
При эритролейкемии незрелые предшественники эритроцитов бесконтрольно размножаются в костном мозге и селезёнке. У пациентов может развиваться тяжёлая анемия, селезёнка увеличивается и рискует разорваться, а состояние здоровья стремительно ухудшается. Текущие терапии ограничены, и многие люди слишком слабы для агрессивного лечения. При этом учёные выяснили, что многие злокачественные заболевания крови опираются на перепрограммированное использование сахара: они активно захватывают глюкозу и быстро превращают её в энергию и строительные блоки, что помогает им размножаться и уклоняться от иммунного ответа. Нацеливание на эту метаболическую «зависимость» стало привлекательной стратегией для новых препаратов.
Лишение раковых клеток сахара
Исследователи сосредоточились на малой синтетической молекуле FKL-137, происходящей из химического семейства, уже известного антираковой активностью. В лабораторных экспериментах они подвергли две линии человеческих клеток эритролейкемии воздействию растущих доз FKL-137. Соединение резко замедляло рост клеток с течением времени и запускало программируемую гибель, что заметно по классическим изменениям формы клеток и активации внутренних механизмов смерти. Важно, что FKL-137 был значительно более активен против лейкемических клеток, чем против нормальных печёночных клеток, а оценка безопасности препарата указывала на относительно низкую токсичность в эффективных дозах.
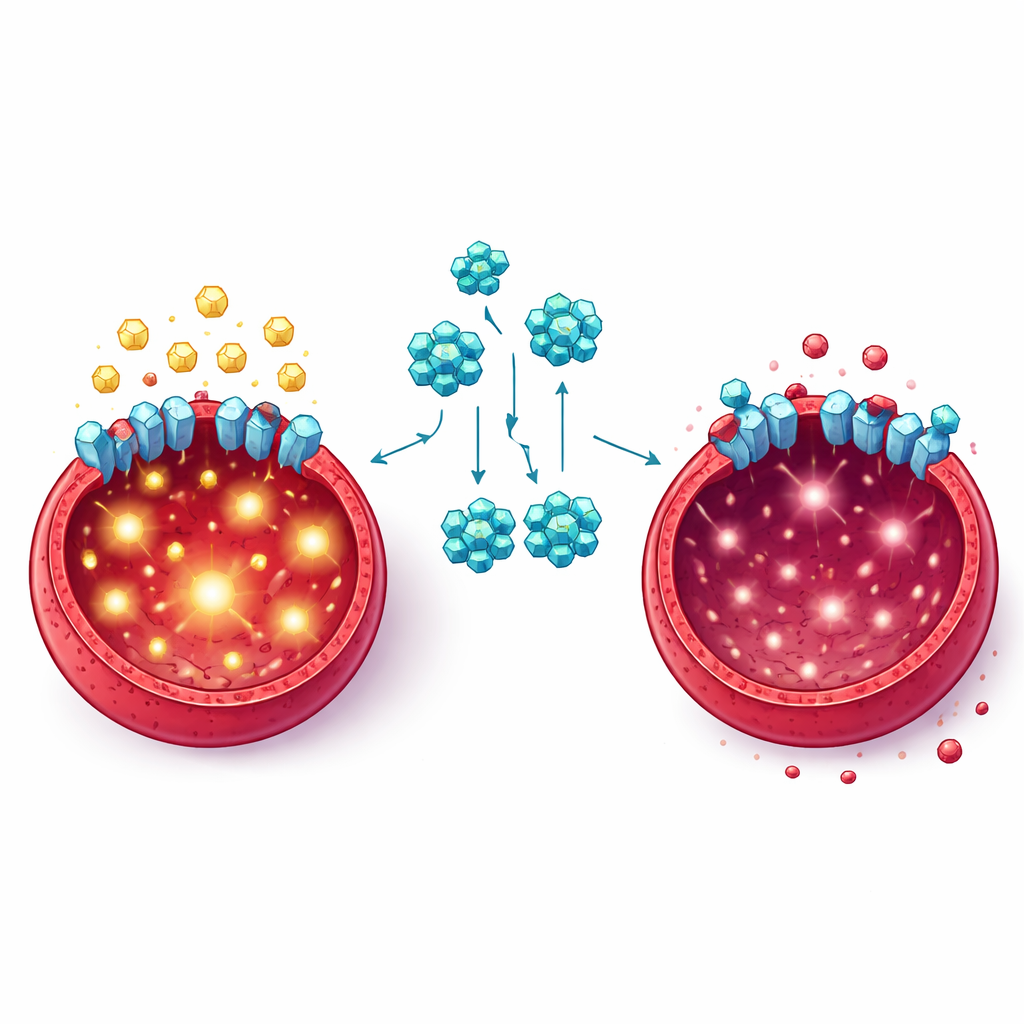
Блокируя «ворота» сахара в клетку
Углубившись в механизмы, команда изучила, как FKL-137 влияет на метаболизм рака. Они обнаружили, что обработанные лейкемические клетки поглощают меньше глюкозы и выделяют меньше лактата — побочного продукта интенсивного расщепления сахара. Ключевые белки, которые обычно помогают превращать глюкозу в энергию и строительные блоки, были подавлены. С помощью компьютерного моделирования, тестов термической стабильности и визуализации исследователи показали, что FKL-137 связывается с GLUT1 — важной «вратами» на поверхности клетки, через которые глюкоза попадает внутрь. Когда уровни GLUT1 уменьшали генетическими приёмами, лейкемические клетки росли медленнее и использовали меньше сахара, а также становились ещё более чувствительны к FKL-137. Это подтвердило, что GLUT1 является как драйвером роста клеток эритролейкемии, так и ключевой мишенью препарата.
Разрывая цикл сигнального роста
Исследование также выявило эффекты, выходящие за рамки непосредственного блокирования ворот для глюкозы. Клетки эритролейкемии обычно используют сигнальный путь PI3K/AKT для поддержания выживания, роста и интенсивного потребления сахара, отчасти поддерживая работу GLUT1. Лечение FKL-137 снизило активные формы ключевых белков этого пути, разорвав подкрепляющий цикл между транспортом сахара и ростовыми сигналами. У мышей, инфицированных вирусом, надёжно вызывающим эритролейкемию, терапия FKL-137 улучшала показатели эритроцитов, уменьшала размер увеличенной селезёнки, снижала инвазию раковых клеток в органы и корректировала нарушенный сахарный метаболизм в тканях селезёнки — всё это без очевидных повреждений сердца, печени, лёгких или почек.
Перспективы, ограничения и дальнейшие шаги
В совокупности работа представляет FKL-137 как кандидат-препарат с двойным действием: он блокирует главный «сахарный ворот» в клетках эритролейкемии и ослабляет мощный ростовой путь, зависящий от этого топлива. Лишая раковые клетки питания, а затем подталкивая их к гибели, соединение предлагает концептуально элегантный способ воспользоваться слабостью, которой нормальные клетки в меньшей степени подвержены. Авторы, однако, предостерегают, что FKL-137 требует доработки: у него относительно узкое терапевтическое окно, раковые клетки могут компенсировать эффект перераспределением метаболизма, и результаты in vitro и на моделях мышей нужно подтвердить на тканях человека. Тем не менее исследование усиливает идею, что точечное воздействие на способы «питания» и роста раковых клеток может открыть новую линию борьбы с этим трудно контролируемым раком крови.
Цитирование: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
Ключевые слова: эритролейкемия, метаболизм рака, инhibитор GLUT1, путь PI3K AKT, таргетная терапия