Clear Sky Science · ru
Исследование взаимодействий иммунного белка колицинa E9 из Escherichia coli с ДНК-гиразой Pseudomonas aeruginosa: передовой вычислительный подход к разработке новых антимикробных стратегий
Преобразование бактериального оружия в новые лекарства
По мере распространения устойчивости к антибиотикам врачам становится всё труднее справляться с опасными инфекциями. Некоторые из самых упорных возбудителей, такие как Pseudomonas aeruginosa, устойчивы ко многим препаратам. В этой работе авторы обращаются к самим бактериям в поисках новых идей, исследуя возможность перепрофилирования встроенного защитного белка одной микробной клетки для дезактивации жизненно важного фермента в другой. С помощью современных компьютерных моделирований исследователи демонстрируют, как небольшой «иммунный» белок может прочно прикрепляться к ключевому бактериальному белку, указывая на новый путь для разработки потенциальных антимикробных средств.
Маленький щит против смертельного токсина
Определённые штаммы Escherichia coli продуцируют мощные белковые токсины — колицины, которые могут убивать соседние бактерии. Чтобы не отравиться самим, эти бактерии синтезируют соответствующие иммунные белки. Один из таких защитников, известный как иммунный белок колицинa E9 (часто обозначаемый Im9), связывается с каталитическим доменом токсина и предотвращает повреждение собственной ДНК. Поскольку это взаимодействие настолько специфично и прочнo, учёные давно предполагали, что его подробное изучение может открыть новые способы контроля вредных бактерий. В данной работе авторы выясняют, может ли Im9 также прикрепляться к ДНК-гиразе Pseudomonas aeruginosa — важному ферменту, управляющему скручиванием и копированием её ДНК.
Атакуя уязвимый фермент в трудноизлечимом микроорганизме
Pseudomonas aeruginosa — важный внутрибольничный патоген, способный переживать в суровых условиях и устойчивый к многим препаратам. ДНК-гираза — один из ключевых ферментов, отвечающий за поддержание правильной топологии длинных молекул ДНК, что необходимо для их репликации. Блокирование этого фермента может остановить рост бактерий, поэтому он уже является проверенной мишенью для ряда антибиотиков. Авторы применили инструмент глубокого обучения для анализа трёхмерной структуры ДНК-гиразы Pseudomonas и выявления возможных «горячих точек» — кластеров аминокислот на поверхности, наиболее важных для связывания партнёров. Эти участки формируют активный карман фермента, где происходит нормальная обработка ДНК и где потенциальный ингибитор мог бы закрепиться.
Моделирование молекулярного рукопожатия
Чтобы оценить, способен ли Im9 схватиться за эти «горячие точки», исследователи использовали программы молекулярного докинга, которые виртуально «подгоняют» белки друг к другу, как 3D-пазлы. Сначала они очистили и восстановили доступные структуры Im9 и ДНК-гиразы, исправили отсутствующую петлю в ферменте и провели короткие симуляции для релаксации напряжённых участков. Затем применили два комплементарных докинговых инструмента — ClusPro и LightDock — чтобы сгенерировать множество кандидатных комплексов. Из них отобрали наиболее перспективные варианты и подвергли их долгим молекулярно-динамическим симуляциям продолжительностью сотни наносекунд. Эти временные «кинофильмы» позволили наблюдать, как оба белка подстраиваются, изгибаются и устаканиваются в более стабильные формы при связывании.
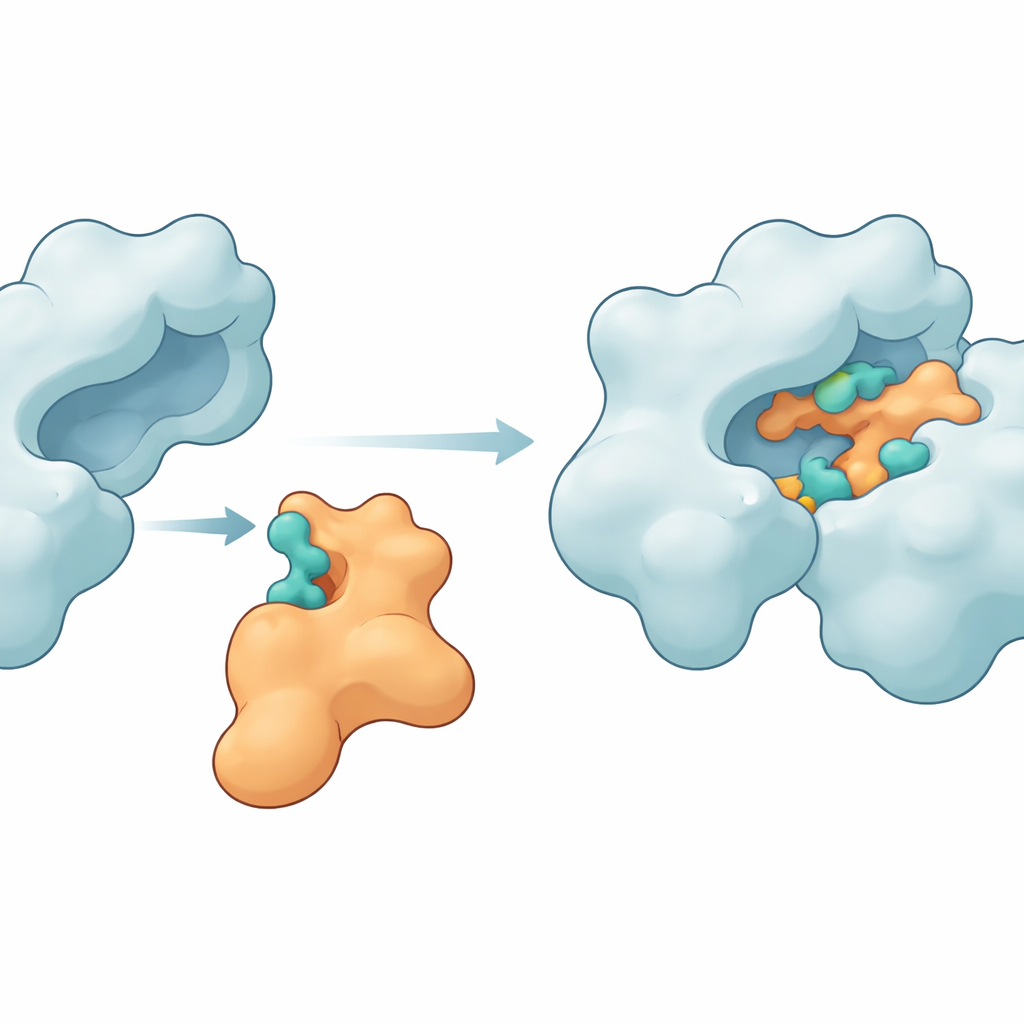
Ключевые контактные точки, удерживающие белки вместе
Симуляции показали, что Im9 действительно способен образовывать плотный и устойчивый комплекс с ДНК-гиразой. Несколько аминокислот фермента — такие как MET27, ASP47, LYS105, LEU198, ASN199, ARG191 и GLU194 — неоднократно образовывали водородные связи и другие привлекательные взаимодействия с соответствующими участками Im9. В одной из ведущих моделей оба партнёра сохраняли от шести до десяти водородных связей на протяжении большей части симуляции, что свидетельствует о прочном и хорошо организованном интерфейсе. Другие структурные показатели, включая степень компактности белков и амплитуду флуктуаций их конформаций, показали, что фермент оставался структурно устойчивым, тогда как иммунный белок достаточно подстраивался, чтобы обхватить поверхность гиразы. Расчёты энергий методом MM-GBSA дополнительно подтвердили, что эти контакты создают благоприятную, пусть и умеренную, свободную энергию связывания, в основном определяемую электростатическими и ван-дер-Ваальсовыми вкладами.
От компьютерных моделей к будущим антимикробным средствам
В совокупности результаты указывают на то, что иммунный белок колицинa E9 может стабильно связываться с активной областью ДНК-гиразы Pseudomonas, формируя долговременный комплекс, который теоретически мог бы блокировать нормальную функцию фермента в обработке ДНК. Хотя эти выводы основаны исключительно на компьютерных моделях и требуют последующей экспериментальной проверки, они дают детальный план мест и способов, где и как белковый ингибитор мог бы прикрепляться. Для неспециалистов главный вывод таков: природные бактериальные «оружие» и «щиты» могут вдохновлять новые стратегии борьбы с трудноизлечимыми инфекциями. Понимание этого микроскопического рукопожатия на атомном уровне приближает учёных к созданию новых антимикробных средств, которые блокируют критические бактериальные ферменты, не повреждая клетки человека.
Цитирование: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
Ключевые слова: устойчивость к антибиотикам, ДНК-гираза, взаимодействия белок–белок, вычислительное проектирование лекарств, Pseudomonas aeruginosa