Clear Sky Science · ru
Кристаллографические данные для долихилфосфат-маннозной синтетазы Pyrococcus furiosus указывают, что фермент может переворачивать свой гликолипидный продукт
Как термофильные микробы поддерживают целостность своей клеточной оболочки
Многие микробы, обитающие в кипящих условиях, выживают благодаря защитной сахарной оболочке на поверхности клетки. Для построения этой оболочки требуются особые липидно-сахарные молекулы, которые синтезируют с одной стороны мембраны, а затем переносят на другую. В этом исследовании разобран один такой фермент, создающий молекулу, у термофильного микроорганизма, и показано, что, не менее поразительно, тот же белок возможно помогает переворачивать свой продукт сквозь мембрану — выполняя две функции одновременно.
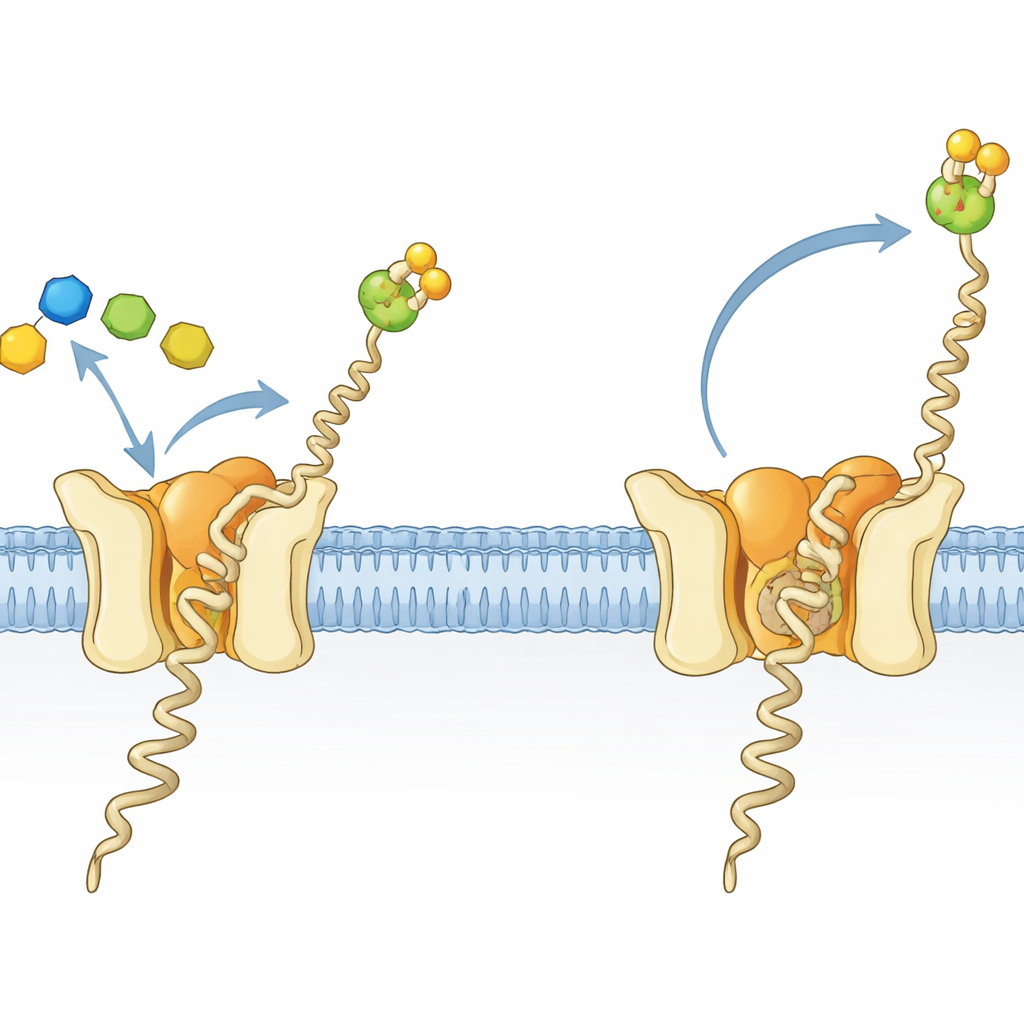
Крошечная фабрика для важной липидно-сахарной молекулы
Клетки во всех доменах жизни украшают множество белков цепочками сахаров — процесс, необходимый для правильного сворачивания, стабильности и межклеточной коммуникации. У архей и эукариот ключевым строительным блоком для таких модификаций является липидно-сахарная молекула долихилфосфат-манноза (Dol-P-Man). Она состоит из длинного гидрофобного хвоста, как якоря в мембране, и сахарно-фосфатной головы, выступающей в водную среду. Dol-P-Man синтезирует фермент долихилфосфат-маннозная синтетаза (DPMS), который переносит маннозу с растворимого донора на мембраносвязываемый липид. У гипертеммофильного археона Pyrococcus furiosus DPMS представляет собой одноцепочечный белок, называемый DPMS типа III, с растворимой каталитической частью, прикреплённой к четырёхспиральному трансмембранному фрагменту, роль которого ранее оставалась неясной.
Запечатление фермента в действии
Исследователи кристаллизовали DPMS P. furiosus вместе с его субстратами и следили за реакцией с помощью рентгеновской кристаллографии. Их новая структура в сочетании с тремя более ранними фиксирует серию снимков вокруг момента переноса сахара. В одном состоянии донор (GDP-манноза) и акцептор, похожий на Dol-P, связаны в точной геометрии, размещающей реактивный углерод маннозы прямо напротив фосфатной группы на Dol-P — идеальная «предпереходная» конфигурация. Петли фермента действуют как входная и выходная двери: они закрываются, чтобы удержать донора и ион металла на месте, затем перестраиваются, чтобы открыть путь для входа Dol-P и выхода использованного GDP после передачи сахара. Эти детали проясняют, как фермент обеспечивает эффективный и точный перенос сахара на поверхности мембраны.
Перевёрнутый продукт, скрытый в мембране
Более удивительным оказалось второе, отличное состояние, обнаруженное в тех же кристаллах. Здесь готовая молекула Dol-P-Man не находится в активном центре, а застряла глубже в трансмембранной части белка в «перевёрнутой» ориентации. Её сахарно-фосфатная голова расположена в полярном кармане между двумя парами спиралей (TMD1 и TMD2), в то время как гидрофобный хвост тянется вдоль желобка, образованного спиралями. Ключевая аминокислота — фенилаланин — по-видимому выступает в роли засовa, который может либо блокировать, либо открывать доступ к этому карману. Качество электронной плотности и упаковка белка в кристалле указывают на то, что этот перевёрнутый Dol-P-Man — не артефакт кристаллических контактов, а подлинное, хорошо населённое состояние, которое фермент может принимать.
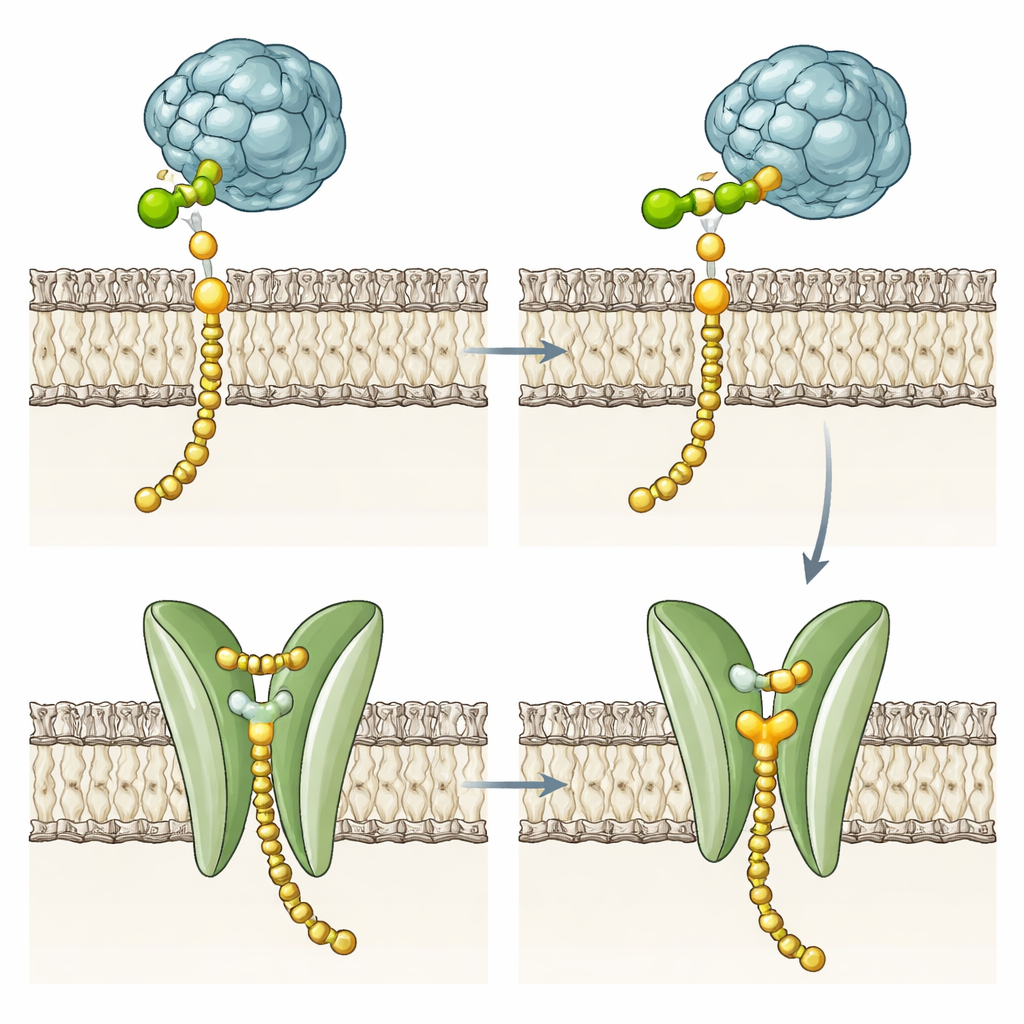
Мутантные ферменты намекают на вторую функцию
Чтобы проверить, необходима ли трансмембранная домен для каталитической химии переноса сахара, команда создала несколько вариантов. Они удалили большую часть или все спирали, заменили их другим мембранным сегментом из дрожжевого DPMS или изменили ключевые остатки в кармане и фенилаланиновый затвор. Удивительно, но эти мутанты по-прежнему синтезировали Dol-P-Man с похожими скоростями, как и целый фермент, хотя некоторые из них были несколько менее стабильны в мембране. Это показывает, что основная химия сосредоточена в растворимой каталитической области и что четырёхспиральный пучок не обязателен для присоединения маннозы к Dol-P. Вместо этого его сохранённый полярный карман, желобок и запорный остаток указывают на специализированную роль в обращении с готовым продуктом, особенно у гипертеммофильных архей, чьи жёсткие мембраны делают спонтанное переворачивание липидов энергетически затратным.
Почему важен фермент с двойной функцией
Собрав структурные и мутaционные данные вместе, авторы предлагают, что DPMS типа III — это «многофункциональный» белок. Сначала он синтезирует Dol-P-Man на внутренней стороне плазматической мембраны археона; затем его трансмембранный домен может помогать переворачивать липидно-сахарную молекулу так, чтобы голова оказалась снаружи клетки, готовой к использованию другими ферментами, которые строят сахарную оболочку. По-видимому, эволюция благоприятствовала такому смешанному дизайну преимущественно у экстремофильных архей, где размещение места синтеза рядом с выделенным желобком для флиппинга могло бы минимизировать потери и тепловое повреждение. Хотя эта работа ещё не доказывает флиппинг непосредственно, она предлагает конкретную структурную модель того, как фермент может одновременно создавать и перемещать ключевой липидный промежуточный продукт через суровый барьер мембраны.
Цитирование: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Ключевые слова: долихилфосфат-манноза, липидный флиппаза, археи, гликозилирование белков, мембранные ферменты