Clear Sky Science · ru
Моделирование патогенеза токсинов Clostridioides difficile и защиты антисерумом на имуннокомпетентной платформе «кишка‑на‑чипе»
Почему эта модель инфекции кишечника важна
Антибиотики спасают жизни, но могут ослабить защиту кишечника и сделать его уязвимым для опасных инфекций. Один из главных виновников — бактерия Clostridioides difficile, вызывающая тяжёлую диарею и угрожающие жизни воспалительные поражения толстой кишки, особенно у госпитализированных пациентов. В этом исследовании представлена миниатюрная «кишка на чипе», воспроизводящая ключевые особенности человеческого кишечника, включая кровеносные сосуды и клетки иммунной системы, что позволяет в реальном времени наблюдать, как токсины C. difficile разрушают кишечник и как антитела могут предотвращать это повреждение.
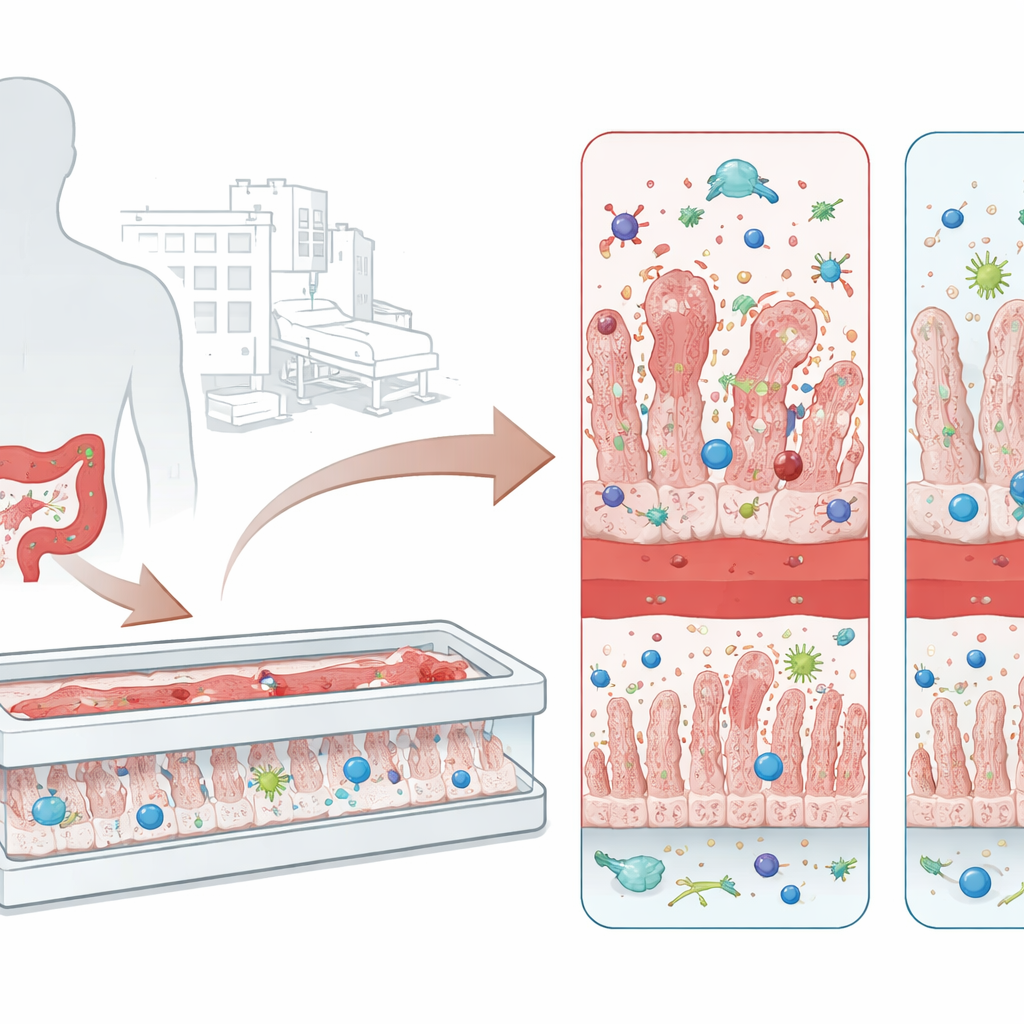
От упрямой госпитальной инфекции до повреждения кишечника
C. difficile процветает у людей, у которых нарушена нормальная микрофлора кишечника, часто после курса широкоспектровых антибиотиков. Микроорганизм выживает в суровых условиях в виде жёстких спор и, закрепившись в толстой кишке, выделяет два основных токсина — TcdA и TcdB. Эти токсины атакуют клетки кишечника, ослабляют плотные контакты между ними и вызывают волны воспаления. Последствия варьируются от назойливой диареи до псевдомембранозного колита — состояния, при котором стенку кишечника покрывают слои погибших тканей и скопления иммунных клеток. Современное лечение в основном опирается на дополнительные антибиотики и иногда на пересадку фекальной микробиоты, но у многих пациентов инфекции повторяются, что подчёркивает необходимость лучших моделей для изучения болезни и проверки препаратов, блокирующих токсины.
Создание крошечной живой кишки на чипе
Традиционные лабораторные модели выращивают плоский слой кишечных клеток в чашке Петри. Хотя такие культуры полезны, двумерные системы лишены кровеносных сосудов, иммунных клеток и мягкого потока жидкости, формирующего настоящий кишечник. Исследователи использовали микроинженерное устройство «кишка‑на‑чипе» с двумя параллельными каналами, разделёнными пористой мембраной. С одной стороны располагаются кишечные клетки, формирующие пальцеобразные выступы, напоминающие ворсинки, и образующие плотный барьер. На противоположной стороне — клетки человеческих сосудов. В эту миниатюрную ткань внедрили макрофаги, полученные из моноцитов, которые оседают в стенке кишки, и циркулирующие нейтрофилы, способные перемещаться по сосудистому каналу и проникать в ткань, создавая имуннокомпетентную кишку‑на‑чипе (i‑IoC), более правдоподобно имитирующую живой кишечник.
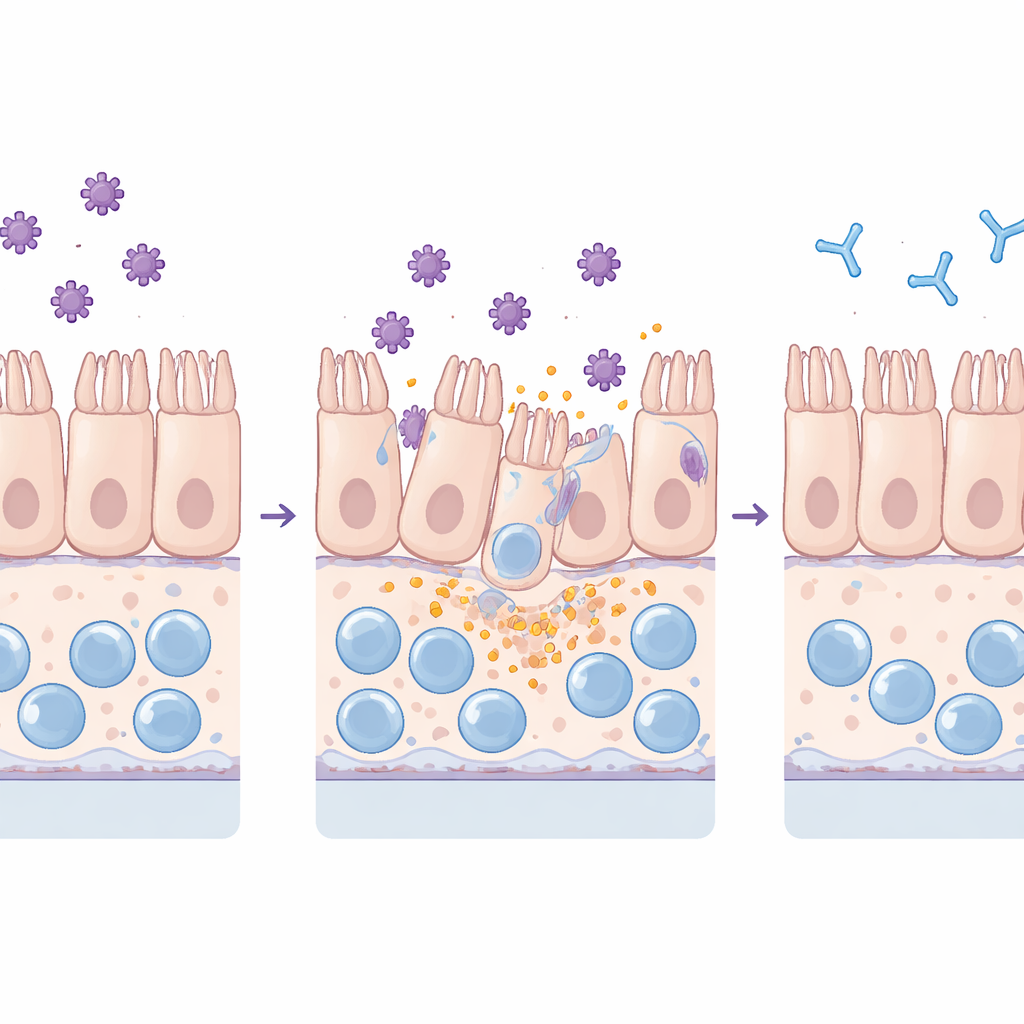
Наблюдение за тем, как токсины повреждают барьер
Команда подвергла действию очищенные TcdA и TcdB как стандартные плоские культуры, так и более сложный чип. Они отслеживали, насколько барьер кишечника препятствует проникновению флуоресцентного красителя, изучали белки контактов, удерживающие соседние клетки вместе, и измеряли воспалительные молекулы и маркеры повреждения клеток в окружающей жидкости. Оба токсина повреждали ткань, но по-разному: TcdA в основном разрушал плотные контакты и вызывал округление клеток, тогда как TcdB приводил к массовой потере клеток из слоя. Существенно, чип фиксировал эти эффекты при намного более низких уровнях токсинов, чем плоские культуры, что отражает его большую чувствительность и более жизнеподобное поведение при непрерывном потоке.
Иммунные клетки разжигают воспаление — и могут быть защищены
Добавление макрофагов и нейтрофилов в чип усиливало реакцию на токсины. Макрофаги усиливали выделение ключевых провоспалительных медиаторов, таких как IL‑6 и IL‑8, но сами при этом истощались, что согласуется с воспалительной формой гибели клеток. Нейтрофилы прилипали к сосудистой стенке и мигрировали в ткань кишки, повторяя приток иммунных клеток, наблюдаемый у пациентов. Длительное воздействие токсинов повреждало не только кишечную выстилку, но в конце концов и слой сосудов. Однако при предварительном смешивании токсинов с сыворотками, нейтрализующими токсины, структурные повреждения, протекание барьера, всплески цитокинов, потеря макрофагов и инфильтрация нейтрофилов были существенно уменьшены. В более длительных экспериментах ткани, повреждённые TcdB, могли частично восстанавливаться после удаления токсинов, тогда как поврежения от TcdA оставались более стойкими, что указывает на различные возможности заживления после действия каждого токсина.
Что это значит для пациентов и терапий
Главная мысль для непрофессионального читателя: эта крошечная живая модель кишечника реалистично воспроизводит, как токсины C. difficile повреждают кишечник и стимулируют иммунитет, а также демонстрирует, насколько антитоксические антитела могут защитить ткань. По сравнению с простыми клеточными слоями кишка‑на‑чип более чувствительна, содержит сосуды и иммунные клетки и может функционировать в течение нескольких дней, позволяя захватить как ранние повреждения, так и попытки восстановления. Это делает её перспективной платформой для тестирования новых методов лечения и вакцин, нейтрализующих токсины без дополнительного нарушения микробиоты, и потенциально инструментом для персонализации терапии с использованием клеток самого пациента в будущем.
Цитирование: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Ключевые слова: Clostridioides difficile, кишка‑на‑чипе, инфекция кишечника, нейтрализующие антитела, модели орган‑на‑чипе