Clear Sky Science · ru
Мультипhotонная микроскопия без меток и машинное обучение для распознавания гепатоцеллюлярной карциномы
Почему это важно для людей с раком печени
Рак печени, особенно гепатоцеллюлярная карцинома, широко распространён и смертельно опасен, и операция часто остаётся единственным шансом на излечение. Во время вмешательства хирурги должны удалить весь опухолевый узел, сохранив как можно больше здоровой ткани печени — сложный компромисс, когда поражённая печень уже выглядит аномально. В этом исследовании рассматривается новый способ «увидеть» рак в реальном времени во время операции без красителей и длительных лабораторных анализов, сочетая продвинутую лазерную микроскопию с искусственным интеллектом. Цель — помочь хирургам быстрее и точнее находить истинную границу опухоли, что потенциально улучшит результаты для пациентов.
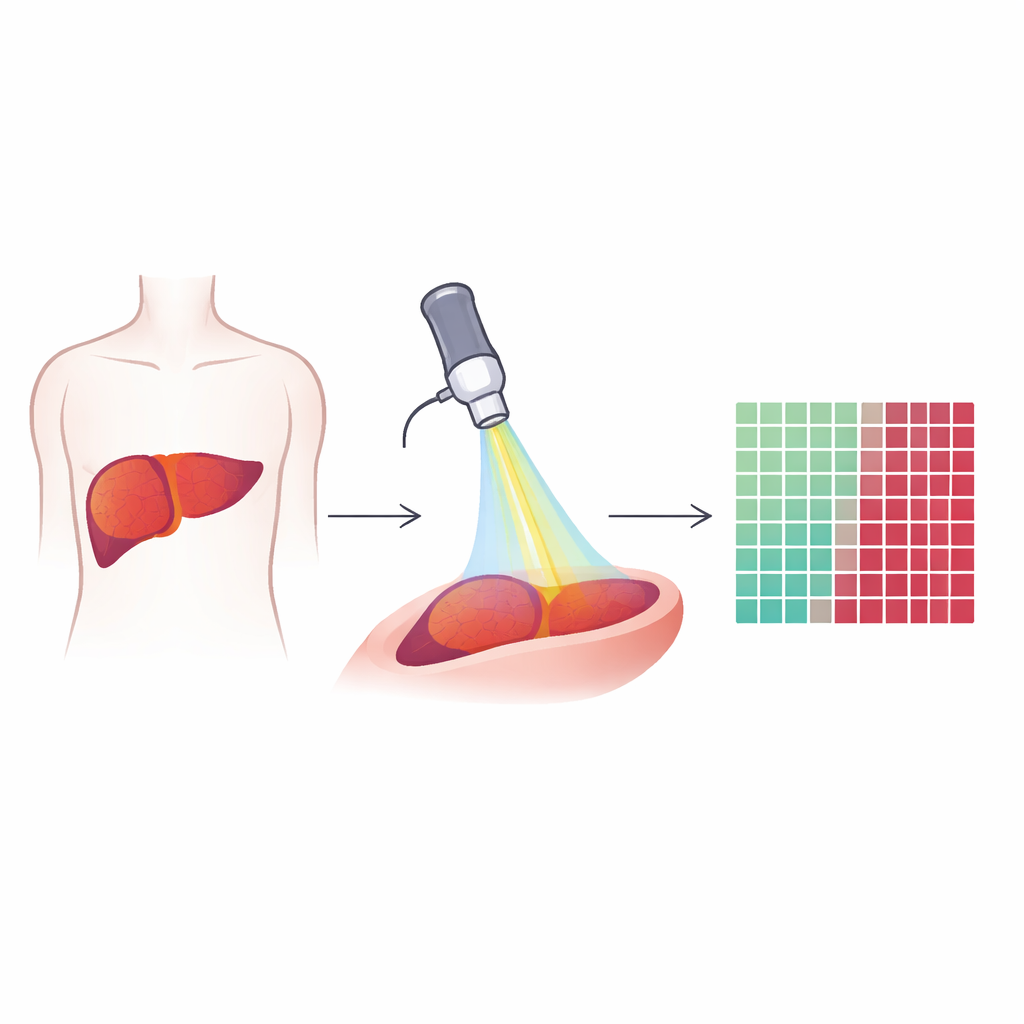
Заглянуть в ткань с помощью особого света
Исследователи использовали метод, называемый мультифотонной микроскопией, основанный на очень коротких лазерных импульсах, которые заставляют естественные молекулы в ткани светиться или генерировать сигналы. Вместо введения красителей или контрастных веществ метод считывает то, что уже присутствует: жиры, коллагеновые волокна и естественно флуоресцирующие вещества внутри клеток. С каждого небольшого поля зрения в образцах печени регистрировали три типа сигналов: один подчёркивал липиды, другой — аутофлуоресценцию молекул, таких как НАДН и витамин A, и третий выявлял жёсткие коллагеновые волокна. Вместе эти сигналы создают цветные, высокоразрешающие изображения, на которых видны как отдельные клетки, так и общая архитектура печени и опухолей.
Фиксация множества вариаций рака печени
Команда исследовала ткани 76 пациентов, перенёсших операцию по поводу рака печени, изучая как саму опухоль, так и окружающую печень. Они показали, что такая микроскопия без меток может воспроизводить классические варианты роста гепатоцеллюлярной карциномы: тонкие или толстые пласты опухолевых клеток, плотные листы и железоподобные структуры. Метод также выявляет изменения в окружающей печени, включая накопление жира и рубцевание — типичные для пациентов с хроническими заболеваниями печени. Важно, что эти паттерны были видны даже при относительно низком разрешении съёмки, сопоставимом с тем, которое могут обеспечить будущие эндоскопические устройства внутри организма. Это говорит о практической применимости подхода в операционной, а не только в лаборатории.
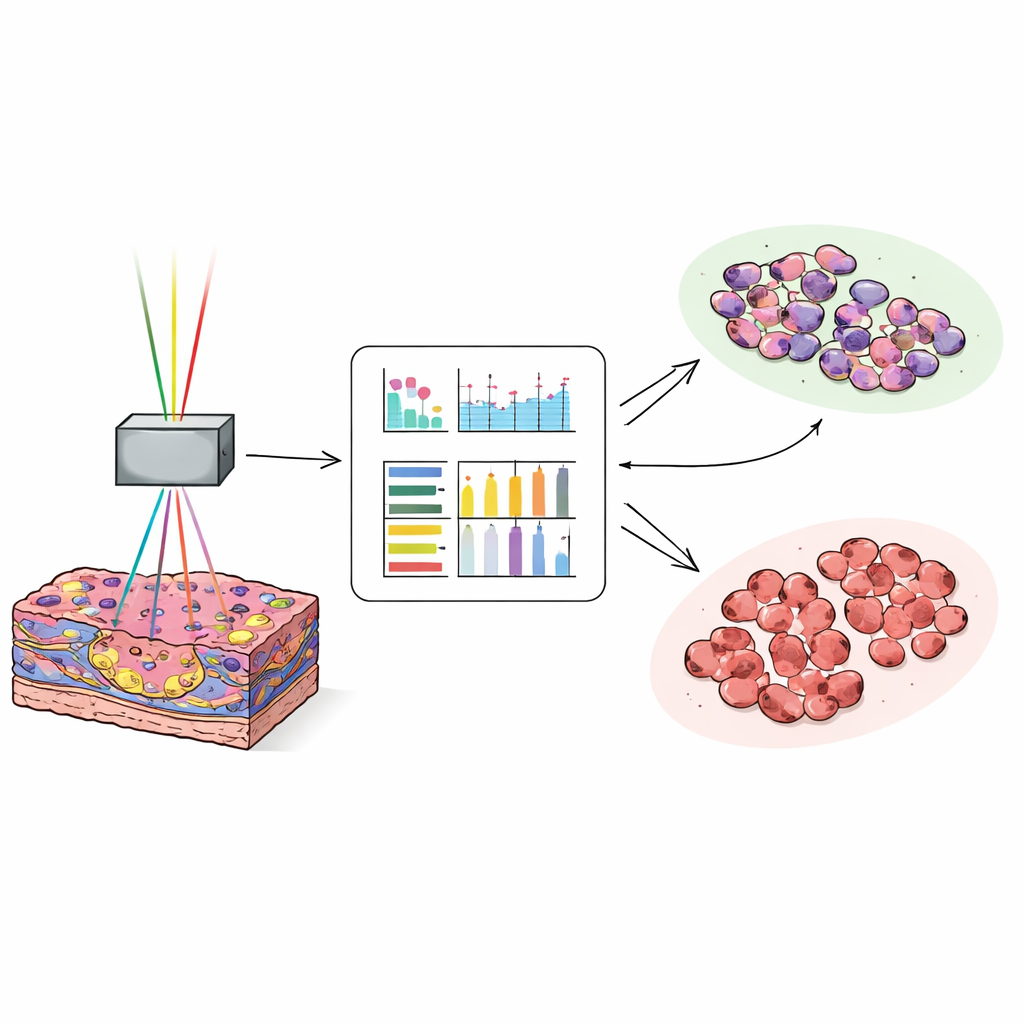
Обучение компьютера находить грань опухоли
Чтобы превратить богатые, но сложные изображения в быстрые решения, учёные преобразовали каждое изображение в набор числовых показателей, описывающих текстуру — насколько гладки, крупнозернисты или разнообразны шаблоны пикселей. Для каждого канала изображения они вычислили по 17 таких измерений и затем обучили нейросеть на примерно 25 000 изображений от 35 пациентов для различения опухолевой ткани и незлокачественной печени. Модель протестировали на ~27 000 новых изображениях от других 38 пациентов. Когда компьютер использовал комбинацию сигналов аутофлуоресценции и чувствительного к коллагену канала, он правильно классифицировал изображения как опухоль или норму примерно в 97 случаях из 100. Даже самые тонко дифференцированные опухоли, которые трудно распознать патологоанатомам на быстрых замороженных срезах, были классифицированы с высокой точностью.
Что световые паттерны рассказывают о раке
Сравнивая разные комбинации сигналов, исследование показало, что наибольшую информативность для отделения рака от нерака несёт аутофлуоресценция. Это свечение обусловлено многими естественными молекулами в клетках и такими структурами, как эластин и коллаген, поэтому оно кодирует плотность клеток, размер и форму ядер (видимые как более тёмные области), жировые капли и строение окружающей ткани. Добавление канала, специфичного к коллагену, дополнительно подчёркивало контраст между опухолью и фоном печени, отражая известные различия в организации волокон и сосудов. Удивительно, но сигнал, ориентированный на липиды, внес меньший вклад в автоматическую классификацию, что даёт практическое преимущество: это может позволить упростить конструкцию прибора, используя один лазерный луч вместо более сложных схем с двумя лучами.
От лабораторного стола к операционной
Чтобы смоделировать реальное хирургическое применение, команда также применила свою лучшую модель к образцам ткани, включающим фактическую границу между опухолью и печенью, создав карты вероятностей, которые выделяли, где опухоль заканчивается, а нормальная ткань начинается. Эти карты в целом хорошо согласовывались с обычной гистологией, хотя участки с высоким содержанием жира или богатые коллагеном иногда сбивали классификатор с толку. Авторы отмечают оставшиеся препятствия до использования этой технологии вживую во время операций, включая ограниченную глубину оптической визуализации, необходимость надёжных стерильных эндоскопов, движение и наличие крови в операционном поле, а также задачу валидации ИИ на больших реальных наборах данных. Тем не менее работа показывает, что мультифотонная визуализация без меток в сочетании с машинным обучением может выступать как быстрый цифровой микроскоп, который однажды поможет хирургам резать более точно и безопасно, повышая шансы полного удаления рака при сохранении максимального объёма здоровой печени.
Цитирование: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Ключевые слова: визуализация рака печени, мультифотонная микроскопия, аутофлуоресценция, хирургические края, машинное обучение