Clear Sky Science · ru
Уточнение взаимосвязи между аффинностью и эффективностью терапевтического IgE
Обращение аллергических антител против рака
Люди, страдающие аллергией, знакомы с силой антител IgE — молекул, которые вызывают зуд в глазах и внезапные чихания. В этом исследовании поставлен неожиданный вопрос: можно ли перенаправить ту же мощную биологию для борьбы с раком, и если да, то как точно следует настраивать эти антитела, чтобы они работали лучше всего? Исследователи сосредоточились на раке молочной железы, который экспрессирует белок HER2, включая случаи с очень низким уровнем HER2, где современные препараты часто неэффективны.
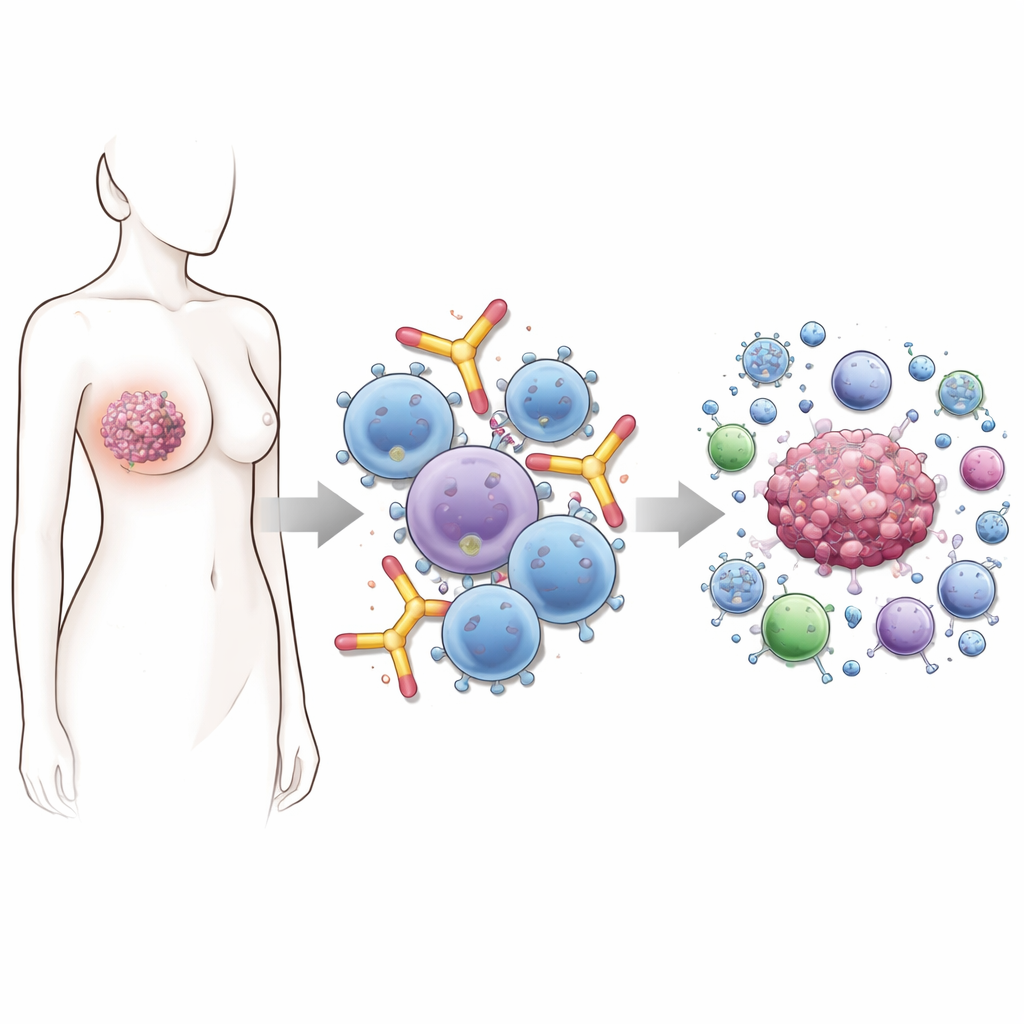
Почему этот класс антител так особенный
Большинство антителовых препаратов на рынке сегодня относятся к классу IgG. Они — «трудяги» современной противораковой терапии, но имеют ограничения — особенно когда опухоли уклоняются от атаки, снижая количество мишенного белка на своей поверхности. Антитела IgE отличаются. Они естественным образом очень крепко связываются с иммунными клетками, такими как тучные клетки, базофилы, моноциты и макрофаги, подготавливая их к быстрой реакции. При аллергии это выражается взрывными реакциями на пыльцу или пищу. В контексте рака та же «проводка» может означать стремительные, сфокусированные атаки на опухолевые клетки, как только IgE встретит свою мишень на поверхности опухоли.
Проектирование более острого IgE, нацеленного на рак
Ранее команда создала антитело IgE под названием EPS 226, которое распознаёт HER2 на раковых клетках молочной железы и способно замедлять рост опухолей в экспериментальных моделях. В этой работе они поставили тонкий, но важный вопрос проектирования: делает ли более сильное «схватывание» HER2 антителом его способность мобилизовать иммунную систему лучше, или же природная «многохватная» связь IgE (авидность) уже выполняет большую часть задачи? Чтобы изучить это, они использовали направленную мутогенезу и селекцию в бактериях, создав миллионы небольших вариаций участка, связывающего HER2, и отобрали 12 новых вариантов IgE, которые связывались с HER2 сильнее, чем исходное антитело.
Испытания на клетках и в животных моделях
Эти улучшенные антитела затем подвергли стресс-тестам в ряде клеточных экспериментов. При загрузке на тучные клетки и контакте с HER2-положительными раковыми клетками большинство более плотносвязывающих IgE вызывали более сильную дегрануляцию — реакцию активации, при которой выделяются мощные иммунные вещества. Один вариант, переименованный в EPS 232, выделялся способностью активировать клетки, при этом эффективно связываясь с HER2 на опухолевых клетках человека и крысы. Дальнейшие испытания показали, что EPS 232 лучше вооружает иммунные клетки для убийства рака: он усиливал цитотоксичность базофилов и способствовал более эффективному фагоцитозу HER2-положительных опухолевых клеток инженерами immune-клетками и первичными человеческими макрофагами. Интересно, что увеличение силы связывания помогало лишь до определённого предела; варианты с чрезвычайно высокой аффинностью не превосходили EPS 232, что указывает на «золотую середину», когда хватка достаточно сильна для эффективности, но не настолько, чтобы ограничивать число антител и иммунных клеток, взаимодействующих с каждой опухолевой клеткой.
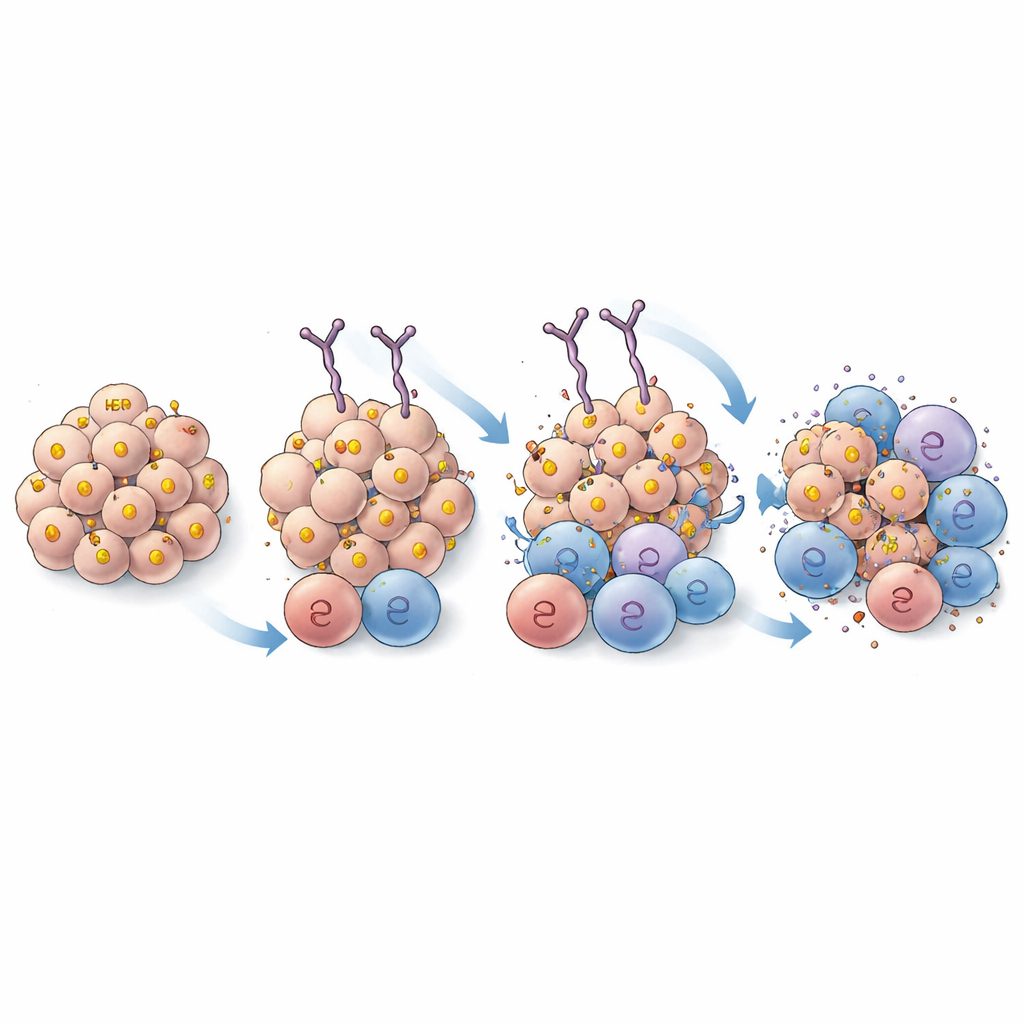
Приближение к тому, как антитело связывается
Чтобы убедиться, что улучшения связаны именно с более сильным захватом, а не с распознаванием новой области HER2, учёные использовали крио-электронную микроскопию высокого разрешения, чтобы визуализировать, как EPS 232 и исходный EPS 226 располагаются на белке HER2. Структуры показали, что оба антитела прикрепляются к одной и той же области HER2 и используют очень похожие точки контакта, с лишь тонкими различиями, которые, как ожидается, не изменяют общую область связывания. Это подтверждает идею, что повышенная эффективность EPS 232 обусловлена улучшенной аффинностью, а не сменой мишени.
От лаборатории к контролю над опухолью
Реальное испытание прошло в животных моделях. У мышей с человеческими опухолями молочной железы при наличии человеческих иммунных клеток EPS 232 замедлял рост опухолей эффективнее и при меньших дозах, чем EPS 226. У крыс с агрессивной моделью рака молочной железы, продуцирующей очень низкие уровни HER2 — аналогично некоторым тройным негативным формам — адаптированная крысинная версия EPS 232 не только сильнее замедляла рост опухолей по сравнению с предшественником, но и продлевала выживание. Опухоли у леченных животных показывали увеличенное инфильтрирование Т‑клетками и макрофагами, что указывает на то, что улучшенное антитело лучше перенастраивает опухолевую среду в сторону, благоприятную для иммунной атаки.
Что это значит для будущих противораковых терапий
Для неспециалиста главный вывод в том, что тонкая настройка того, насколько плотно антитело IgE захватывает свою раковую мишень, может реально повлиять на его эффективность, даже несмотря на то, что IgE уже образует множество одновременных контактов с клетками. Исследование выделяет EPS 232 как ведущего кандидата среди IgE-препаратов против HER2-положительных и HER2‑low раков молочной железы, включая формы, для которых сейчас мало эффективных вариантов лечения. В более широком плане оно показывает, что «аллергоподобные» антитела можно инжинирингово настроить с правильным балансом силы связывания, чтобы превратить систему, склонную к чиханию, в механизм, помогающий иммунной системе находить и уничтожать опухоли.
Цитирование: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Ключевые слова: терапевтический IgE, рак молочной железы HER2, аффинность антител, иммунотерапия рака, тройной негативный рак молочной железы